名校
解题方法
1 . [Cu(NH3)4]SO4·H2O是一种重要的染料及合成农药中间体。下列说法错误的是
| A.阴离子的空间构型是正四面体形 |
| B.中心原子是Cu2+,Cu元素位于周期表d区 |
C. 分子中的键角小于 分子中的键角小于 离子中的键角 离子中的键角 |
| D.1mol该物质中含配位键的数目为4NA |
您最近一年使用:0次
名校
2 . 下面叙述中,正确的是
| A.H2O分子比H2S分子稳定是因为前者分子间存在氢键 |
| B.各1mol的金刚石与SiO2中所含的共价键的数目相同 |
| C.共价晶体的原子间只存在共价键,而分子晶体内只存在范德华力 |
| D.熔点:SiC>NaCl>C60 |
您最近一年使用:0次
名校
3 . 冠醚能与碱金属离子作用,并随环的大小不同而与不同的金属离子作用。12-冠-4与 作用而不与
作用而不与 、
、 作用;18-冠-6与
作用;18-冠-6与 作用(如图),但不与
作用(如图),但不与 或
或 作用。下列说法正确的是
作用。下列说法正确的是
 作用而不与
作用而不与 、
、 作用;18-冠-6与
作用;18-冠-6与 作用(如图),但不与
作用(如图),但不与 或
或 作用。下列说法正确的是
作用。下列说法正确的是
| A.冠醚可作为一些有机反应中的相转移催化剂,与其能与碱金属阳离子作用有关 |
B.18-冠-6与 作用,不与 作用,不与 或 或 作用,这体现了超分子的“自组装”的特征 作用,这体现了超分子的“自组装”的特征 |
C.18-冠-6中O原子与 间存在离子键 间存在离子键 |
| D.18-冠-6分子具有旋光性 |
您最近一年使用:0次
4 . 铍的氧化物广泛应用于原子能、航天、电子、陶瓷等领域,是重要的战略物资。利用绿柱石(主要化学成分为 ,还含有一定量的
,还含有一定量的 和
和 )生产
)生产 的一种工艺流程如下。
的一种工艺流程如下。
①绿柱石主要化学成分写成氧化物的形式为: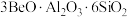
② 与
与 在周期表位置符合对角线规则,
在周期表位置符合对角线规则, 与
与 性质相似,
性质相似, 与
与 性质相似
性质相似
③ 被沉淀完全的
被沉淀完全的 ;
;
回答问题:
(1)粉碎的目的是______ ;
(2)无水 可用作聚合反应的催化剂。
可用作聚合反应的催化剂。 、
、 与
与 在600~800℃制备
在600~800℃制备 且生成一种毒性气体,化学方程式为
且生成一种毒性气体,化学方程式为_____ 。
(3)残渣主要成分是(填化学式)_____ 。浸取中浓硫酸的作用除了用于溶解矿石外,还起的作用_____ ;
(4)该流程中能循环使用的物质是_____ (填化学式)。
(5)沉铍时,用氢氧化钠溶液代替氨水得到 的量可能减少,用离子方程说明理由
的量可能减少,用离子方程说明理由_____ 。
(6)wg绿柱石( 含量14%)经过一系列反应后得到
含量14%)经过一系列反应后得到 ag(纯度90%),则
ag(纯度90%),则 的产率为
的产率为_____ 。
 ,还含有一定量的
,还含有一定量的 和
和 )生产
)生产 的一种工艺流程如下。
的一种工艺流程如下。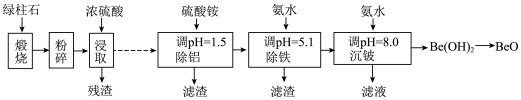
①绿柱石主要化学成分写成氧化物的形式为:
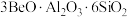
②
 与
与 在周期表位置符合对角线规则,
在周期表位置符合对角线规则, 与
与 性质相似,
性质相似, 与
与 性质相似
性质相似③
 被沉淀完全的
被沉淀完全的 ;
;回答问题:
(1)粉碎的目的是
(2)无水
 可用作聚合反应的催化剂。
可用作聚合反应的催化剂。 、
、 与
与 在600~800℃制备
在600~800℃制备 且生成一种毒性气体,化学方程式为
且生成一种毒性气体,化学方程式为(3)残渣主要成分是(填化学式)
(4)该流程中能循环使用的物质是
(5)沉铍时,用氢氧化钠溶液代替氨水得到
 的量可能减少,用离子方程说明理由
的量可能减少,用离子方程说明理由(6)wg绿柱石(
 含量14%)经过一系列反应后得到
含量14%)经过一系列反应后得到 ag(纯度90%),则
ag(纯度90%),则 的产率为
的产率为
您最近一年使用:0次
名校
5 .  的配位化合物较稳定且运用广泛。它可与
的配位化合物较稳定且运用广泛。它可与 、
、 、
、 、
、 等形成配离子使溶液显色。如:显浅紫色的
等形成配离子使溶液显色。如:显浅紫色的 、红色的
、红色的 、黄色的
、黄色的 、无色的
、无色的 。某同学按如下步骤完成实验:
。某同学按如下步骤完成实验:

下列说法不正确的是
 的配位化合物较稳定且运用广泛。它可与
的配位化合物较稳定且运用广泛。它可与 、
、 、
、 、
、 等形成配离子使溶液显色。如:显浅紫色的
等形成配离子使溶液显色。如:显浅紫色的 、红色的
、红色的 、黄色的
、黄色的 、无色的
、无色的 。某同学按如下步骤完成实验:
。某同学按如下步骤完成实验:
下列说法不正确的是
A.为了能观察到溶液Ⅰ中 的颜色,可向该溶液中加入稀盐酸 的颜色,可向该溶液中加入稀盐酸 |
B.溶液Ⅰ呈黄色可能是由 水解产物的颜色引起的 水解产物的颜色引起的 |
C. 与 与 的配位能力强于 的配位能力强于 |
| D.向溶液Ⅲ中加入足量的KSCN固体,溶液可能再次变为红色 |
您最近一年使用:0次
名校
6 . 制取催化剂 的原理为:
的原理为: 。下列说法错误的是
。下列说法错误的是
 的原理为:
的原理为: 。下列说法错误的是
。下列说法错误的是A.基态碳原子价电子轨道表示式为 |
B. 中3p-3p轨道重叠示意图为 中3p-3p轨道重叠示意图为 |
C. 为非极性分子 为非极性分子 |
D.CO电子式为: |
您最近一年使用:0次
名校
7 . 下列关于原子核外电子排布与元素在周期表中位置关系的表述正确的是
A.原子的价电子排布式为 的元素一定是主族元素 的元素一定是主族元素 |
| B.基态原子的p能级上有5个电子的元素一定是第ⅦA族元素 |
C.原子的价电子排布式为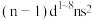 的元素一定位于第ⅢB~第ⅧB族 的元素一定位于第ⅢB~第ⅧB族 |
| D.基态原子的N层上只有1个电子的元素一定是主族元素 |
您最近一年使用:0次
8 . 下列描述正确的是
A.在中性条件下可用KSCN溶液检验补铁剂中是否含有 |
| B.可用核磁共振法测定出青蒿素的相对分子质量 |
| C.液晶属于晶体的一种,可用于制造液晶显示器 |
D. 、石墨烯、碳纳米管都是碳的同素异形体,是纳米材料中的“明星” 、石墨烯、碳纳米管都是碳的同素异形体,是纳米材料中的“明星” |
您最近一年使用:0次
名校
9 . 有A、B、C、D、E5种元素,它们的核电荷数依次增大,且都小于20.其中只有C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为 ;B和D也属同一族,它们原子最外层的p能级电子数是最外层的s能级电子数的两倍;C基态原子占据两种形状的原子轨道,且两种形状轨道中的电子总数均相同。
;B和D也属同一族,它们原子最外层的p能级电子数是最外层的s能级电子数的两倍;C基态原子占据两种形状的原子轨道,且两种形状轨道中的电子总数均相同。
请回答下列问题:
(1)C是_______ (填元素名称)。
(2)上述元素中位于s区的有_______ (填元素符号)。
(3)与 互为等电子体的阴离子为
互为等电子体的阴离子为_______ 。
(4)已知C的氧化物CO与NiO的晶体结构相同,其中 和
和 的离子半径分别为66pm和69pm,则熔点:CO
的离子半径分别为66pm和69pm,则熔点:CO_____ NiO(填“>”“<”或“=”)。
(5)浸金时,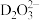 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成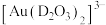 。
。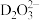 中的配位原子为
中的配位原子为_____ (填元素符号),其位置在______ (填“中心”或“端位”),理由是______ 。
 ;B和D也属同一族,它们原子最外层的p能级电子数是最外层的s能级电子数的两倍;C基态原子占据两种形状的原子轨道,且两种形状轨道中的电子总数均相同。
;B和D也属同一族,它们原子最外层的p能级电子数是最外层的s能级电子数的两倍;C基态原子占据两种形状的原子轨道,且两种形状轨道中的电子总数均相同。请回答下列问题:
(1)C是
(2)上述元素中位于s区的有
(3)与
 互为等电子体的阴离子为
互为等电子体的阴离子为(4)已知C的氧化物CO与NiO的晶体结构相同,其中
 和
和 的离子半径分别为66pm和69pm,则熔点:CO
的离子半径分别为66pm和69pm,则熔点:CO(5)浸金时,
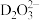 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成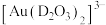 。
。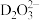 中的配位原子为
中的配位原子为
您最近一年使用:0次
名校
10 . 对于物质的结构与性质描述中,前者大于后者的是
| 结构与性质 | 前者 | 后者 | |
| A | 熔点 | 碳化硅 | 晶体硅 |
| B | 沸点 |
|
|
| C | 分子的极性 |  |  |
| D | 在水中的溶解度 |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次