名校
1 . 设 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是A.1mol甲基(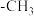 )的电子数为9 )的电子数为9 |
B.60g  晶体中含Si-O键的数目为4 晶体中含Si-O键的数目为4 |
C.1mol  分子中,S原子的价层电子对数目为2 分子中,S原子的价层电子对数目为2 |
D.标准状况下,22.4L乙烷中含有的极性键的数目为6 |
您最近一年使用:0次
名校
2 . 下列有关化学用语表示正确的是
A.全氟丙烷的球棍模型: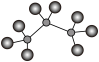 |
B.基态溴原子的简化电子排布式: |
C.乙烯的结构简式: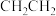 |
D. 的电子式: 的电子式: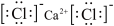 |
您最近一年使用:0次
名校
3 . 化学与生活紧密相关,下列说法错误的是
| A.霓虹灯的发光原理与氢原子光谱形成的原理基本相同 |
| B.碳纳米材料属于新型无机非金属材料,是一种新型化合物 |
| C.羊毛织品水洗后变形,与蛋白质结构改变有关,即原先部位的氢键发生移动 |
| D.壁虎的足与墙体之间的作用力,本质上是足上的细毛与墙体之间的范德华力 |
您最近一年使用:0次
名校
4 . 甲硝唑主要用作治疗或预防厌氧菌引起的系统或局部感染,结构简式如图所示,杂环中存在大 键。下列说法错误的是
键。下列说法错误的是
 键。下列说法错误的是
键。下列说法错误的是
A.该分子中①号 更易和盐酸形成盐,增大药物水溶性 更易和盐酸形成盐,增大药物水溶性 |
| B.该分子可发生加成反应、消去反应 |
| C.该分子中含有两种含氧官能团 |
| D.该分子是极性分子 |
您最近一年使用:0次
名校
5 . 下列化学用语表达正确的是
A.乙酸的分子式: | B. 的电子式: 的电子式: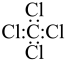 |
C.甲烷分子的空间填充模型: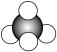 | D.乙烯的结构简式: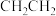 |
您最近一年使用:0次
6 . 下列化学用语正确的是
A.乙烯分子的空间填充模型: |
B.甲基的电子式: |
C.聚丙烯的结构简式: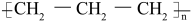 |
D.烷烃的通式: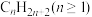 |
您最近一年使用:0次
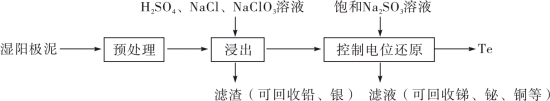
7 . 碲(Te)是一种重要的稀有分散元素,广泛应用于冶金、石油、化工、航空、电子等领域。以某冶炼厂的湿阳极泥(含水26%,主要含锑、砷、铅、铋、银和少量铜、碲等)为原料回收碲的流程如下:
请回答下列问题:
(1)52Te的基态原子的电子排布式为___________ 。
(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是_______________ ;氧化后的原料还需粉碎、过筛,目的是_________________ 。
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为___________ 、___________ ;添加 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式________________ 。
(4)电解时为防止除Te以外的单质生成,需控制电位的范围为___________ ;加入饱和Na2SO3溶液还原 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成_____________ (填化学式)。
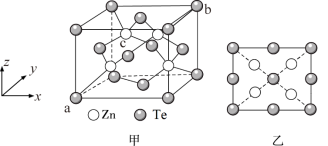
(5)将碲与锌一起加热,然后升华可制得碲化锌。碲化锌是一种重要的半导体材料,图甲为它的一种立方晶胞结构,图乙为该晶胞沿z轴投影图。已知a点的坐标为(0,0,0),b点的坐标为(1,1,1),则c点的坐标为_______________ ,设ZnTe的摩尔质量为M,阿伏加德罗常数的值为NA,密度为dg/cm3,则Zn与Te最近距离为___________ nm(列出计算式即可)。
物质 |
|
|
|
|
|
氧化还原电位(E)/V | 0.342 | 0.568 | 0.16 | 小于0.16 | 小于0.16 |
(1)52Te的基态原子的电子排布式为
(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为
 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式(4)电解时为防止除Te以外的单质生成,需控制电位的范围为
 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成(5)将碲与锌一起加热,然后升华可制得碲化锌。碲化锌是一种重要的半导体材料,图甲为它的一种立方晶胞结构,图乙为该晶胞沿z轴投影图。已知a点的坐标为(0,0,0),b点的坐标为(1,1,1),则c点的坐标为
您最近一年使用:0次
7日内更新
|
53次组卷
|
2卷引用:福建省永春一中2023-2024学年高三化学最后一卷试卷
名校
解题方法
8 . 叠氮化钠 是汽车安全气囊的气体发生剂,可由
是汽车安全气囊的气体发生剂,可由 和氨基钠
和氨基钠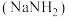 为原料加热制得,某小组对
为原料加热制得,某小组对 的制备和产品纯度测定进行相关探究。回答下列问题。
的制备和产品纯度测定进行相关探究。回答下列问题。
查阅资料:部分物质及性质
Ⅰ.制备
 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(2)按气流方向,仪器口的连接顺序为a→___________ →h.
(3)装置B的生成物中除了 和
和 外,还有一种生成物是
外,还有一种生成物是___________ (填化学式)。
(4)在装置E中将氮元素转化为对环境无污染的气体,同时生成 沉淀,发生反应的化学方程式为
沉淀,发生反应的化学方程式为___________ 。
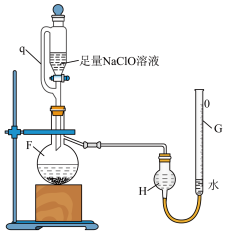
Ⅱ.用如图所示装置测定产品纯度。___________ ,恒压分液漏斗中侧管q的作用除平衡气压有利于液体顺利流下外,还有___________ 。
(6)取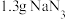 样品与足量的
样品与足量的 反应(杂质不与
反应(杂质不与 溶液反应),利用如图装置测量所得氮气的体积,初始时G、H两液面相平,G管的读数为
溶液反应),利用如图装置测量所得氮气的体积,初始时G、H两液面相平,G管的读数为 ,充分反应后,恢复至室温,移动G使两液面再次相平,G管读数为
,充分反应后,恢复至室温,移动G使两液面再次相平,G管读数为 (其中
(其中 ),则产品中
),则产品中 的质量分数为
的质量分数为___________ %(本实验条件下气体摩尔体积为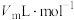 )。
)。
 是汽车安全气囊的气体发生剂,可由
是汽车安全气囊的气体发生剂,可由 和氨基钠
和氨基钠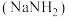 为原料加热制得,某小组对
为原料加热制得,某小组对 的制备和产品纯度测定进行相关探究。回答下列问题。
的制备和产品纯度测定进行相关探究。回答下列问题。查阅资料:部分物质及性质
| 物质 | 氨基钠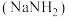 |  |  |
| 性质 | 易氧化、易潮解 | 遇强酸易爆炸 | 有强氧化性,与酸、碱不反应 |


 ,反应的离子方程式为
,反应的离子方程式为(2)按气流方向,仪器口的连接顺序为a→
(3)装置B的生成物中除了
 和
和 外,还有一种生成物是
外,还有一种生成物是(4)在装置E中将氮元素转化为对环境无污染的气体,同时生成
 沉淀,发生反应的化学方程式为
沉淀,发生反应的化学方程式为Ⅱ.用如图所示装置测定产品纯度。
(6)取
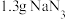 样品与足量的
样品与足量的 反应(杂质不与
反应(杂质不与 溶液反应),利用如图装置测量所得氮气的体积,初始时G、H两液面相平,G管的读数为
溶液反应),利用如图装置测量所得氮气的体积,初始时G、H两液面相平,G管的读数为 ,充分反应后,恢复至室温,移动G使两液面再次相平,G管读数为
,充分反应后,恢复至室温,移动G使两液面再次相平,G管读数为 (其中
(其中 ),则产品中
),则产品中 的质量分数为
的质量分数为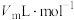 )。
)。
您最近一年使用:0次
名校
9 . 工业上用 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。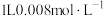 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。
 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
A.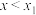 时, 时, 主要被氧化为 主要被氧化为 |
B.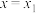 时,生成的 时,生成的 的物质的量为 的物质的量为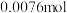 |
C.生成硝氮的离子方程式: |
D. 时,分批加入 时,分批加入 可以降低总氮残余率 可以降低总氮残余率 |
您最近一年使用:0次

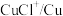

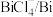
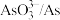
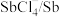
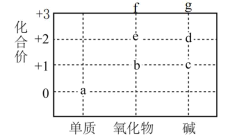
 反应可以生成c
反应可以生成c 溶液可检验f中是否含有e
溶液可检验f中是否含有e

