名校
解题方法
1 . 物质结构的知识被科学家应用于各个科学领域,如医药、材料、染料等,造福着人类。下列说法不正确的是
| A.微波炉的工作原理是微波对食物中的极性分子产生作用 |
| B.石墨的导电性具有一定的方向性 |
| C.DNA的双螺旋结构靠大量氢键相连而稳定存在于生命体中 |
D.铁血红素分子中都以 与原卟啉环形成配合物的形式存在 与原卟啉环形成配合物的形式存在 |
您最近一年使用:0次
名校
2 . 冠醚是一种超分子,它是由多个二元醇分子之间脱水形成的环状化合物。18—冠—6可用作相转移催化其与 形成的螯合离子结构如图所示。下列说法正确的是
形成的螯合离子结构如图所示。下列说法正确的是
 形成的螯合离子结构如图所示。下列说法正确的是
形成的螯合离子结构如图所示。下列说法正确的是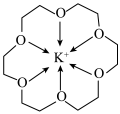
| A.该螯合离子形成的晶体类型为分子晶体 |
B.与二甲醚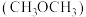 相比,该整合离子中“C-O-C”键角更大 相比,该整合离子中“C-O-C”键角更大 |
| C.该螯合离子中碳原子与氧原子杂化类型不同 |
| D.该螯合离子中所有非氢原子可以位于同一平面 |
您最近一年使用:0次
名校
3 . 一种抗癫痫药物的合成中间体的结构如图所示,下列关于该有机物的说法正确的是
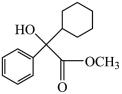
| A.属于芳香烃 | B.分子式为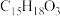 |
| C.苯环上的一氯代物有3种 | D.分子中含有2个手性碳原子 |
您最近一年使用:0次
名校
4 . 一种有机物催化剂由原子序数依次递增的前20号元素X、Y、Z、W、M组成,结构式如图。下列说法错误的是
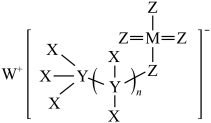
| A.简单离子半径:M>Z>W |
| B.简单气态氢化物稳定性:Z>Y |
| C.基态M原子核外有5种不同能量的电子 |
| D.Z元素所在周期中,第一电离能大于Z的元素有2种 |
您最近一年使用:0次
5 . 为了方便和环保,煤应综合利用,干馏是较易实现的成熟方式。如下叙述不正确的是
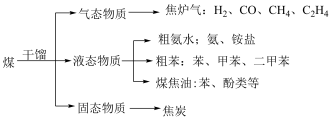
| A.煤的干馏属于化学变化,由粗苯获得甲苯属于物理变化 |
| B.煤的主要成分是炭和苯等 |
| C.粗氨水可以用于制化肥 |
| D.焦炭可用于炼铁 |
您最近一年使用:0次
名校
解题方法
6 . I.有一块镀铜的铁制品,已严重锈蚀[铜锈成分视为 ],铁锈成分视为
],铁锈成分视为 ],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
(1)气体甲的成分是___________ (填化学式),固体乙的成分是___________ (填名称)。
(2)铁发生的反应属于四种基本反应类型中的___________ 。
(3)滤液丙的颜色可能是___________(选填编号)。
(4)确认滤液丙中是否含有亚铁离子,适宜的试剂是___________(选填编号)。
Ⅱ.铁与不同浓度硝酸反应时主要还原产物不同。现将过量铁与一定浓度的硝酸充分反应,测得消耗的铁与被还原的硝酸的物质的量之比为 。
。
(5)假若反应生成的还原产物只有一种,则还原产物是___________ 。
(6)所得溶液与碳酸氢铵溶液混合可获得碳酸亚铁沉淀,同时有气体生成。写出反应生成碳酸亚铁的离子方程式___________ 。
 ],铁锈成分视为
],铁锈成分视为 ],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。(1)气体甲的成分是
(2)铁发生的反应属于四种基本反应类型中的
(3)滤液丙的颜色可能是___________(选填编号)。
| A.棕黄色 | B.蓝色 | C.浅绿色 | D.无色 |
A. 溶液 溶液 | B.NaOH溶液 |
C.KSCN溶液和 溶液 溶液 | D. 淀粉试纸 淀粉试纸 |
Ⅱ.铁与不同浓度硝酸反应时主要还原产物不同。现将过量铁与一定浓度的硝酸充分反应,测得消耗的铁与被还原的硝酸的物质的量之比为
 。
。(5)假若反应生成的还原产物只有一种,则还原产物是
(6)所得溶液与碳酸氢铵溶液混合可获得碳酸亚铁沉淀,同时有气体生成。写出反应生成碳酸亚铁的离子方程式
您最近一年使用:0次
7 . 硝酸银是常用化学试剂,见光或受热会分解。某兴趣小组开展以下探究活动。
I.资料查阅
①AgOH不稳定,极易分解生成 和
和 。
。
②氧化银为棕黑色粉末,难溶于水,可溶于氨水和稀硝酸,见光或200℃左右分解为单质。
③银晶体是银白色金属光泽的固体,粉末是黑色固体,与硝酸反应的情况和铜类似。
Ⅱ.久置的硝酸银溶液底部有黑色固体甲,探究甲的成分
【猜想】固体甲中含有Ag、 中的一种或两种。
中的一种或两种。
【实验】i.取少量固体甲于试管中,加入过量稀硝酸振荡;
ii.另取少量固体甲于试管中,加入过量氨水振荡。
【结论】固体甲为Ag和 的混合物。
的混合物。
(1)①步骤i反应的离子方程式___________ 。
②写出步骤ii观察到的现象为___________ 。
【应用】
(2)实验室保存硝酸银溶液采取的措施为___________ (写出两条)。
Ⅲ.利用如图装置探究硝酸银固体受热分解的产物 至
至___________ (填现象)后再加热。
(4)加热后观察到实验现象:A中有银白色金属光泽的固体生成,出现红棕色气体。A中反应的化学方程式为___________ 。
(5)停止加热后,应再通入 一段时间再拆卸装置,目的是防止倒吸、避免固体产物与空气反应、
一段时间再拆卸装置,目的是防止倒吸、避免固体产物与空气反应、___________ 。
I.资料查阅
①AgOH不稳定,极易分解生成
 和
和 。
。②氧化银为棕黑色粉末,难溶于水,可溶于氨水和稀硝酸,见光或200℃左右分解为单质。
③银晶体是银白色金属光泽的固体,粉末是黑色固体,与硝酸反应的情况和铜类似。
Ⅱ.久置的硝酸银溶液底部有黑色固体甲,探究甲的成分
【猜想】固体甲中含有Ag、
 中的一种或两种。
中的一种或两种。【实验】i.取少量固体甲于试管中,加入过量稀硝酸振荡;
ii.另取少量固体甲于试管中,加入过量氨水振荡。
【结论】固体甲为Ag和
 的混合物。
的混合物。(1)①步骤i反应的离子方程式
②写出步骤ii观察到的现象为
【应用】
(2)实验室保存硝酸银溶液采取的措施为
Ⅲ.利用如图装置探究硝酸银固体受热分解的产物
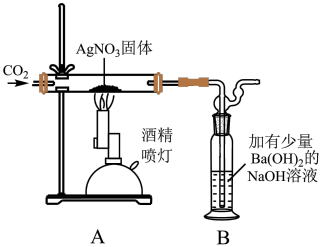
 至
至(4)加热后观察到实验现象:A中有银白色金属光泽的固体生成,出现红棕色气体。A中反应的化学方程式为
(5)停止加热后,应再通入
 一段时间再拆卸装置,目的是防止倒吸、避免固体产物与空气反应、
一段时间再拆卸装置,目的是防止倒吸、避免固体产物与空气反应、
您最近一年使用:0次
名校
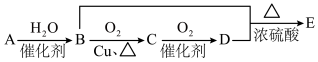
8 . 有机物A-E有如下转化关系,A是最简单的不饱和烃,B和D可做食品调味剂,E有浓郁香味。回答下列问题,___________ 。
(2)B的官能团名称是___________ 。
(3)A至E中属于电解质的物质的电离方程式是___________ 。
(4)以下物质与B溶液、D溶液作用有明显不同现象的是___________。
(5)如上转化中涉及多种反应类型,写出属于取代反应的化学方程式___________ 。
(6)E有较多的同分异构体,写出其中一种含有 和
和 的结构简式
的结构简式___________ 。
(7)A与苯反应生成乙苯: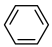

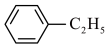 ,反应类型是
,反应类型是___________ 。
(2)B的官能团名称是
(3)A至E中属于电解质的物质的电离方程式是
(4)以下物质与B溶液、D溶液作用有明显不同现象的是___________。
| A.NaOH溶液 | B.NaHCO3溶液 | C.紫色石蕊试液 | D.苯 |
(5)如上转化中涉及多种反应类型,写出属于取代反应的化学方程式
(6)E有较多的同分异构体,写出其中一种含有
 和
和 的结构简式
的结构简式(7)A与苯反应生成乙苯:


 ,反应类型是
,反应类型是
您最近一年使用:0次
名校
9 . 铜与稀硝酸反应慢,与铁离子反应快。某同学认为铁离子可催化铜与稀硝酸的反应,特设计如下验证实验:
如下有关说明正确的是
| 操作 | 现象 | |
| I | 颗粒均匀的铜粉均分为三份 | |
| Ⅱ | 取 溶液于试管中,调节 溶液于试管中,调节 ,加入第一份铜粉 ,加入第一份铜粉 | 铜粉溶解,溶液变为深棕色[是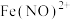 的颜色] 的颜色] |
| Ⅲ | 取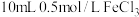 溶液于试管中,调节 溶液于试管中,调节 ,加入第二份铜粉 ,加入第二份铜粉 | 铜粉溶解,溶液变为蓝绿色 |
| IV | 取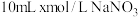 溶液于试管中,调节 溶液于试管中,调节 ,加入第三份铜粉 ,加入第三份铜粉 | 观察10分钟没有明显现象 |
A.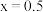 |
| B.若加入的铜足量,实验Ⅱ和Ⅲ溶解的铜一样多 |
C.该实验条件下氧化性强弱: |
| D.往实验IV中加硫酸亚铁也能较快观察到铜溶解现象 |
您最近一年使用:0次
名校
10 . 在101kPa、60℃下,2个烧瓶分别装有如下表的气体,按如图装置进行喷泉实验。下列叙述正确的是

| 实验编号 | 甲 | 乙 |
| 气体成分 | 200mL NH3和50mL空气 | 200mL NO2和50mL空气 |
| A.实验过程中,甲、乙都发生化学反应 |
| B.乙中最后的剩余气体显红棕色 |
| C.实验所得两溶液,溶质的物质的量浓度一定相同 |
| D.甲中如果没有空气,所得溶液溶质的物质的量浓度更大 |
您最近一年使用:0次



