1 . 化学渗透在社会生活的各个方面。下列叙述错误的是
| A.宇航员餐食中的油脂属于天然高分子化合物 |
| B.用于制作飞机轴承的氮化硅陶瓷材料是新型无机非金属材料 |
C.“九章三号”光量子计算原型机所用芯片的主要成分 能溶于 能溶于 溶液 溶液 |
| D.稀土永磁材料是电子技术通信中的重要材料,稀土元素均为金属元素 |
您最近一年使用:0次
解题方法
2 . 氧化锌在橡胶、油漆涂料、化工、医疗及食品等行业有着广泛应用。一种由含锌烟灰(含有ZnO、CuO、PbO、FeO、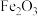 、MnO、
、MnO、 、CdO等)制备氧化锌的工艺流程如图所示。
、CdO等)制备氧化锌的工艺流程如图所示。
(ⅱ)二价金属氧化物能分别与氨形成配位化合物,如Fe(Ⅱ)、Mn(Ⅱ)可生成 、
、 ;
;
(ⅲ)Fe、Mn元素对应优势微粒与溶液的pH及氧化剂氧化电位(Eh)关系如图: 见下表:
见下表:
回答下列问题:
(1)O的价电子排布图为___________ ,Zn在周期表中的位置是___________ 。
(2)“氧化预处理”时,加入 溶液的目的为氧化含锌烟灰中的铁(Ⅱ)和锰(Ⅱ),则氧化产物为
溶液的目的为氧化含锌烟灰中的铁(Ⅱ)和锰(Ⅱ),则氧化产物为___________ 。
(3)“浸出”阶段溶解ZnO时消耗的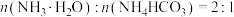 ,写出该反应的离子方程式
,写出该反应的离子方程式___________ 。
(4)“深度净化”时,可采用以下两种方案:
方案甲:加入足量锌粉。该方案所得滤渣c中除了含Zn、Cd之外,还含有___________ (填化学式)。
方案乙:加入 粉末。已知杂质离子浓度较为接近且远小于含锌离子的浓度。则杂质离子生成沉淀的先后顺序依次为
粉末。已知杂质离子浓度较为接近且远小于含锌离子的浓度。则杂质离子生成沉淀的先后顺序依次为___________ (写沉淀的化学式);工业生产中常采用方案甲而不采用方案乙,其原因为___________ 。
(5)“蒸氨”时得到混合气体e和固体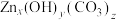 。混合气体e可返回至
。混合气体e可返回至___________ 工序循环利用。
(6)氧化锌有六边纤锌矿和立方闪锌矿两种常见晶体结构,晶胞结构如图。___________ 。
②原子1的分数坐标为 ,则原子2的分数坐标为
,则原子2的分数坐标为___________ 。
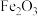 、MnO、
、MnO、 、CdO等)制备氧化锌的工艺流程如图所示。
、CdO等)制备氧化锌的工艺流程如图所示。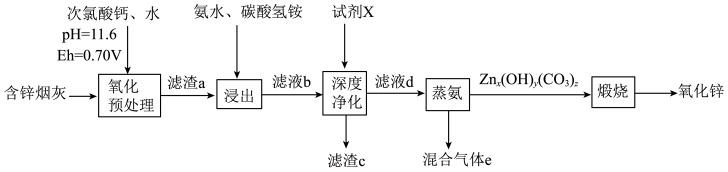
(ⅱ)二价金属氧化物能分别与氨形成配位化合物,如Fe(Ⅱ)、Mn(Ⅱ)可生成
 、
、 ;
;(ⅲ)Fe、Mn元素对应优势微粒与溶液的pH及氧化剂氧化电位(Eh)关系如图:

 见下表:
见下表:| 物质 | MnS | FeS | ZnS | PbS | CdS | CuS |
 | 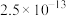 |  |  | 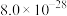 | 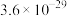 |  |
(1)O的价电子排布图为
(2)“氧化预处理”时,加入
 溶液的目的为氧化含锌烟灰中的铁(Ⅱ)和锰(Ⅱ),则氧化产物为
溶液的目的为氧化含锌烟灰中的铁(Ⅱ)和锰(Ⅱ),则氧化产物为(3)“浸出”阶段溶解ZnO时消耗的
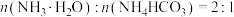 ,写出该反应的离子方程式
,写出该反应的离子方程式(4)“深度净化”时,可采用以下两种方案:
方案甲:加入足量锌粉。该方案所得滤渣c中除了含Zn、Cd之外,还含有
方案乙:加入
 粉末。已知杂质离子浓度较为接近且远小于含锌离子的浓度。则杂质离子生成沉淀的先后顺序依次为
粉末。已知杂质离子浓度较为接近且远小于含锌离子的浓度。则杂质离子生成沉淀的先后顺序依次为(5)“蒸氨”时得到混合气体e和固体
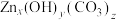 。混合气体e可返回至
。混合气体e可返回至(6)氧化锌有六边纤锌矿和立方闪锌矿两种常见晶体结构,晶胞结构如图。
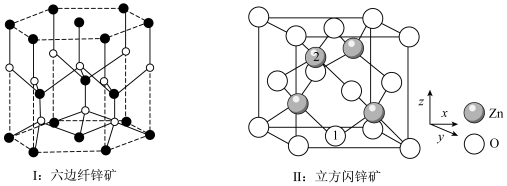
②原子1的分数坐标为
 ,则原子2的分数坐标为
,则原子2的分数坐标为
您最近一年使用:0次
2024-05-14更新
|
66次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
3 . 硫酸工业在国民经济中占有重要地位。
(1)我国古籍记载了硫酸的制备方法-“炼石胆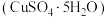 取精华法”。借助现代仪器分析,该制备过程中
取精华法”。借助现代仪器分析,该制备过程中 分解的TG曲线(热重)及DSC曲线如下图所示,DSC图中,吸热效应呈现向下凸起的峰(热焓增加),放热效应反之,则700℃左右有二个吸热峰,此时分解生成的氧化物有
分解的TG曲线(热重)及DSC曲线如下图所示,DSC图中,吸热效应呈现向下凸起的峰(热焓增加),放热效应反之,则700℃左右有二个吸热峰,此时分解生成的氧化物有___________ 种。875℃左右的吸热峰表示化学反应的方程式为___________ 。
①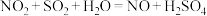 (慢反应) ②
(慢反应) ② (快反应)
(快反应)
(ⅰ)上述过程中 的作用为
的作用为___________ 。其中反应___________ (填“①”或“②”)是该反应的决速步。
(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是___________ (答出两点即可)。
(3)接触法制硫酸的关键反应为 的催化氧化:
的催化氧化:
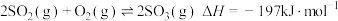
(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如图所示,下列说法不正确的是___________ 。
b.α=0.88的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同α下的最大速率,选择最佳生产温度
(ⅱ)设 的平衡分压为p,
的平衡分压为p, 的平衡转化率为b,用含p和b的代数式表示上述催化氧化反应的
的平衡转化率为b,用含p和b的代数式表示上述催化氧化反应的
___________ (用平衡分压代替平衡浓度计算)。
(4)二氧化硫一空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。___________ ;
(ⅱ)相同条件下,放电过程中消耗的 和
和 的体积比为
的体积比为___________ 。
(1)我国古籍记载了硫酸的制备方法-“炼石胆
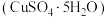 取精华法”。借助现代仪器分析,该制备过程中
取精华法”。借助现代仪器分析,该制备过程中 分解的TG曲线(热重)及DSC曲线如下图所示,DSC图中,吸热效应呈现向下凸起的峰(热焓增加),放热效应反之,则700℃左右有二个吸热峰,此时分解生成的氧化物有
分解的TG曲线(热重)及DSC曲线如下图所示,DSC图中,吸热效应呈现向下凸起的峰(热焓增加),放热效应反之,则700℃左右有二个吸热峰,此时分解生成的氧化物有
①
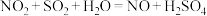 (慢反应) ②
(慢反应) ② (快反应)
(快反应)(ⅰ)上述过程中
 的作用为
的作用为(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是
(3)接触法制硫酸的关键反应为
 的催化氧化:
的催化氧化: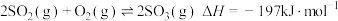
(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如图所示,下列说法不正确的是

b.α=0.88的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同α下的最大速率,选择最佳生产温度
(ⅱ)设
 的平衡分压为p,
的平衡分压为p, 的平衡转化率为b,用含p和b的代数式表示上述催化氧化反应的
的平衡转化率为b,用含p和b的代数式表示上述催化氧化反应的
(4)二氧化硫一空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。

(ⅱ)相同条件下,放电过程中消耗的
 和
和 的体积比为
的体积比为
您最近一年使用:0次
2024-05-14更新
|
42次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
4 . 非洛地平是一种降血压药。一种合成路线如下:
(1)物质Ⅱ的官能团是___________ (填名称),Ⅲ的分子式是___________ ,非洛地平有___________ 个手性碳原子。
(2)Ⅳ→Ⅴ的反应类型是___________ 。
(3)在催化剂、加热条件下,1molⅦ最多能与___________ mol 发生加成反应。
发生加成反应。
(4)写出Ⅵ→Ⅶ的化学方程式:___________ 。该反应实际分两步进行,第一步是加成反应,第二步是___________ 反应。
(5)在Ⅰ的芳香族同分异构体中,同时具备下列条件的结构有___________ 种。(已知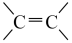 连有—OH的结构不稳定)
连有—OH的结构不稳定)
①含三种官能团;②苯环直接与 、
、 连接;③苯环上有3个取代基;④只有一个环。
连接;③苯环上有3个取代基;④只有一个环。
(6)以苯为原料制备苯甲醛,设计合成路线___________ (其他试剂自选)。
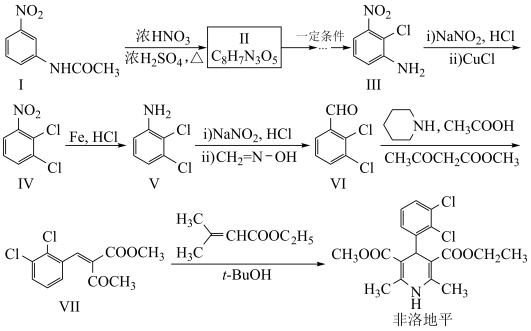
(1)物质Ⅱ的官能团是
(2)Ⅳ→Ⅴ的反应类型是
(3)在催化剂、加热条件下,1molⅦ最多能与
 发生加成反应。
发生加成反应。(4)写出Ⅵ→Ⅶ的化学方程式:
(5)在Ⅰ的芳香族同分异构体中,同时具备下列条件的结构有
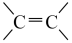 连有—OH的结构不稳定)
连有—OH的结构不稳定)①含三种官能团;②苯环直接与
 、
、 连接;③苯环上有3个取代基;④只有一个环。
连接;③苯环上有3个取代基;④只有一个环。(6)以苯为原料制备苯甲醛,设计合成路线
您最近一年使用:0次
2024-05-14更新
|
48次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
5 . 富马酸亚铁为棕红色固体,较难溶于水,是一种治疗缺铁性贫血的安全有效的补铁制剂。某实验小组用富马酸(HOOCCH=CHCOOH)和 制备富马酸亚铁,并对其纯度进行测定,过程如下:
制备富马酸亚铁,并对其纯度进行测定,过程如下:
Ⅰ.制备富马酸亚铁
①将少量富马酸固体置于烧杯中,加入50mL热水搅拌使之溶解;
②向烧杯中加入50mL一定浓度的 溶液,控制pH为6.5~6.7,并将其转移到仪器b中;
溶液,控制pH为6.5~6.7,并将其转移到仪器b中;
③通 并加热一段时间后,通过仪器a缓慢加入40mL新配置的
并加热一段时间后,通过仪器a缓慢加入40mL新配置的 溶液,继续加热约1小时后,出现大量棕红色沉淀。
溶液,继续加热约1小时后,出现大量棕红色沉淀。
④将反应混合液冷却后,减压过滤,洗涤,干燥,得粗产品。___________ ,仪器b适宜的规格是___________ 。
A.100mL B.250mL C.500mL
(2)已知反应容器中反应物 和富马酸按恰好完全反应的比例进行起始投料,步骤②中加入的
和富马酸按恰好完全反应的比例进行起始投料,步骤②中加入的 溶液要适量,若
溶液要适量,若 溶液加入过量,溶液pH偏高,则制得产品可能含有
溶液加入过量,溶液pH偏高,则制得产品可能含有___________ (填写化学式)。
(3)合成富马酸亚铁反应的化学方程式为___________ 。
(4)采用减压过滤的优点是___________ ,步骤④检验沉淀是否洗净的试剂是___________ 。
Ⅱ.产品纯度测定
取0.510g样品置于250mL锥形瓶中,加入15.00mL稀硫酸,加热使之溶解,冷却后再加入50.00mL新煮沸过的冷水和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色);立即用
呈无色);立即用 硫酸铈铵
硫酸铈铵 标准液滴定(还原产物为
标准液滴定(还原产物为 ),滴定至终点。平行测定三次,消耗标准液体积如下:
),滴定至终点。平行测定三次,消耗标准液体积如下:
(5)①硫酸铈铵 溶液应装入
溶液应装入___________ (填“酸式”或“碱式”)滴定管。
②滴定终点的现象为___________ ,该滴定过程的标准液不宜为酸性高锰酸钾溶液,原因是___________ 。
③产品的纯度是___________ %(保留4位有效数字)。
 制备富马酸亚铁,并对其纯度进行测定,过程如下:
制备富马酸亚铁,并对其纯度进行测定,过程如下:Ⅰ.制备富马酸亚铁
①将少量富马酸固体置于烧杯中,加入50mL热水搅拌使之溶解;
②向烧杯中加入50mL一定浓度的
 溶液,控制pH为6.5~6.7,并将其转移到仪器b中;
溶液,控制pH为6.5~6.7,并将其转移到仪器b中;③通
 并加热一段时间后,通过仪器a缓慢加入40mL新配置的
并加热一段时间后,通过仪器a缓慢加入40mL新配置的 溶液,继续加热约1小时后,出现大量棕红色沉淀。
溶液,继续加热约1小时后,出现大量棕红色沉淀。④将反应混合液冷却后,减压过滤,洗涤,干燥,得粗产品。

A.100mL B.250mL C.500mL
(2)已知反应容器中反应物
 和富马酸按恰好完全反应的比例进行起始投料,步骤②中加入的
和富马酸按恰好完全反应的比例进行起始投料,步骤②中加入的 溶液要适量,若
溶液要适量,若 溶液加入过量,溶液pH偏高,则制得产品可能含有
溶液加入过量,溶液pH偏高,则制得产品可能含有(3)合成富马酸亚铁反应的化学方程式为
(4)采用减压过滤的优点是
Ⅱ.产品纯度测定
取0.510g样品置于250mL锥形瓶中,加入15.00mL稀硫酸,加热使之溶解,冷却后再加入50.00mL新煮沸过的冷水和2滴邻二氮菲指示剂(邻二氮菲遇
 呈红色,遇
呈红色,遇 呈无色);立即用
呈无色);立即用 硫酸铈铵
硫酸铈铵 标准液滴定(还原产物为
标准液滴定(还原产物为 ),滴定至终点。平行测定三次,消耗标准液体积如下:
),滴定至终点。平行测定三次,消耗标准液体积如下:| 第一次 | 第二次 | 第三次 |
| 19.96mL | 20.20mL | 20.04mL |
 溶液应装入
溶液应装入②滴定终点的现象为
③产品的纯度是
您最近一年使用:0次
2024-05-14更新
|
45次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
6 . 298K时,向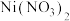 、
、 、
、 的混合液中滴加KCN溶液,混合液中lgx与
的混合液中滴加KCN溶液,混合液中lgx与 的关系如图所示,
的关系如图所示, 或
或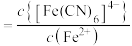 或
或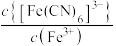 。下列叙述不正确的是
。下列叙述不正确的是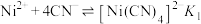 ;
;
(2) ;
;
(3)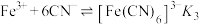 ,且
,且 。
。
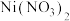 、
、 、
、 的混合液中滴加KCN溶液,混合液中lgx与
的混合液中滴加KCN溶液,混合液中lgx与 的关系如图所示,
的关系如图所示, 或
或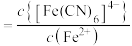 或
或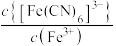 。下列叙述不正确的是
。下列叙述不正确的是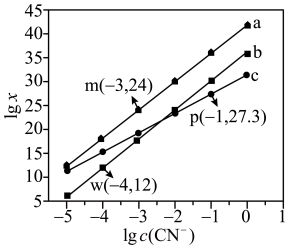
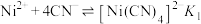 ;
;(2)
 ;
;(3)
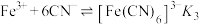 ,且
,且 。
。A.直线b代表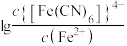 与 与 的关系 的关系 |
B.根据图像可计算平衡常数 数量级为 数量级为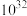 |
C. 的平衡常数 的平衡常数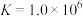 |
D.向含相同浓度的 和 和 的溶液中滴加 的溶液中滴加 溶液,先生成 溶液,先生成 |
您最近一年使用:0次
2024-05-14更新
|
62次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
解题方法
7 . 清华大学段吴泓副教授课题组首次利用糠醛创制了一种如图a所示的新型可充放电的“生物质电池”,该电池在充放电过程中可生产高附加值化学品糠醇和糠酸盐,其原理可用图b表示。下列说法正确的是




| A.该装置在生成糠酸盐时将电能转化为化学能 |
| B.膜a为阴离子交换膜 |
| C.充电时电极B附近碱性增强 |
| D.若使用铅蓄电池为其充电,当1mol糠醛转化时,Pb电极增重96g |
您最近一年使用:0次
2024-05-14更新
|
56次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
解题方法
8 . 一种催化还原NO的机理如图所示,下列说法正确的是
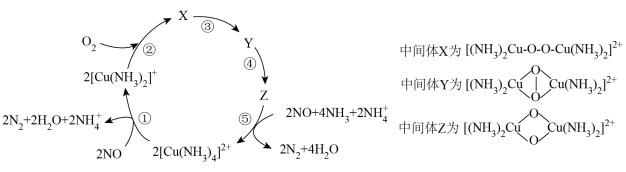

| A.中间体X和Z中O和Cu的化合价均不变 |
B.使用催化剂 ,可以提高NO的反应速率和平衡转化率 ,可以提高NO的反应速率和平衡转化率 |
| C.过程①中既有极性键的断裂,也有极性键的形成 |
D.该催化还原过程的总反应方程式为 |
您最近一年使用:0次
2024-05-14更新
|
49次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
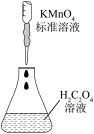
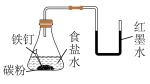
9 . 下列实验能达到实验目的的是
|
|
|
|
| A | B | C | D |
A.测定 溶液的浓度 溶液的浓度 | B.证明苯环使羟基活化 |
| C.吸收制盐酸 | D.验证铁的吸氧腐蚀 |
您最近一年使用:0次
2024-05-14更新
|
65次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
10 . N-甲基咪唑的结构简式为: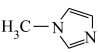 ,且4个碳原子和2个氮原子共平面,下列说法不正确的是
,且4个碳原子和2个氮原子共平面,下列说法不正确的是
| A.电负性:H<C<N<O |
B.咪唑分子中存在大π键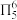 |
C.N-甲基咪唑分子中氮原子的杂化方式为 、 、 |
| D.N-甲基咪唑可以做配位体形成配位键 |
您最近一年使用:0次
2024-05-14更新
|
94次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学