解题方法
1 . 如图为某实验测得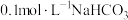 溶液在升温过程中(不考虑水挥发)的
溶液在升温过程中(不考虑水挥发)的 变化曲线,
变化曲线,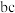 段有少量
段有少量 放出。下列说法正确的是
放出。下列说法正确的是
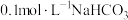 溶液在升温过程中(不考虑水挥发)的
溶液在升温过程中(不考虑水挥发)的 变化曲线,
变化曲线,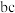 段有少量
段有少量 放出。下列说法正确的是
放出。下列说法正确的是
A. 点溶液的 点溶液的 等于 等于 点溶液的 点溶液的 |
B. 点时, 点时,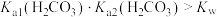 |
C. 点溶液中, 点溶液中,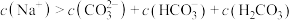 |
D. 段, 段, 减小说明升温抑制了 减小说明升温抑制了 的水解 的水解 |
您最近一年使用:0次
名校
解题方法
2 . 短周期主族元素a、b、c、d的原子序数依次增大,同周期主族元素中,b的原子半径最大。原子半径与原子序数、价层电子数关系如图所示。下列叙述正确的是

| A.a和d的简单氢化物的VSEPR模型完全相同 |
| B.工业上可通过电解熔融态的c的氧化物制备c单质 |
C. 和 和 所含化学键类型完全相同 所含化学键类型完全相同 |
| D.a的简单氢化物由液态转化为气态的过程中,断裂了极性键 |
您最近一年使用:0次
名校
解题方法
3 . 下列离子方程式正确的是
A.二元弱碱 与足量稀硫酸溶液反应: 与足量稀硫酸溶液反应: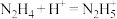 |
B. 溶于浓氨水: 溶于浓氨水: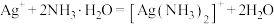 |
C. 溶液中加 溶液中加 溶液: 溶液: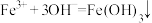 |
D. 溶液吸收 溶液吸收 : : |
您最近一年使用:0次
名校
4 . 木质纤维素代替传统的化石原料用于生产对二甲苯可以缓解日益紧张的能源危机,再利用对二甲苯为起始原料结合 生产聚碳酸对二甲苯酯可以实现碳减排,路线如下:
生产聚碳酸对二甲苯酯可以实现碳减排,路线如下:
(1)葡萄糖中含有的官能团有___________ (写名称)。
(2)化合物II中C原子的杂化方式为___________ 。VI生成VII的反应类型为___________ 。
(3)1mol化合物III与1mol乙烯反应得到1molIV,化合物IV的结构简式为___________ 。
(4)已知化合物V的核磁共振氢谱有2组峰,且峰面积之比为2:3,写出V生成VI的化学方程式___________ 。
(5)化合物III的同分异构体中符合下列条件的有___________ 种(不含立体异构)。 杂化的C上。
杂化的C上。
(6)参照上述信息,写出以CH2=CH-CH3和CO2为起始有机原料合成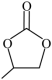 的路线(其它无机试剂任选)
的路线(其它无机试剂任选)___________ 。
 生产聚碳酸对二甲苯酯可以实现碳减排,路线如下:
生产聚碳酸对二甲苯酯可以实现碳减排,路线如下: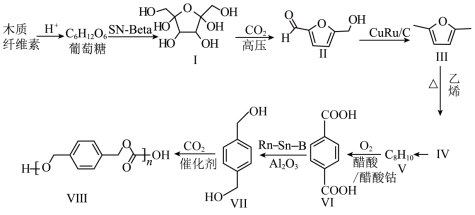
已知: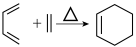 。
。
(1)葡萄糖中含有的官能团有
(2)化合物II中C原子的杂化方式为
(3)1mol化合物III与1mol乙烯反应得到1molIV,化合物IV的结构简式为
(4)已知化合物V的核磁共振氢谱有2组峰,且峰面积之比为2:3,写出V生成VI的化学方程式
(5)化合物III的同分异构体中符合下列条件的有
①含有环戊二烯(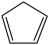 )的结构;
)的结构;
 杂化的C上。
杂化的C上。(6)参照上述信息,写出以CH2=CH-CH3和CO2为起始有机原料合成
 的路线(其它无机试剂任选)
的路线(其它无机试剂任选)
您最近一年使用:0次
名校
5 . 三草酸合铁( )酸钾晶体
)酸钾晶体 (
(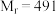 ),
), 时在水中溶解度为
时在水中溶解度为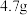 ,
, 时溶解度为
时溶解度为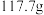 ,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室中先利用如图装置制备
,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室中先利用如图装置制备 (夹持装置略去),后续再制取三草酸合铁(
(夹持装置略去),后续再制取三草酸合铁( )酸钾晶体。
)酸钾晶体。
实验一: 晶体的制备
晶体的制备
(1)打开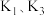 和
和 ,关闭
,关闭 ,向装置
,向装置 中加入稍过量的稀硫酸。
中加入稍过量的稀硫酸。
① 中盛放
中盛放 溶液的仪器名称为
溶液的仪器名称为___________ 。
②A中有气体产生,该气体的作用是___________ 。
(2)收集 并验纯后,打开
并验纯后,打开 ,关闭
,关闭___________ ,让A中浅绿色溶液流入 中,以生成
中,以生成 ,并分离得
,并分离得 晶体。
晶体。
实验二:三草酸合铁( )酸钾晶体的制备
)酸钾晶体的制备
(3)将实验一得到的 溶于水,加入
溶于水,加入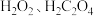 和
和 ,酒精灯微热并不断搅拌,反应制得
,酒精灯微热并不断搅拌,反应制得 ,冷却、过滤、洗涤、干燥。
,冷却、过滤、洗涤、干燥。
①写出该反应的化学方程式:___________ 。
②“微热、搅拌”过程中,温度不宜过高的原因是___________ 。
③过滤后需用___________ 洗涤,其优点是___________ 。
(4)产品纯度的测定
常温下,取 三草酸合铁(Ⅲ)酸钾晶体溶于水配制成
三草酸合铁(Ⅲ)酸钾晶体溶于水配制成 绿色溶液,取出25.00mL,用
绿色溶液,取出25.00mL,用 的酸性高锰酸钾标准液进行滴定,重复三次,平均消耗标准液20.00mL。
的酸性高锰酸钾标准液进行滴定,重复三次,平均消耗标准液20.00mL。
①滴定终点的判断依据是___________ 。
②该三草酸合铁( )酸钾晶体的纯度为
)酸钾晶体的纯度为___________ (保留三位有效数字)。
 )酸钾晶体
)酸钾晶体 (
( ),
), 时在水中溶解度为
时在水中溶解度为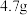 ,
, 时溶解度为
时溶解度为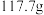 ,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室中先利用如图装置制备
,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室中先利用如图装置制备 (夹持装置略去),后续再制取三草酸合铁(
(夹持装置略去),后续再制取三草酸合铁( )酸钾晶体。
)酸钾晶体。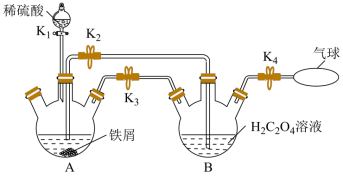
实验一:
 晶体的制备
晶体的制备(1)打开
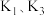 和
和 ,关闭
,关闭 ,向装置
,向装置 中加入稍过量的稀硫酸。
中加入稍过量的稀硫酸。①
 中盛放
中盛放 溶液的仪器名称为
溶液的仪器名称为②A中有气体产生,该气体的作用是
(2)收集
 并验纯后,打开
并验纯后,打开 ,关闭
,关闭 中,以生成
中,以生成 ,并分离得
,并分离得 晶体。
晶体。实验二:三草酸合铁(
 )酸钾晶体的制备
)酸钾晶体的制备(3)将实验一得到的
 溶于水,加入
溶于水,加入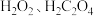 和
和 ,酒精灯微热并不断搅拌,反应制得
,酒精灯微热并不断搅拌,反应制得 ,冷却、过滤、洗涤、干燥。
,冷却、过滤、洗涤、干燥。①写出该反应的化学方程式:
②“微热、搅拌”过程中,温度不宜过高的原因是
③过滤后需用
(4)产品纯度的测定
常温下,取
 三草酸合铁(Ⅲ)酸钾晶体溶于水配制成
三草酸合铁(Ⅲ)酸钾晶体溶于水配制成 绿色溶液,取出25.00mL,用
绿色溶液,取出25.00mL,用 的酸性高锰酸钾标准液进行滴定,重复三次,平均消耗标准液20.00mL。
的酸性高锰酸钾标准液进行滴定,重复三次,平均消耗标准液20.00mL。①滴定终点的判断依据是
②该三草酸合铁(
 )酸钾晶体的纯度为
)酸钾晶体的纯度为
您最近一年使用:0次
名校
6 . 磷酸铁锂电池充电时锂离子由 电极迁移至石墨电极形成LiCx,
电极迁移至石墨电极形成LiCx, 的前体
的前体 可由
可由  、
、 、
、 在pH=2的条件下反应制得,已知锂的燃烧热为299kJ·mol-1,下列化学反应表示正确的是
在pH=2的条件下反应制得,已知锂的燃烧热为299kJ·mol-1,下列化学反应表示正确的是
 电极迁移至石墨电极形成LiCx,
电极迁移至石墨电极形成LiCx, 的前体
的前体 可由
可由  、
、 、
、 在pH=2的条件下反应制得,已知锂的燃烧热为299kJ·mol-1,下列化学反应表示正确的是
在pH=2的条件下反应制得,已知锂的燃烧热为299kJ·mol-1,下列化学反应表示正确的是A.锂燃烧的热化学方程式:2Li(s) +O2(g)=Li2O2(s)  H=+299kJ·mol-1 H=+299kJ·mol-1 |
| B.磷酸铁锂电池放电时的负极反应:LiCx +e-=Li++ Cx |
C. 的水解“释氨”过程: 的水解“释氨”过程: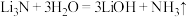 |
D.制备 的离子方程式: 的离子方程式: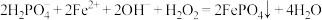 |
您最近一年使用:0次
7 . 室温下,下列实验方案能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 分离Fe粉和Cu粉 | 加入过量稀盐酸,过滤、洗涤、干燥 |
| B | 除去Cl2中混有的HCl | 将混合气体通入饱和碳酸氢钠溶液 |
| C | 探究 、 、 溶度积的大小 溶度积的大小 | 向2mL0.2mol/LMgCl2溶液中滴加4滴2mol/LNaOH溶液,充分振荡后,再滴加4滴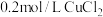 溶液,静置观察 溶液,静置观察 |
| D | 检验CH3CH2Cl中的氯原子 | 将CH3CH2Cl与过量NaOH水溶液混合加热,冷却后向溶液中加入AgNO3溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 明矾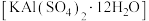 是一种常用的净水剂,以废易拉罐(主要成分为铝和少量不溶于碱性溶液的物质)为原料制取明矾的实验流程如图所示。
是一种常用的净水剂,以废易拉罐(主要成分为铝和少量不溶于碱性溶液的物质)为原料制取明矾的实验流程如图所示。
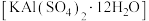 是一种常用的净水剂,以废易拉罐(主要成分为铝和少量不溶于碱性溶液的物质)为原料制取明矾的实验流程如图所示。
是一种常用的净水剂,以废易拉罐(主要成分为铝和少量不溶于碱性溶液的物质)为原料制取明矾的实验流程如图所示。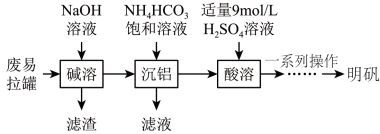
| A.“碱溶”步骤中有H2产生 |
| B.“沉铝”步骤所得滤液呈酸性 |
| C.用浓硫酸配制9mol/L H2SO4溶液,将浓硫酸缓慢加入到水中,并用玻璃棒搅拌 |
| D.“一系列操作”中还需要加入K2SO4 |
您最近一年使用:0次
9 . 工业上监测SO2含量是否达到排放标准的化学反应原理是:SO2+H2O2+BaCl2=BaSO4↓+2HCl,设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,11.2LSO2含有的原子总数为NA |
B.17gH2O2中含有 键数目为2NA 键数目为2NA |
| C.反应转移的电子数为0.2NA时,生成0.1mol的BaSO4沉淀 |
| D.常温下pH=1的HCl溶液中含有的H+数目为0.1NA |
您最近一年使用:0次
名校
10 . 甲氧基肉桂酸辛酯是一种化学防晒剂,其分子结构如图。下列说法错误的是

| A.分子式为C18H26O3 | B.分子中有2种含氧官能团 |
| C.能与氢氧化钠溶液发生反应 | D.分子中有2个手性碳原子 |
您最近一年使用:0次



