名校
解题方法
1 . 氮是生命体重要的组成元素,自然界中氮的循环对生命活动有重要意义。
(1)汽车尾气主要含有 、CO、
、CO、 、
、 等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、
等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、 ,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为
,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为______ 。
(2)“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。______ ;丙为钠盐,其化学式为______ 。
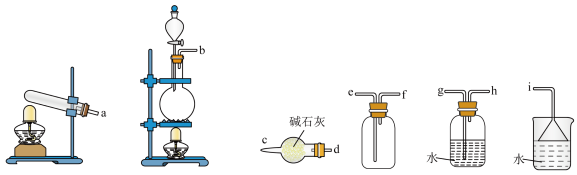
②甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为______ 。实验室用该反应原理制取并收集一瓶干燥的甲气体,从下图中选择合适的装置,其连接顺序为______ 。(按从左到右的气流方向,用小写字母 和箭头表示)______ (填字母)。
A. B.
B. C.
C. D.
D.
④丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与KI按物质的量1:1恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式______ 。
(1)汽车尾气主要含有
 、CO、
、CO、 、
、 等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、
等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、 ,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为
,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为(2)“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。

②甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为
A.
 B.
B. C.
C. D.
D.
④丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与KI按物质的量1:1恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式
您最近一年使用:0次
2 . 在下列有机物①CH3CH2CH3;②CH3-CH=CH2;③ ;④
;④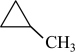 ;⑤
;⑤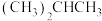 ;⑥
;⑥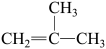 ;⑦
;⑦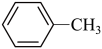 ;⑧
;⑧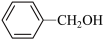 ;⑨
;⑨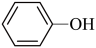 ,⑩CH3CH2Cl⑪O2⑫O3⑬
,⑩CH3CH2Cl⑪O2⑫O3⑬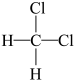 ⑭
⑭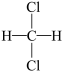 中,
中,
(2)写出有机物
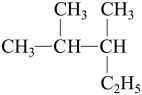 的系统命名
的系统命名(3)按系统命名法,
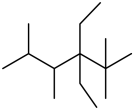 的名称是
的名称是(4)
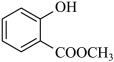 中含有的官能团的名称为
中含有的官能团的名称为(5)2,3—二甲基—4—乙基己烷
(6)支链上只有一个乙基,且式量最小的烷烃
您最近一年使用:0次
2024-05-12更新
|
849次组卷
|
3卷引用:广西钦州市第四中学2023-2024学年高二下学期期中考试化学试卷
名校
解题方法
3 . 任何化学反应都伴随着能量的变化,通过化学反应化学能可转化为热能、电能等不同形式的能量。
(1) 可用于工业合成氨气,已知常温常压下拆开
可用于工业合成氨气,已知常温常压下拆开 键、
键、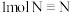 键分别需要吸收的能量为436kJ、946kJ,形成
键分别需要吸收的能量为436kJ、946kJ,形成 键会放出391kJ能量。
键会放出391kJ能量。
①根据上述数据判断工业合成氨的反应是___________ (填“吸热”或“放热”)反应。
②若消耗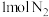 和
和 ,理论上放出或吸收热量为
,理论上放出或吸收热量为 ,则
,则 为
为___________ kJ。
(2)用图甲、乙所示装置进行实验,回答以下问题。
(3)某同学利用生活或实验室中常用的物品,设计了一个原电池,如图所示。 。
。
实验用品:电极(铁钉、铜钉)、稀硫酸、烧杯、导线、耳机(或电流表)。
①如果将装置中的耳机改为电流表,则铁钉应连接电流表的___________ 极,其电极反应式为___________ ;该电极上发生了___________ (填“氧化”或“还原”)反应。
②反应结束后,测得铁钉质量减轻了2.8克,则转移电子的物质的量为___________ 。
(1)
 可用于工业合成氨气,已知常温常压下拆开
可用于工业合成氨气,已知常温常压下拆开 键、
键、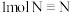 键分别需要吸收的能量为436kJ、946kJ,形成
键分别需要吸收的能量为436kJ、946kJ,形成 键会放出391kJ能量。
键会放出391kJ能量。①根据上述数据判断工业合成氨的反应是
②若消耗
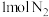 和
和 ,理论上放出或吸收热量为
,理论上放出或吸收热量为 ,则
,则 为
为(2)用图甲、乙所示装置进行实验,回答以下问题。
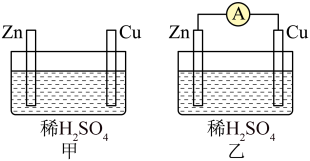
| A.甲中铜片是正极,乙中锌片是负极 |
| B.两烧杯中溶液的pH均增大 |
| C.两烧杯中铜片表面均有气泡产生 |
| D.若反应过程中有0.2mol电子转移,生成的氢气在标况下的体积均为2.24L |
(3)某同学利用生活或实验室中常用的物品,设计了一个原电池,如图所示。
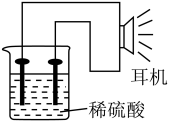
 。
。实验用品:电极(铁钉、铜钉)、稀硫酸、烧杯、导线、耳机(或电流表)。
①如果将装置中的耳机改为电流表,则铁钉应连接电流表的
②反应结束后,测得铁钉质量减轻了2.8克,则转移电子的物质的量为
您最近一年使用:0次
2024-05-04更新
|
227次组卷
|
2卷引用:广西南宁市新民中学2023-2024学年高一下学期3月考试化学试题
名校
4 . 电化学原理在电池制造、能量转换、物质合成等方面应用广泛。
(1)微型纽扣银锌电池(如下图)在生活中有广泛应用,其电极分别是 和
和 ,电解质为
,电解质为 溶液,电极反应分别为:
溶液,电极反应分别为: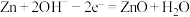 ;
;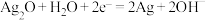 。
。 是电池的
是电池的___________ 极,电池的总反应方程式为___________ 。在使用过程中,电解质溶液的
___________ (填“增大”、“减小”或“不变”)。
(2)燃料电池必须从电池外部不断地向电池提供燃料。如甲烷 -空气燃料电池,工作原理如下图甲。ab均为惰性电极。a为
-空气燃料电池,工作原理如下图甲。ab均为惰性电极。a为___________ 极,正极的电极反应式为___________ 。当通入 (标准状况下)甲烷气体完全反应时,测得电路中转移
(标准状况下)甲烷气体完全反应时,测得电路中转移 电子,则甲烷的利用率为
电子,则甲烷的利用率为___________ 。
写出该装置负极的电极反应式___________ ,若此过程中转移了 电子,则理论上质子膜两侧电解液的质量变化差[
电子,则理论上质子膜两侧电解液的质量变化差[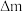 左
左 右]为
右]为___________ 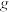 (忽略气体的溶解)。
(忽略气体的溶解)。
(1)微型纽扣银锌电池(如下图)在生活中有广泛应用,其电极分别是
 和
和 ,电解质为
,电解质为 溶液,电极反应分别为:
溶液,电极反应分别为: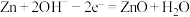 ;
;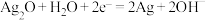 。
。
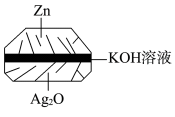
 是电池的
是电池的
(2)燃料电池必须从电池外部不断地向电池提供燃料。如甲烷
 -空气燃料电池,工作原理如下图甲。ab均为惰性电极。a为
-空气燃料电池,工作原理如下图甲。ab均为惰性电极。a为 (标准状况下)甲烷气体完全反应时,测得电路中转移
(标准状况下)甲烷气体完全反应时,测得电路中转移 电子,则甲烷的利用率为
电子,则甲烷的利用率为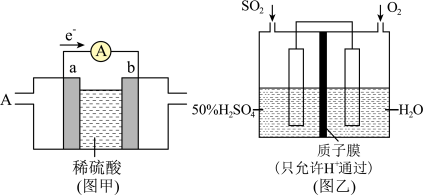
写出该装置负极的电极反应式
 电子,则理论上质子膜两侧电解液的质量变化差[
电子,则理论上质子膜两侧电解液的质量变化差[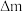 左
左 右]为
右]为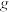 (忽略气体的溶解)。
(忽略气体的溶解)。
您最近一年使用:0次
名校
5 . Ⅰ.请写出下列反应的离子方程式:
(1)往 溶液中滴加浓烧碱并加热:
溶液中滴加浓烧碱并加热:___________ 。
(2)往 溶液中滴加稀盐酸溶液:
溶液中滴加稀盐酸溶液:___________ 。
(3)将 气体与
气体与 充分发生反应:
充分发生反应:___________ 。
(4) 溶液中通入少量
溶液中通入少量 气体:
气体:___________ 。
(5)往 溶液中通入少量
溶液中通入少量 :
:___________ 。
Ⅱ.请按要求完成下列热化学知识小题(能量数据均为常温常压下的测定值):
(6)将 氢气与足量氧气充分反应生成液态水,放出
氢气与足量氧气充分反应生成液态水,放出 的热量。则表示氢气燃烧热的热化学方程式为:
的热量。则表示氢气燃烧热的热化学方程式为:___________ 。
(7)将含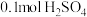 的稀硫酸溶液与足量稀
的稀硫酸溶液与足量稀 溶液迅速反应,测得放出
溶液迅速反应,测得放出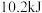 的热量。则表示该反应的热化学方程式为:
的热量。则表示该反应的热化学方程式为:___________ 。
(8)已知反应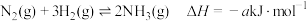 ;
; 、
、 键能分别为
键能分别为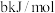 、
、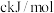 ,则
,则 的键能为
的键能为___________  (用含a、b、c的式子表示)。
(用含a、b、c的式子表示)。
(9)已知:
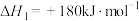

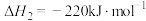
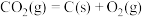
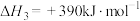
则反应 的
的
___________  。
。
(1)往
 溶液中滴加浓烧碱并加热:
溶液中滴加浓烧碱并加热:(2)往
 溶液中滴加稀盐酸溶液:
溶液中滴加稀盐酸溶液:(3)将
 气体与
气体与 充分发生反应:
充分发生反应:(4)
 溶液中通入少量
溶液中通入少量 气体:
气体:(5)往
 溶液中通入少量
溶液中通入少量 :
:Ⅱ.请按要求完成下列热化学知识小题(能量数据均为常温常压下的测定值):
(6)将
 氢气与足量氧气充分反应生成液态水,放出
氢气与足量氧气充分反应生成液态水,放出 的热量。则表示氢气燃烧热的热化学方程式为:
的热量。则表示氢气燃烧热的热化学方程式为:(7)将含
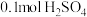 的稀硫酸溶液与足量稀
的稀硫酸溶液与足量稀 溶液迅速反应,测得放出
溶液迅速反应,测得放出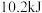 的热量。则表示该反应的热化学方程式为:
的热量。则表示该反应的热化学方程式为:(8)已知反应
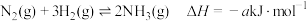 ;
; 、
、 键能分别为
键能分别为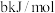 、
、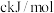 ,则
,则 的键能为
的键能为 (用含a、b、c的式子表示)。
(用含a、b、c的式子表示)。(9)已知:

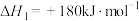

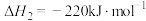
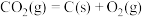
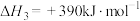
则反应
 的
的
 。
。
您最近一年使用:0次
名校
6 . 卤素单质及其化合物在工农业生产中有着广泛的应用。回答下列问题:
(1)类卤素 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):
①硫氰酸和异硫氰酸分子中 键和
键和 键个数之比
键个数之比___________ (填“相等”或“不相等”)。
②异硫氰酸中N的杂化轨道类型是___________ 。
③硫氰酸的电子式为___________ 。
(2) 的VSEPR模型是
的VSEPR模型是___________ , 的中心原子的价层电子对数是
的中心原子的价层电子对数是___________ 。
(3)键角:
___________ (填“>”“<”或“=”) ,判断的理由为
,判断的理由为___________ 。
(4)酸性:三氟乙酸( )
)___________ (填“>”或“<”) ,判断的理由为
,判断的理由为___________ 。
(5) 与水反应的化学方程式为
与水反应的化学方程式为___________ (该反应为非氧化还原反应)。
(1)类卤素
 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):①硫氰酸和异硫氰酸分子中
 键和
键和 键个数之比
键个数之比②异硫氰酸中N的杂化轨道类型是
③硫氰酸的电子式为
(2)
 的VSEPR模型是
的VSEPR模型是 的中心原子的价层电子对数是
的中心原子的价层电子对数是(3)键角:

 ,判断的理由为
,判断的理由为(4)酸性:三氟乙酸(
 )
) ,判断的理由为
,判断的理由为(5)
 与水反应的化学方程式为
与水反应的化学方程式为
您最近一年使用:0次
2024-04-26更新
|
217次组卷
|
2卷引用:广西壮族自治区桂林市联考2023-2024学年高二下学期3月月考化学试题
名校
解题方法
7 . 请完成下列问题:
现代社会中,人类的一切活动都离不开能量,化学反应中不仅有新物质的生成,而且伴随着能量的变化,同时,化学电池也成为人类生产和生活的重要能量来源之一;
(1)下列反应属于放热反应的是___________ (填序号)。
①碳酸钙高温分解 ②生石灰和水的反应 ③ 在
在 中燃烧
中燃烧
(2)如图是原电池的装置图。请回答下列问题:___________ (填“正极”或“负极”),发生___________ 反应(填“氧化”或“还原”);电子由___________ 片通过导线流向___________ 片。(均填化学式)
②溶液中的 向
向___________ 片移动。(填化学式)
③Cu片上发生反应的电极反应式为___________ 。
④若Fe电极消耗5.6g,则外电路转移___________  。
。
现代社会中,人类的一切活动都离不开能量,化学反应中不仅有新物质的生成,而且伴随着能量的变化,同时,化学电池也成为人类生产和生活的重要能量来源之一;
(1)下列反应属于放热反应的是
①碳酸钙高温分解 ②生石灰和水的反应 ③
 在
在 中燃烧
中燃烧(2)如图是原电池的装置图。请回答下列问题:
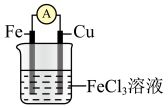
②溶液中的
 向
向③Cu片上发生反应的电极反应式为
④若Fe电极消耗5.6g,则外电路转移
 。
。
您最近一年使用:0次
8 . 硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括___________ 、___________ 和玻璃。
(2)光导纤维的主要成分是 。
。 为
为___________ (“酸性”、“碱性”或“两性”)氧化物,写出 与烧碱反应的化学方程式
与烧碱反应的化学方程式___________ 。
(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是______(填字母)。
(4)硅单质可作硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:___________ 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成 、
、 和一种气体单质,写出发生反应的化学方程式
和一种气体单质,写出发生反应的化学方程式___________ ;在制备高纯硅的过程中若混入 ,可能引起的后果是
,可能引起的后果是___________ 。
(1)传统的无机非金属材料多为硅酸盐材料,主要包括
(2)光导纤维的主要成分是
 。
。 为
为 与烧碱反应的化学方程式
与烧碱反应的化学方程式(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是______(填字母)。
A. 能与水反应 能与水反应 | B. 在一定条件下能与氧化钙反应 在一定条件下能与氧化钙反应 |
C. 是制作光导纤维的主要原料 是制作光导纤维的主要原料 | D. 能与稀硫酸反应 能与稀硫酸反应 |
(4)硅单质可作硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:

②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成
 、
、 和一种气体单质,写出发生反应的化学方程式
和一种气体单质,写出发生反应的化学方程式 ,可能引起的后果是
,可能引起的后果是
您最近一年使用:0次
名校
解题方法
9 . 硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。河南焦作的山药富含硒( ),有抗癌、抗衰老等重要功能。请回答下列问题。
),有抗癌、抗衰老等重要功能。请回答下列问题。
(1) 的原子结构示意图为
的原子结构示意图为______________ ,其在周期表中的位置为______________ 。
(2)氧、硫、硒位于同一主族,其性质具有一定的递变性。
①下列说法正确的是______________ (填标号)。
A.还原性: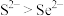
B.浓硒酸可能具有强氧化性、吸水性
C.稳定性:
D.氧化性: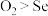
② 通入
通入 的水溶液中会生成不溶于水的
的水溶液中会生成不溶于水的 ,该反应的化学方程式为
,该反应的化学方程式为______________ ; 能与浓硫酸反应生成
能与浓硫酸反应生成 和
和 ,则浓硫酸、
,则浓硫酸、 和
和 三者中,氧化性最弱的为
三者中,氧化性最弱的为______________ 。
(3)某混合物中硒主要以 和
和 的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
ⅰ.将该混合物与浓硫酸混合焙烧,产生 、
、 的烟气
的烟气
ⅱ.用水吸收ⅰ中烟气,可得 固体
固体
已知: 的熔点为315℃,沸点为684.9℃。
的熔点为315℃,沸点为684.9℃。
①可用足量 溶液吸收烟气中的
溶液吸收烟气中的 ,二者反应生成一种盐,该盐的化学式为
,二者反应生成一种盐,该盐的化学式为__________ 。
② 中
中 的化合价为
的化合价为_________ 价;焙烧时, 与浓
与浓 反应的化学方程式为
反应的化学方程式为_________________ ,理论上该反应每转移1 电子,得到的
电子,得到的 的质量为
的质量为_________ g。
 ),有抗癌、抗衰老等重要功能。请回答下列问题。
),有抗癌、抗衰老等重要功能。请回答下列问题。(1)
 的原子结构示意图为
的原子结构示意图为(2)氧、硫、硒位于同一主族,其性质具有一定的递变性。
①下列说法正确的是
A.还原性:
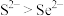
B.浓硒酸可能具有强氧化性、吸水性
C.稳定性:

D.氧化性:
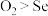
②
 通入
通入 的水溶液中会生成不溶于水的
的水溶液中会生成不溶于水的 ,该反应的化学方程式为
,该反应的化学方程式为 能与浓硫酸反应生成
能与浓硫酸反应生成 和
和 ,则浓硫酸、
,则浓硫酸、 和
和 三者中,氧化性最弱的为
三者中,氧化性最弱的为(3)某混合物中硒主要以
 和
和 的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:ⅰ.将该混合物与浓硫酸混合焙烧,产生
 、
、 的烟气
的烟气ⅱ.用水吸收ⅰ中烟气,可得
 固体
固体已知:
 的熔点为315℃,沸点为684.9℃。
的熔点为315℃,沸点为684.9℃。①可用足量
 溶液吸收烟气中的
溶液吸收烟气中的 ,二者反应生成一种盐,该盐的化学式为
,二者反应生成一种盐,该盐的化学式为②
 中
中 的化合价为
的化合价为 与浓
与浓 反应的化学方程式为
反应的化学方程式为 电子,得到的
电子,得到的 的质量为
的质量为
您最近一年使用:0次
2024-04-21更新
|
240次组卷
|
3卷引用:广西壮族自治区百所名校2023-2024学年高一下学期3月联合考试化学试题
名校
10 . 在一定条件下,某些物质具有如图所示的转化关系。丙为白色固体,其悬浊液在空气中会迅速变为灰绿色,最终变为红褐色。请回答下列问题:
(1)根据分析可知丙为________________ (填化学式);甲可能是__________ (填标号,下同),乙可能是__________ 。
A.稀硝酸 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液
(2)实验室保存 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量___________ (填药品名称);可以用______________ (填化学式)溶液来检验 溶液中的
溶液中的 是否被氧化。
是否被氧化。
(3)丙的悬浊液在空气中变色的原因为____________________ (填化学方程式);工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是____________________ (填化学方程式)。
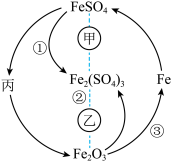
(1)根据分析可知丙为
A.稀硝酸 B.
 溶液 C.
溶液 C. D.
D. 溶液
溶液(2)实验室保存
 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量 溶液中的
溶液中的 是否被氧化。
是否被氧化。(3)丙的悬浊液在空气中变色的原因为
您最近一年使用:0次
2024-04-21更新
|
168次组卷
|
2卷引用:广西壮族自治区百所名校2023-2024学年高一下学期3月联合考试化学试题



