Ⅰ.请写出下列反应的离子方程式:
(1)往 溶液中滴加浓烧碱并加热:
溶液中滴加浓烧碱并加热:___________ 。
(2)往 溶液中滴加稀盐酸溶液:
溶液中滴加稀盐酸溶液:___________ 。
(3)将 气体与
气体与 充分发生反应:
充分发生反应:___________ 。
(4) 溶液中通入少量
溶液中通入少量 气体:
气体:___________ 。
(5)往 溶液中通入少量
溶液中通入少量 :
:___________ 。
Ⅱ.请按要求完成下列热化学知识小题(能量数据均为常温常压下的测定值):
(6)将 氢气与足量氧气充分反应生成液态水,放出
氢气与足量氧气充分反应生成液态水,放出 的热量。则表示氢气燃烧热的热化学方程式为:
的热量。则表示氢气燃烧热的热化学方程式为:___________ 。
(7)将含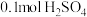 的稀硫酸溶液与足量稀
的稀硫酸溶液与足量稀 溶液迅速反应,测得放出
溶液迅速反应,测得放出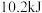 的热量。则表示该反应的热化学方程式为:
的热量。则表示该反应的热化学方程式为:___________ 。
(8)已知反应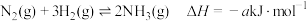 ;
; 、
、 键能分别为
键能分别为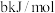 、
、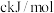 ,则
,则 的键能为
的键能为___________  (用含a、b、c的式子表示)。
(用含a、b、c的式子表示)。
(9)已知:
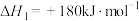

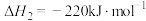
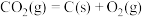
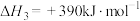
则反应 的
的
___________  。
。
(1)往
 溶液中滴加浓烧碱并加热:
溶液中滴加浓烧碱并加热:(2)往
 溶液中滴加稀盐酸溶液:
溶液中滴加稀盐酸溶液:(3)将
 气体与
气体与 充分发生反应:
充分发生反应:(4)
 溶液中通入少量
溶液中通入少量 气体:
气体:(5)往
 溶液中通入少量
溶液中通入少量 :
:Ⅱ.请按要求完成下列热化学知识小题(能量数据均为常温常压下的测定值):
(6)将
 氢气与足量氧气充分反应生成液态水,放出
氢气与足量氧气充分反应生成液态水,放出 的热量。则表示氢气燃烧热的热化学方程式为:
的热量。则表示氢气燃烧热的热化学方程式为:(7)将含
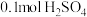 的稀硫酸溶液与足量稀
的稀硫酸溶液与足量稀 溶液迅速反应,测得放出
溶液迅速反应,测得放出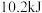 的热量。则表示该反应的热化学方程式为:
的热量。则表示该反应的热化学方程式为:(8)已知反应
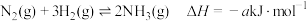 ;
; 、
、 键能分别为
键能分别为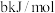 、
、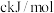 ,则
,则 的键能为
的键能为 (用含a、b、c的式子表示)。
(用含a、b、c的式子表示)。(9)已知:

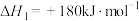

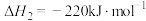
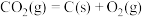
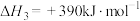
则反应
 的
的
 。
。
更新时间:2024-04-29 22:15:13
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
(1)下列物质中:①SO2 ②液态氯化氢 ③CH4 ④熔融NaOH ⑤NH4Cl固体 ⑥氨水。能导电的是__________ (填序号,下同)。属于电解质的是__________ 。属于非电解质的是__________ 。
(2)1.204×1024个H2SO4分子的物质的量为__________ mol,共含__________ 个氢原子。将上述H2SO4溶于水配成600 mL溶液,再加水稀释到1000 mL,稀释后溶液的物质的量浓度为__________ mol/L。
(3)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L, 浓度为0.9mol/L,则K+的物质的量浓度为
浓度为0.9mol/L,则K+的物质的量浓度为__________ mol/L。
(4)Al2O3与稀盐酸反应的离子方程式为__________ 。向Ba(OH)2溶液中逐滴加入NaHSO4溶液至不再产生沉淀,离子方程式为__________ 。
(1)下列物质中:①SO2 ②液态氯化氢 ③CH4 ④熔融NaOH ⑤NH4Cl固体 ⑥氨水。能导电的是
(2)1.204×1024个H2SO4分子的物质的量为
(3)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,
 浓度为0.9mol/L,则K+的物质的量浓度为
浓度为0.9mol/L,则K+的物质的量浓度为(4)Al2O3与稀盐酸反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
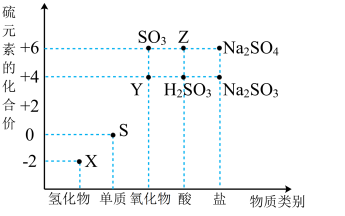
(1)仅从硫元素化合价 变化的角度分析,图中既有氧化性又有还原性的化合物 有___________ (填化学式)。
(2)X与Z在一定条件下可以发生反应: (浓)
(浓)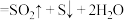 。用双线桥法标出上述反应转移的电子数目和方向
。用双线桥法标出上述反应转移的电子数目和方向___________ 。
(3)请预测X与Y能否共存___________ (填能或不能),若不能请写出化学方程式若能请说明理由___________ 。
(4)写出一个上述含硫物质间相互转化的非氧化还原反应的离子方程式___________ 。
(5) 是重要的化工原料。从氧化还原反应的角度分析,下列制备
是重要的化工原料。从氧化还原反应的角度分析,下列制备 的方案理论上可行的是___________(填字母)。
的方案理论上可行的是___________(填字母)。

(1)仅从
(2)X与Z在一定条件下可以发生反应:
 (浓)
(浓)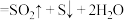 。用双线桥法标出上述反应转移的电子数目和方向
。用双线桥法标出上述反应转移的电子数目和方向(3)请预测X与Y能否共存
(4)写出一个上述含硫物质间相互转化的非氧化还原反应的离子方程式
(5)
 是重要的化工原料。从氧化还原反应的角度分析,下列制备
是重要的化工原料。从氧化还原反应的角度分析,下列制备 的方案理论上可行的是___________(填字母)。
的方案理论上可行的是___________(填字母)。A. | B. | C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.写出下列反应的离子方程式:
(1)CuSO4溶液与Ba(OH)2溶液混合:___________ 。
(2)鸡蛋壳(主要成份为碳酸钙)溶解在盐酸中:___________ 。
(3)铝片溶解在氢氧化钠溶液中:___________ 。
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其中可能含有 、Na+、
、Na+、 、H+、
、H+、 、
、 、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL该溶液加入稀硝酸酸化的BaCl2溶液,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(4)原溶液中一定存在的离子是___________ ,一定不存在的离子是___________ 。
(5)按上述实验操不能确定原溶液中有Cl-,请说明原因:___________ 。
(1)CuSO4溶液与Ba(OH)2溶液混合:
(2)鸡蛋壳(主要成份为碳酸钙)溶解在盐酸中:
(3)铝片溶解在氢氧化钠溶液中:
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其中可能含有
 、Na+、
、Na+、 、H+、
、H+、 、
、 、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL该溶液加入稀硝酸酸化的BaCl2溶液,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(4)原溶液中一定存在的离子是
(5)按上述实验操不能确定原溶液中有Cl-,请说明原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如图是CO和H2反应生成CH3OH的能量变化图:
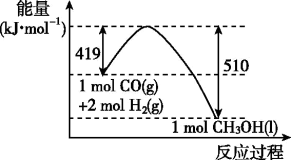
(1)写出该反应的化学方程式:_______
(2)从图中可知,1molCO和2molH2化学键的断裂共_______ (“放出”或“吸收”,下同)419kJ的热量,形成1molCH3OH_______ 510kJ热量。
(3)该反应是_______ (“放热”或“吸热”)反应。比较1molCH3OH(液体)和1molCH3OH(气体)的稳定性,稳定性好的是_______ (“前者”或“后者”)
(4)下列措施能加快该反应速率的是_______

(1)写出该反应的化学方程式:
(2)从图中可知,1molCO和2molH2化学键的断裂共
(3)该反应是
(4)下列措施能加快该反应速率的是_______
| A.降低温度 | B.缩小体积 | C.体积不变加入Ar | D.使用催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学变化过程中均存在物质变化与能量变化。
(1)某化学兴趣小组进行如图所示实验装置,以验证此结论。
①进行实验时,装置a中溶液变色,装置b中能闻到___________ ;装置a中温度计中水银液面变化是___________ (填“升高”或“降低”,下同);装置b中温度计中水银液面变化是___________ 。
②下列化学反应中的能量变化关系与图c相符合的是___________ 。
A.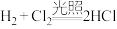
B.天然气的燃烧
C.
D.
(2)汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示,若反应生成2 mol NO气体(选“吸收”或“放出”)___________ kJ热量,该反应的反应物的总能量___________ (填“大于”、“等于”或“小于”)生成物的总能量。___________ (填“氧化”或“还原”)反应。
②乙池中铝片为___________ 极,写出铝电极的电极反应式:___________ 。
(1)某化学兴趣小组进行如图所示实验装置,以验证此结论。
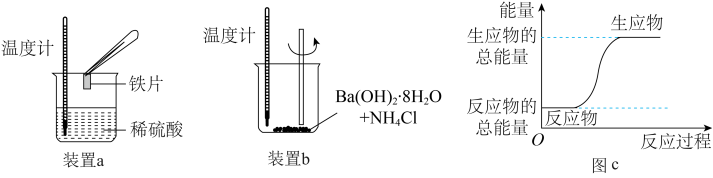
①进行实验时,装置a中溶液变色,装置b中能闻到
②下列化学反应中的能量变化关系与图c相符合的是
A.
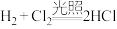
B.天然气的燃烧
C.

D.

(2)汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示,若反应生成2 mol NO气体(选“吸收”或“放出”)

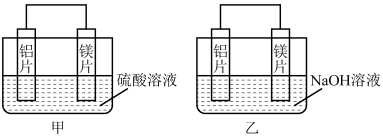
②乙池中铝片为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】 和
和 是汽车尾气的主要成分,它们能缓慢地发生反应Ⅰ:
是汽车尾气的主要成分,它们能缓慢地发生反应Ⅰ: 。
。
(1)汽车行驶时, 和
和 在电火花作用下产生
在电火花作用下产生 ,各物质所含化学键键能数据如下表:
,各物质所含化学键键能数据如下表:
相同条件下, 、
、 、
、 三种物质中最稳定的是
三种物质中最稳定的是_______ ;
_______ 。
(2)工业上可通过 和
和 化合制备甲醇,反应的化学方程式为
化合制备甲醇,反应的化学方程式为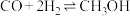 。
。
已知:①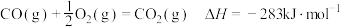
②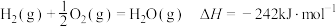
③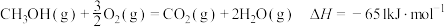
写出工业上用 和
和 合成
合成 的热化学方程式:
的热化学方程式:_______ 。
(3)反应I在常温下可以自发进行,则该反应的正反应为_______ (填“吸热”或“放热”)反应。
(4)为减少汽车尾气污染,下列措施合理的有_______(填字母)。
 和
和 是汽车尾气的主要成分,它们能缓慢地发生反应Ⅰ:
是汽车尾气的主要成分,它们能缓慢地发生反应Ⅰ: 。
。(1)汽车行驶时,
 和
和 在电火花作用下产生
在电火花作用下产生 ,各物质所含化学键键能数据如下表:
,各物质所含化学键键能数据如下表:| 物质 |  |  |  |
化学键键能 | 946 | 498 | 632 |
 、
、 、
、 三种物质中最稳定的是
三种物质中最稳定的是
(2)工业上可通过
 和
和 化合制备甲醇,反应的化学方程式为
化合制备甲醇,反应的化学方程式为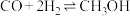 。
。已知:①
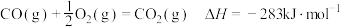
②
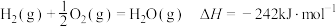
③
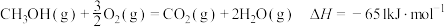
写出工业上用
 和
和 合成
合成 的热化学方程式:
的热化学方程式:(3)反应I在常温下可以自发进行,则该反应的正反应为
(4)为减少汽车尾气污染,下列措施合理的有_______(填字母)。
| A.开发氢能源 | B.寻找反应I的高效催化剂 |
| C.市民大量移居城市郊区 | D.戴上呼吸面具 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应I:
反应Ⅱ: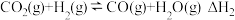
反应Ⅲ: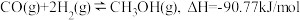
回答下列问题:
(1)反应Ⅱ的△H=____________ 。
(2)反应Ⅲ自发进行条件是________ (填“较低温度”、“较高温度”或“任何温度”)。
(3)在一体积为1L的密闭容器中,通入一定量的CO和H2O,在 发生如下反应:
发生如下反应: ,CO和H2O浓度变化如图:
,CO和H2O浓度变化如图:

①0~4min的平均反应速率v(CO)=______ mol/(L·min)。
②850℃时,若向该容器中充入1.0molCO、3.0molH2O,则CO的平衡转化率为_______ 。
(4)在某温度下,1L恒容密闭容器中充入2a(a>0)molH2和amolCO,在一定条件下合成甲醇, ,达到平衡时各物质的量总和为1.8amol。
,达到平衡时各物质的量总和为1.8amol。
①在该温度下,平衡常数K=__________ (用含a的代数式表示)。
②下列情况表明反应达到平衡状态的是____________ 。
A.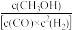 不再改变 B. CO的消耗速率等于
不再改变 B. CO的消耗速率等于 的生成速率
的生成速率
C.混合气体的平均摩尔质量不再改变 D.混合气体的密度不再改变
(5)由CO2制备甲醇还需要氢气。工业上用电解法制取 ,同时获得氢气:
,同时获得氢气: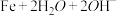
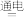
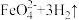 ,工作原理如图所示。电解一段时间后,
,工作原理如图所示。电解一段时间后, 降低的区域在
降低的区域在______ (填“阴极室”或“阳极室”);该室发生的电极反应式为:__________________ 。

反应I:

反应Ⅱ:
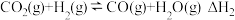
反应Ⅲ:
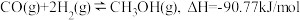
回答下列问题:
(1)反应Ⅱ的△H=
(2)反应Ⅲ自发进行条件是
(3)在一体积为1L的密闭容器中,通入一定量的CO和H2O,在
 发生如下反应:
发生如下反应: ,CO和H2O浓度变化如图:
,CO和H2O浓度变化如图:
①0~4min的平均反应速率v(CO)=
②850℃时,若向该容器中充入1.0molCO、3.0molH2O,则CO的平衡转化率为
(4)在某温度下,1L恒容密闭容器中充入2a(a>0)molH2和amolCO,在一定条件下合成甲醇,
 ,达到平衡时各物质的量总和为1.8amol。
,达到平衡时各物质的量总和为1.8amol。①在该温度下,平衡常数K=
②下列情况表明反应达到平衡状态的是
A.
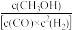 不再改变 B. CO的消耗速率等于
不再改变 B. CO的消耗速率等于 的生成速率
的生成速率C.混合气体的平均摩尔质量不再改变 D.混合气体的密度不再改变
(5)由CO2制备甲醇还需要氢气。工业上用电解法制取
 ,同时获得氢气:
,同时获得氢气: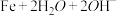
 ,工作原理如图所示。电解一段时间后,
,工作原理如图所示。电解一段时间后, 降低的区域在
降低的区域在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)已知拆开1mol H—H键、1mol N—H键、1molN≡N键需要的能量分别是436 kJ、391 kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___ 。
(2)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,回答下列问题:
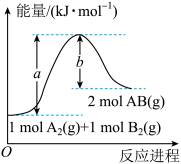
①该反应的ΔH___ 0(填“大于”“小于”或“等于”);
②反应物的总键能为__ ;
③写出该反应的热化学方程式____ 。
(3)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
①2O2(g)+N2(g)=N2O4(l) ΔH1 ②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=___ ,联氨和N2O4可作为火箭推进剂的主要原因为____ 。
(2)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,回答下列问题:

①该反应的ΔH
②反应物的总键能为
③写出该反应的热化学方程式
(3)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
①2O2(g)+N2(g)=N2O4(l) ΔH1 ②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】近年来,全国部分地区被雾霾笼罩,机动车尾气排放成为引发雾霾的罪魁祸首。提高空气质量,减少机动车尾气排放成为当务之急。汽车内燃机工作时引起反应:N2(g)+O2(g)  2NO(g),是导致汽车尾气中含有NO的原因之一。已知断裂某些共价键需要的能量如表:
2NO(g),是导致汽车尾气中含有NO的原因之一。已知断裂某些共价键需要的能量如表:
(1)机动车发动机工作时会引发N2和O2的反应,该反应是____ (填“放热”或“吸热”)反应,1 molO2与1 molN2的总能量比2 molNO的总能量___ (填“大”或“小”)。
(2)N2与O2合成NO的热化学方程式可以表示为 N2(g)+
N2(g)+ O2(g)=NO(g)ΔH,则ΔH=
O2(g)=NO(g)ΔH,则ΔH=_____ 。
(3)NO与CO反应的热化学方程式可以表示为2NO(g)+2CO(g)=2CO2(g)+N2(g) ΔH=a kJ·mol-1,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后,a___ (填“增大”“减小”或“不变”)。
(4)已知:①Fe(s)+ O2(g)=FeO(s) ΔH1=-275.0 kJ·mol-1;
O2(g)=FeO(s) ΔH1=-275.0 kJ·mol-1;
②2Al(s)+ O2(g)=Al2O3(s) ΔH2=-1 675.0 kJ·mol-1。
O2(g)=Al2O3(s) ΔH2=-1 675.0 kJ·mol-1。
Al和FeO发生铝热反应的热化学方程式是_______ 。
 2NO(g),是导致汽车尾气中含有NO的原因之一。已知断裂某些共价键需要的能量如表:
2NO(g),是导致汽车尾气中含有NO的原因之一。已知断裂某些共价键需要的能量如表:| 断裂的共价键 | O =O | N≡N | N—O |
| 需要的能量 | 495 kJ·mol-1 | 945 kJ·mol-1 | 630 kJ·mol-1 |
(1)机动车发动机工作时会引发N2和O2的反应,该反应是
(2)N2与O2合成NO的热化学方程式可以表示为
 N2(g)+
N2(g)+ O2(g)=NO(g)ΔH,则ΔH=
O2(g)=NO(g)ΔH,则ΔH=(3)NO与CO反应的热化学方程式可以表示为2NO(g)+2CO(g)=2CO2(g)+N2(g) ΔH=a kJ·mol-1,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后,a
(4)已知:①Fe(s)+
 O2(g)=FeO(s) ΔH1=-275.0 kJ·mol-1;
O2(g)=FeO(s) ΔH1=-275.0 kJ·mol-1;②2Al(s)+
 O2(g)=Al2O3(s) ΔH2=-1 675.0 kJ·mol-1。
O2(g)=Al2O3(s) ΔH2=-1 675.0 kJ·mol-1。Al和FeO发生铝热反应的热化学方程式是
您最近一年使用:0次
【推荐2】填空。
I.
(1)下列反应中,属于吸热反应的是___________ (填序号),属于放热反应的是___________ (填序号)。
①物质燃烧②炸药爆炸③浓硫酸稀释④二氧化碳通过炽热的碳⑤硝酸铵溶于水吸热⑥ 与
与 反应⑦铁粉与稀盐酸反应
反应⑦铁粉与稀盐酸反应
(2)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为 。H—H的键能为
。H—H的键能为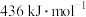 ,N—H的键能为
,N—H的键能为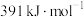 ,生成
,生成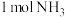 过程中放出46kJ的热量。则
过程中放出46kJ的热量。则 的键能为
的键能为___________  。
。
II.航天技术中使用的氢氧燃料电池具有高能、轻便和不污染环境等优点。
(3)某碱式氢氧燃料电池的电解质溶液是KOH溶液,则其负极反应为___________ 。
(4)氢氧燃料电池用于航天飞船,电极反应产生的水经过冷凝后可用作航天员的饮用水,当得到1.8g饮用水时,转移的电子数为___________ 。
I.
(1)下列反应中,属于吸热反应的是
①物质燃烧②炸药爆炸③浓硫酸稀释④二氧化碳通过炽热的碳⑤硝酸铵溶于水吸热⑥
 与
与 反应⑦铁粉与稀盐酸反应
反应⑦铁粉与稀盐酸反应(2)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为
 。H—H的键能为
。H—H的键能为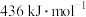 ,N—H的键能为
,N—H的键能为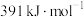 ,生成
,生成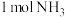 过程中放出46kJ的热量。则
过程中放出46kJ的热量。则 的键能为
的键能为 。
。II.航天技术中使用的氢氧燃料电池具有高能、轻便和不污染环境等优点。
(3)某碱式氢氧燃料电池的电解质溶液是KOH溶液,则其负极反应为
(4)氢氧燃料电池用于航天飞船,电极反应产生的水经过冷凝后可用作航天员的饮用水,当得到1.8g饮用水时,转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)已知下列各种共价键的键能:C—H:a kJ· mol-1、O—H:b kJ· mol-1、O=O:c kJ·mol-1、C=O:d kJ·mol-1。写出甲烷气体完全燃烧生成CO2气体和气体水的热化学方程式:_________________________________
(2)火箭中的主要燃料是“肼(也称为联氨)”的液体物质。此化合物的相对分子质量为32。其中,含N的质量分数为87.5%,其余为H元素。则:
①肼的化学式为__________________ ,其结构式为_____________________________
②此燃料的氧化剂是N2O4气体,若燃烧0.2 mol肼液体放出的热量为 400 kJ,燃烧的产物对大气都无污染(生成的水为液态),则肼与N2O4气体反应的热化学方程式为:__________________________
(2)火箭中的主要燃料是“肼(也称为联氨)”的液体物质。此化合物的相对分子质量为32。其中,含N的质量分数为87.5%,其余为H元素。则:
①肼的化学式为
②此燃料的氧化剂是N2O4气体,若燃烧0.2 mol肼液体放出的热量为 400 kJ,燃烧的产物对大气都无污染(生成的水为液态),则肼与N2O4气体反应的热化学方程式为:
您最近一年使用:0次





 白磷(
白磷( )燃烧生成
)燃烧生成 时放出2982
时放出2982 热量,白磷(
热量,白磷(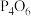 、
、 的结构如图所示,则上表中
的结构如图所示,则上表中

 完全反应生成固态
完全反应生成固态

