硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括___________ 、___________ 和玻璃。
(2)光导纤维的主要成分是 。
。 为
为___________ (“酸性”、“碱性”或“两性”)氧化物,写出 与烧碱反应的化学方程式
与烧碱反应的化学方程式___________ 。
(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是______(填字母)。
(4)硅单质可作硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:___________ 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成 、
、 和一种气体单质,写出发生反应的化学方程式
和一种气体单质,写出发生反应的化学方程式___________ ;在制备高纯硅的过程中若混入 ,可能引起的后果是
,可能引起的后果是___________ 。
(1)传统的无机非金属材料多为硅酸盐材料,主要包括
(2)光导纤维的主要成分是
 。
。 为
为 与烧碱反应的化学方程式
与烧碱反应的化学方程式(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是______(填字母)。
A. 能与水反应 能与水反应 | B. 在一定条件下能与氧化钙反应 在一定条件下能与氧化钙反应 |
C. 是制作光导纤维的主要原料 是制作光导纤维的主要原料 | D. 能与稀硫酸反应 能与稀硫酸反应 |
(4)硅单质可作硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:

②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成
 、
、 和一种气体单质,写出发生反应的化学方程式
和一种气体单质,写出发生反应的化学方程式 ,可能引起的后果是
,可能引起的后果是
更新时间:2024-04-24 14:20:54
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】盛放Na2CO3溶液等碱性溶液的试剂瓶为什么不用磨口玻璃塞?
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】请回答下列问题:
①光导纤维的成分是_______ (填化学式)。
②普通陶瓷的生产原料主要是_______ 。
③普通玻璃的主要成分是Na2SiO3、_______ (填化学式)和SiO2。
④水泥的主要性质是具有_______ 性。
⑤区别真丝织品和化纤织品的方法是取样后灼烧,若是真丝,则主要现象是__________ 。
①光导纤维的成分是
②普通陶瓷的生产原料主要是
③普通玻璃的主要成分是Na2SiO3、
④水泥的主要性质是具有
⑤区别真丝织品和化纤织品的方法是取样后灼烧,若是真丝,则主要现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】完成下列反应的化学方程式:
(1)氨的实验室制法_______ 。
(2)粗硅制取反应_______ 。
(3)二氧化氮与水反应_______ 。
(4)铜和浓硫酸反应_______ 。
(5)氨的催化氧化反应_______ 。
(1)氨的实验室制法
(2)粗硅制取反应
(3)二氧化氮与水反应
(4)铜和浓硫酸反应
(5)氨的催化氧化反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】I.完成以下方程式:⑴写离子方程式,⑵⑶⑷写化学方程式
⑴Na与H2O:________________ ;
⑵氢氧化亚铁露置在空气中:________________ ;
⑶制粗Si:________________ ;
⑷少量CO2通入Na2SiO3溶液:________________ 。
II.有以下物质:①Fe2O3②Na2CO3③Cl2④浓盐酸⑤浓硫酸⑥SO2⑦高岭石Al2(Si2O5)(OH)4
⑸属于碱性氧化物的是________________ (填序号);
⑹工业上用③与石灰乳制取漂白粉,漂白粉的有效成分的化学式是_____________ ;
⑺写出Cu与⑤反应的化学方程式________________ 。
⑻请将物质⑦改写成氧化物的形式________________ 。
⑴Na与H2O:
⑵氢氧化亚铁露置在空气中:
⑶制粗Si:
⑷少量CO2通入Na2SiO3溶液:
II.有以下物质:①Fe2O3②Na2CO3③Cl2④浓盐酸⑤浓硫酸⑥SO2⑦高岭石Al2(Si2O5)(OH)4
⑸属于碱性氧化物的是
⑹工业上用③与石灰乳制取漂白粉,漂白粉的有效成分的化学式是
⑺写出Cu与⑤反应的化学方程式
⑻请将物质⑦改写成氧化物的形式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】华为公司于2021年2月2日提交了一项全新的“硅碳复合材料”的专利,该专利可有效延长电池的使用寿命。该公司发行的5G平板电脑,创新搭载了3D石墨烯散热技术。华为还入股了国产碳化硅晶片制造行业。
(1)硅碳复合材料中以石墨为骨架,硅材料均匀分布在无定形碳中。工业上用焦炭还原石英砂(主要成分为SiO2)制取粗硅,该反应的化学方程式是__ 。
(2)石墨烯应用于5G平板电脑,是利用了石墨烯良好的__ 性。
(3)碳化硅的化学式是__ ,其中的碳原子和硅原子之间通过__ (填“离子”或“共价”)键相连,具有类似金刚石的结构,所以它具有的性质是__ (写一种)。
(1)硅碳复合材料中以石墨为骨架,硅材料均匀分布在无定形碳中。工业上用焦炭还原石英砂(主要成分为SiO2)制取粗硅,该反应的化学方程式是
(2)石墨烯应用于5G平板电脑,是利用了石墨烯良好的
(3)碳化硅的化学式是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】胃舒平主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·nH2O)等化合物。
(1)三硅酸镁的氧化物形式为_____ 。
(2)Al2O3、MgO和SiO2都可以制耐火材料,其原因是____ 。
a.Al2O3、MgO和SiO2都是白色固体
b.Al2O3、MgO和SiO2都是金属氧化物
c.Al2O3、MgO和SiO2都有很高的熔点
(1)三硅酸镁的氧化物形式为
(2)Al2O3、MgO和SiO2都可以制耐火材料,其原因是
a.Al2O3、MgO和SiO2都是白色固体
b.Al2O3、MgO和SiO2都是金属氧化物
c.Al2O3、MgO和SiO2都有很高的熔点
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)硅的原子结构示意图为_______ 。现代通信材料“光导纤维”的化学成分是_______ 。
(2)强碱缓慢腐蚀玻璃,盛强碱的试剂瓶瓶塞不能用玻璃塞的原因_______ 。(用离子方程式解释)
(3)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等。硅光电池是一种把_______ 能转化为_______ 能的装置。
(4)工业上可以通过如图所示的流程制取纯硅:
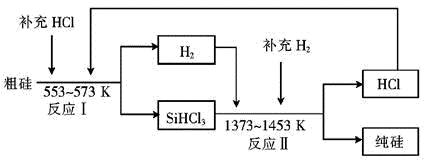
①若反应I为Si(粗)+3HCl SiHCl3+H2,则反应II的化学方程式为
SiHCl3+H2,则反应II的化学方程式为_______ 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程式:_______ 。
③假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%,则在第二轮次的生产中,补充投入HCl和H2的物质的量之比是_______ 。
(1)硅的原子结构示意图为
(2)强碱缓慢腐蚀玻璃,盛强碱的试剂瓶瓶塞不能用玻璃塞的原因
(3)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等。硅光电池是一种把
(4)工业上可以通过如图所示的流程制取纯硅:

①若反应I为Si(粗)+3HCl
 SiHCl3+H2,则反应II的化学方程式为
SiHCl3+H2,则反应II的化学方程式为②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程式:
③假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%,则在第二轮次的生产中,补充投入HCl和H2的物质的量之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】如何用所提供的试剂和方法除去各粉末状混合物中的杂质(括号内为杂质)。将所选答案的编号填在表中相应的空格内。
可供选择的试剂:A.盐酸 B.NaOH溶液 C.O2 D.水 E.不用其他试剂
可选用的操作:①水洗 ②加热 ③过滤 ④结晶
可供选择的试剂:A.盐酸 B.NaOH溶液 C.O2 D.水 E.不用其他试剂
可选用的操作:①水洗 ②加热 ③过滤 ④结晶
| 粉末状混合物 | 所选试剂 | 所选操作 | |
| (1) | CaCO3(SiO2) | ||
| (2) | NaCl(SiO2) | ||
| (3) | SiO2(Fe2O3) | ||
| (4) | SiO2(CaCO3) | ||
| (5) | SiO2(Si) | ||
| (6) | SiO2(H2SiO3) |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】材料是人类赖以生存的重要物质基础。材料种类很多,通常可分为金属材料、无机非金属材料、高分子合成材料及复合材料。
(1)生活中的铝合金属于上述材料中的___________ 。
(2)玻璃是重要的硅酸盐制品,生产玻璃时,纯碱和石英反应的化学方程式___________ 。
(3)在全球每年被腐蚀的钢铁中,电化学腐蚀比化学腐蚀所占比例___________ (填“高”或“低”),钢铁发生电化学吸氧腐蚀时,正极的电极反应方程式为___________ 。
(4)通常,在海水中行驶的轮船船身上装有一定数量的___________ (填“锌”或“铜”) 块来防止钢铁的腐蚀。自行车的钢圈通常采用___________ (填“涂油漆”或“镀Cr”) 防腐蚀。
(1)生活中的铝合金属于上述材料中的
(2)玻璃是重要的硅酸盐制品,生产玻璃时,纯碱和石英反应的化学方程式
(3)在全球每年被腐蚀的钢铁中,电化学腐蚀比化学腐蚀所占比例
(4)通常,在海水中行驶的轮船船身上装有一定数量的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的 。
。
(1)水晶和玛瑙的主要成分均为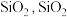 为
为___________ (填“酸性”、“碱性”或“两性”)氧化物,写出 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:___________ 。
(2)用 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作___________ 。
(3)工业上制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥 气体在300℃反应制得
气体在300℃反应制得 和
和 ;
;
③ 与过量
与过量 在1000~1100℃反应制得纯硅。
在1000~1100℃反应制得纯硅。
Ⅰ.第②步制备 反应的化学方程式为:
反应的化学方程式为:___________ ,步骤①②③中属于氧化还原反应的是___________ (填序号)。
Ⅱ.整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和另一种物质,写出该反应的化学方程式:
和另一种物质,写出该反应的化学方程式:___________ 。
 。
。(1)水晶和玛瑙的主要成分均为
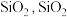 为
为 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:(2)用
 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作(3)工业上制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥
 气体在300℃反应制得
气体在300℃反应制得 和
和 ;
;③
 与过量
与过量 在1000~1100℃反应制得纯硅。
在1000~1100℃反应制得纯硅。Ⅰ.第②步制备
 反应的化学方程式为:
反应的化学方程式为:Ⅱ.整个制备过程必须严格控制无水无氧。
 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和另一种物质,写出该反应的化学方程式:
和另一种物质,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】N、Si、Al的化合物常用于制作新型无机非金属材料,如SiO2可用于制作光导纤维,AlN可用于制作耐高温材料,Al2O3可用于制作生物陶瓷。
(1)光导纤维应避免与碱性物质接触,推测SiO2属于___ 氧化物。
(2)用氯化铝和氮气经气相反应可以制得AlN。
①AlN中N元素的化合价为___ 。
②写出实验室制取氨气的化学方程式___ 。
③在水溶液中,氯化铝与氨气反应无法制得AlN,用化学方程式解释___ 。
(3)用铝土矿(主要成分为Al2O3)冶炼铝时,常用碱液浸取。写出Al2O3与NaOH溶液反应的离子方程式___ 。
(1)光导纤维应避免与碱性物质接触,推测SiO2属于
(2)用氯化铝和氮气经气相反应可以制得AlN。
①AlN中N元素的化合价为
②写出实验室制取氨气的化学方程式
③在水溶液中,氯化铝与氨气反应无法制得AlN,用化学方程式解释
(3)用铝土矿(主要成分为Al2O3)冶炼铝时,常用碱液浸取。写出Al2O3与NaOH溶液反应的离子方程式
您最近一年使用:0次



