名校
1 . 按要求填空:
Ⅰ.下列各组中的两种有机物,可能是:
(A)相同的物质,(B)同系物,(C)同分异构体。
(1)请判断它们之间的关系(用a、B、C填空)
①2-甲基丁烷和丁烷___________ ,
②正戊烷和2,2-二甲基丙烷___________ ,
③对二甲苯和1,4—二甲苯___________ ,
④1-己烯和环己烷___________ 。
Ⅱ.按官能团的不同,可以对有机物进行分类,将符合要求的答案(用序号填空)填在横线上。___________ ,
②醛:___________ ,
③酯:___________ 。
Ⅰ.下列各组中的两种有机物,可能是:
(A)相同的物质,(B)同系物,(C)同分异构体。
(1)请判断它们之间的关系(用a、B、C填空)
①2-甲基丁烷和丁烷
②正戊烷和2,2-二甲基丙烷
③对二甲苯和1,4—二甲苯
④1-己烯和环己烷
Ⅱ.按官能团的不同,可以对有机物进行分类,将符合要求的答案(用序号填空)填在横线上。
①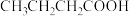 ②
②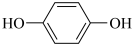 ③
③ 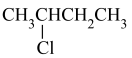 ④
④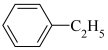 ⑤
⑤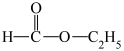 ⑥
⑥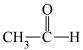
②醛:
③酯:
您最近一年使用:0次
2 . 金属钛(Ti)及其化合物广泛应用于航空航天,被称为“未来世界的金属”。
(1)按电子排布Ti元素在元素周期表分区中属于___________ 区元素,钛元素基态原子未成对电子数为___________ 个。
(2)某含钛化合物的化学式为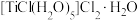 ,化合物中含有的化学键类型是
,化合物中含有的化学键类型是___________ ,0.5 mol该配合物中含有的σ键数目是___________ 。
(3)二氧化钛是很好的催化剂,可以催化如下反应: 杂化的碳原子个数与
杂化的碳原子个数与 杂化的碳原子个数之比为
杂化的碳原子个数之比为___________ ;化合物乙中采取 杂化的原子的第一电离能由大到小的顺序为
杂化的原子的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(4) 、
、 、KH按熔点由高到低的顺序排列为
、KH按熔点由高到低的顺序排列为___________ ,熔点差异的原因:___________ 。
(1)按电子排布Ti元素在元素周期表分区中属于
(2)某含钛化合物的化学式为
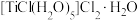 ,化合物中含有的化学键类型是
,化合物中含有的化学键类型是(3)二氧化钛是很好的催化剂,可以催化如下反应:
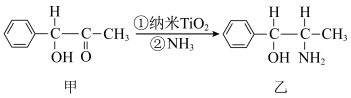
 杂化的碳原子个数与
杂化的碳原子个数与 杂化的碳原子个数之比为
杂化的碳原子个数之比为 杂化的原子的第一电离能由大到小的顺序为
杂化的原子的第一电离能由大到小的顺序为(4)
 、
、 、KH按熔点由高到低的顺序排列为
、KH按熔点由高到低的顺序排列为
您最近一年使用:0次
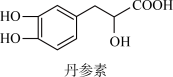
3 . 丹参素能明显抑制血小板的聚集,其结构如图所示。___________ 。
(2)丹参素___________ (填“是”或“否”)属于芳香烃。
(3)下列反应类型中丹参素不能发生的___________ (填序号)。
①加成反应 ②取代反应 ③氧化反应 ④加聚反应
(4)向丹参素溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丹参素溶液具有___________ 性。
(5)根据丹参素结构,预测1mol丹参素和足量的氢氧化钠溶液反应时,最多能够消耗___________ molNaOH;1mol丹参素与足量Na反应,可以产生___________ mol 。
。
已知:①在表示有机化合物的组成和结构时,如果将碳、氢元素符号省略,只表示分子中键的连接情况和官能团,每个拐点或终点均表示有一个碳原子,则得到键线式。如丙烯可表示为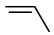 ,乙醇可表示为
,乙醇可表示为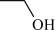 。
。
③苯酚(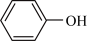 )是最简单的酚,酚羟基在水中可微弱电离,产生
)是最简单的酚,酚羟基在水中可微弱电离,产生 而显弱酸性
而显弱酸性
(2)丹参素
(3)下列反应类型中丹参素不能发生的
①加成反应 ②取代反应 ③氧化反应 ④加聚反应
(4)向丹参素溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丹参素溶液具有
(5)根据丹参素结构,预测1mol丹参素和足量的氢氧化钠溶液反应时,最多能够消耗
 。
。
您最近一年使用:0次
解题方法
4 . 认识有机物组成和结构对有机物的学习非常重要。
Ⅰ.根据下列有机物的空间填充模型,填空。_______ 种;
(2)乙中σ键与π键的个数比为_______ ;
(3)丙中碳原子的杂化方式_______ ;
(4)丁的结构简式为_______ ;
(5)分子中所有原子一定在同一平面内的是_______ (填序号)。
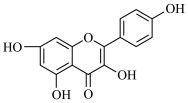
Ⅱ.中药小柴胡可以用来治疗感冒发烧,其主要成分之一是山奈酚,结构如图所示。_______ mol  。
。
Ⅲ.以下是几种烃分子的球棍模型:_______ 。
(8)写出D的键线式_______ 。
Ⅰ.根据下列有机物的空间填充模型,填空。
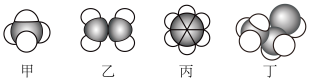
(2)乙中σ键与π键的个数比为
(3)丙中碳原子的杂化方式
(4)丁的结构简式为
(5)分子中所有原子一定在同一平面内的是
Ⅱ.中药小柴胡可以用来治疗感冒发烧,其主要成分之一是山奈酚,结构如图所示。
 。
。Ⅲ.以下是几种烃分子的球棍模型:
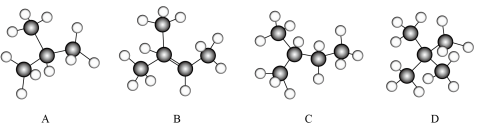
(8)写出D的键线式
您最近一年使用:0次
5 . 氢气是未来理想的能源。
(1)实验室用铁与 的硫酸反应生成
的硫酸反应生成 的物质的量与反应时间的关系如图所示。按要求回答下列问题:
的物质的量与反应时间的关系如图所示。按要求回答下列问题: 的平均反应速率最大的时间段是
的平均反应速率最大的时间段是_______ (填“0~2min”“2~4min”或“4~6min”),该时间段内对反应速率起关键作用的影响因素是_______ 。
②若向体系中加入少量硫酸铜溶液,可以加快氢气的生成速率,其原因是_______ 。
③要加快上述实验中产生氢气的速率,还可采取的措施是_______ (填一种)。
(2)工业上用海水制氢气的新技术的原理为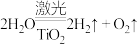 。回答下列问题:
。回答下列问题:
①分解海水的反应属于_______ 反应(填“放热”或“吸热”)。
②分解产生的氢气储存比较困难,有一种储存方法的原理可表示为
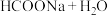 。下列说法正确的是
。下列说法正确的是_______ (填序号)。
A.储氢、释氢过程中均有能量变化
B.储氢时反应物中只有离子键的断裂
C.储氢过程中, 被还原
被还原
D.释氢过程中,每消耗0.1mol 放出2.24L
放出2.24L
(3) 可与
可与 发生反应:
发生反应: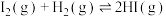 。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是_______(填序号)。
。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是_______(填序号)。
(1)实验室用铁与
 的硫酸反应生成
的硫酸反应生成 的物质的量与反应时间的关系如图所示。按要求回答下列问题:
的物质的量与反应时间的关系如图所示。按要求回答下列问题: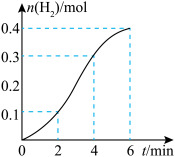
 的平均反应速率最大的时间段是
的平均反应速率最大的时间段是②若向体系中加入少量硫酸铜溶液,可以加快氢气的生成速率,其原因是
③要加快上述实验中产生氢气的速率,还可采取的措施是
(2)工业上用海水制氢气的新技术的原理为
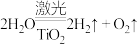 。回答下列问题:
。回答下列问题:①分解海水的反应属于
②分解产生的氢气储存比较困难,有一种储存方法的原理可表示为

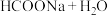 。下列说法正确的是
。下列说法正确的是A.储氢、释氢过程中均有能量变化
B.储氢时反应物中只有离子键的断裂
C.储氢过程中,
 被还原
被还原D.释氢过程中,每消耗0.1mol
 放出2.24L
放出2.24L
(3)
 可与
可与 发生反应:
发生反应: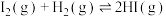 。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是_______(填序号)。
。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是_______(填序号)。A. |
| B.断裂1mol H―H键的同时形成1mol I―I键 |
| C.容器内气体的压强不变 |
| D.容器内气体的颜色不变 |
您最近一年使用:0次
6 . 用系统命名法命名下列物质:
①
____________ 
____________
①

②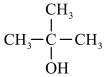
③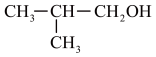
④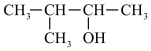

您最近一年使用:0次
名校
7 . 环境保护与绿色发展是新时代人们关心的共同话题。NO、 是大气主要污染物,因此对工业烟气(主要成分为
是大气主要污染物,因此对工业烟气(主要成分为 ,
, 、
、 )脱硝是工业生产中的重要一环。脱除的方法有多种,比较常见的有水吸收法、酸吸收法、碱吸收法、氧化吸收法、还原吸收法和综合吸收法等。
)脱硝是工业生产中的重要一环。脱除的方法有多种,比较常见的有水吸收法、酸吸收法、碱吸收法、氧化吸收法、还原吸收法和综合吸收法等。
(1)碱液吸收:NaOH溶液可吸收工业烟气,获得副产品 。
。
①等物质的量的NO与 被NaOH溶液吸收,反应的离子方程式为
被NaOH溶液吸收,反应的离子方程式为____________ 。
②若吸收时NO与 的比例控制不当,则吸收液经浓缩结晶、过滤得到的
的比例控制不当,则吸收液经浓缩结晶、过滤得到的 晶体中最有可能混有的杂质是
晶体中最有可能混有的杂质是______ (填化学式)。
(2)目前常见方法是采用酸化处理的NaClO溶液液相氧化法脱除烟气中的 ,其主要过程如下:
,其主要过程如下:
Ⅰ.
 kJ/mol
kJ/mol
Ⅱ.
 kJ/mol
kJ/mol
①写出 转化为
转化为 的热化学方程式:
的热化学方程式:____________ 。
②研究不同温度下对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是______ 。
(3)氨气催化吸收处理尾气法:已知6mol氨气恰好能将含NO和 共7mol的混合气体完全转化为
共7mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比为
的物质的量之比为______ 。
方法1:直接使用尿素 溶液吸收烟气中的
溶液吸收烟气中的 。
。
方法2:先用合适的氧化剂将 中的NO氧化为
中的NO氧化为 ,再用
,再用 溶液还原吸收。
溶液还原吸收。
还原吸收等量的 ,消耗尿素较少的是
,消耗尿素较少的是______ (填“方法1”或“方法2”)。工业上选择方法2处理 的原因是
的原因是____________ 。
 是大气主要污染物,因此对工业烟气(主要成分为
是大气主要污染物,因此对工业烟气(主要成分为 ,
, 、
、 )脱硝是工业生产中的重要一环。脱除的方法有多种,比较常见的有水吸收法、酸吸收法、碱吸收法、氧化吸收法、还原吸收法和综合吸收法等。
)脱硝是工业生产中的重要一环。脱除的方法有多种,比较常见的有水吸收法、酸吸收法、碱吸收法、氧化吸收法、还原吸收法和综合吸收法等。(1)碱液吸收:NaOH溶液可吸收工业烟气,获得副产品
 。
。①等物质的量的NO与
 被NaOH溶液吸收,反应的离子方程式为
被NaOH溶液吸收,反应的离子方程式为②若吸收时NO与
 的比例控制不当,则吸收液经浓缩结晶、过滤得到的
的比例控制不当,则吸收液经浓缩结晶、过滤得到的 晶体中最有可能混有的杂质是
晶体中最有可能混有的杂质是(2)目前常见方法是采用酸化处理的NaClO溶液液相氧化法脱除烟气中的
 ,其主要过程如下:
,其主要过程如下:Ⅰ.

 kJ/mol
kJ/molⅡ.

 kJ/mol
kJ/mol①写出
 转化为
转化为 的热化学方程式:
的热化学方程式:②研究不同温度下对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
(3)氨气催化吸收处理尾气法:已知6mol氨气恰好能将含NO和
 共7mol的混合气体完全转化为
共7mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比为
的物质的量之比为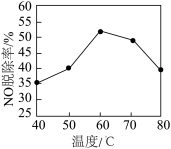
方法1:直接使用尿素
 溶液吸收烟气中的
溶液吸收烟气中的 。
。方法2:先用合适的氧化剂将
 中的NO氧化为
中的NO氧化为 ,再用
,再用 溶液还原吸收。
溶液还原吸收。还原吸收等量的
 ,消耗尿素较少的是
,消耗尿素较少的是 的原因是
的原因是
您最近一年使用:0次
名校
8 . 氮族元素是位于元素周期表ⅤA族的元素,包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)等,这一族元素在化合物中可以呈现-3、+1、+2、+3、+4、+5等多种化合价,它们的原子最外层都有5个电子。回答下列问题:
(1)白磷( )分子为正四面体结构,
)分子为正四面体结构, 键角为
键角为______ 。
(2)第三周期元素中第一电离能比P小的元素有______ 种。
(3)写出基态As原子核外简化电子排布式:______ 。
(4)根据铋(Bi)核外电子排布,得知Bi属于周期表______ 区。
(5)五氧化二锑( )可由
)可由 通过水解制得,写出该反应的化学方程式:
通过水解制得,写出该反应的化学方程式:____________ ;为提高水解率可采取的措施有______ 。
(1)白磷(
 )分子为正四面体结构,
)分子为正四面体结构, 键角为
键角为(2)第三周期元素中第一电离能比P小的元素有
(3)写出基态As原子核外简化电子排布式:
(4)根据铋(Bi)核外电子排布,得知Bi属于周期表
(5)五氧化二锑(
 )可由
)可由 通过水解制得,写出该反应的化学方程式:
通过水解制得,写出该反应的化学方程式:
您最近一年使用:0次
名校
9 .  (亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂。
(亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂。
(1)用石灰乳吸收硝酸工业尾气中 、
、 ,既能获得
,既能获得 ,亦能净化尾气。
,亦能净化尾气。
① 和
和 与石灰乳生成
与石灰乳生成 的化学方程式为
的化学方程式为_______ 。
②下列措施能提高尾气中 和
和 去除率的有
去除率的有_______ (填字母)
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量石灰乳
③吸收后经处理得到 晶体,该晶体的主要杂质是
晶体,该晶体的主要杂质是_______ (填化学式);吸收后排放的尾气含量较高的氮氧化物是_______ (填化学式)。
(2)实验室可用反应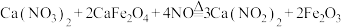 制备
制备 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为_______ 。对于 硫酸和硝酸的混合溶液,若硫酸和硝酸的物质的量浓度存在如下关系:
硫酸和硝酸的混合溶液,若硫酸和硝酸的物质的量浓度存在如下关系: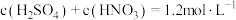 ,则理论上最多能溶解的铜的物质的量为
,则理论上最多能溶解的铜的物质的量为_______  .
.
 (亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂。
(亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂。(1)用石灰乳吸收硝酸工业尾气中
 、
、 ,既能获得
,既能获得 ,亦能净化尾气。
,亦能净化尾气。①
 和
和 与石灰乳生成
与石灰乳生成 的化学方程式为
的化学方程式为②下列措施能提高尾气中
 和
和 去除率的有
去除率的有A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量石灰乳
③吸收后经处理得到
 晶体,该晶体的主要杂质是
晶体,该晶体的主要杂质是(2)实验室可用反应
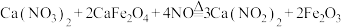 制备
制备 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为 硫酸和硝酸的混合溶液,若硫酸和硝酸的物质的量浓度存在如下关系:
硫酸和硝酸的混合溶液,若硫酸和硝酸的物质的量浓度存在如下关系: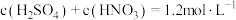 ,则理论上最多能溶解的铜的物质的量为
,则理论上最多能溶解的铜的物质的量为 .
.
您最近一年使用:0次
名校
10 . 研究 、
、 、CO等大气污染气体的处理具有重要意义。可采用还原法处理氮的氧化物,一定条件下
、CO等大气污染气体的处理具有重要意义。可采用还原法处理氮的氧化物,一定条件下 还原NO生成
还原NO生成 和气态水。已知几种化学键的键能数据如下:
和气态水。已知几种化学键的键能数据如下:
写出 还原NO生成
还原NO生成 和气态水的热化学方程式
和气态水的热化学方程式___________ 。
 、
、 、CO等大气污染气体的处理具有重要意义。可采用还原法处理氮的氧化物,一定条件下
、CO等大气污染气体的处理具有重要意义。可采用还原法处理氮的氧化物,一定条件下 还原NO生成
还原NO生成 和气态水。已知几种化学键的键能数据如下:
和气态水。已知几种化学键的键能数据如下:| 化学键 | H—H | NO中的共价键 | N≡N | H—O |
键能( ) ) | 436 | 630 | 946 | 463 |
 还原NO生成
还原NO生成 和气态水的热化学方程式
和气态水的热化学方程式
您最近一年使用:0次



