名校
解题方法
1 . 高铁酸钾 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是| A.氢氧化铁胶体具有碱性,可用于净水 |
B. 具有氧化性,可作为特定环境中的抗氧化剂 具有氧化性,可作为特定环境中的抗氧化剂 |
| C.高铁酸钾能溶于水,水溶液呈紫色,可作氧化剂 |
| D.氧化铁呈红棕色且遮盖效果好,可用作红色颜料 |
您最近一年使用:0次
2023-12-31更新
|
258次组卷
|
2卷引用:新疆乌鲁木齐市第十二中学2023-2024学年高三下学期2月月考化学试题
名校
解题方法
2 . 下列物质的性质与用途具有对应关系的是
| A.二氧化氯具有强氧化性,可用来漂白织物 |
| B.铝合金的熔点比纯铝低,所以硬铝是制造飞机的理想材料 |
| C.碳酸氢钠能与碱反应,可用作食品膨松剂 |
D. 是淡黄色固体,在呼吸面具中用作供氧剂 是淡黄色固体,在呼吸面具中用作供氧剂 |
您最近一年使用:0次
2023-07-17更新
|
159次组卷
|
4卷引用:新疆生产建设兵团第三师图木舒克市第二中学2023-2024学年高一下学期开学考试化学试题
新疆生产建设兵团第三师图木舒克市第二中学2023-2024学年高一下学期开学考试化学试题吉林省长春吉大附中实验学校2023-2024学年高一上学期1月期末化学试题甘肃省酒泉市2022-2023学年高一上学期1月期末考试化学试题(已下线)专项05 常见物质的性质、用途与转化-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
3 . 物质的性质决定用途。下列两者对应关系正确的是
| A.铝具有还原性,可用于制作门窗框架 |
| B.晶体硅的硬度大、熔点高,可用来制作计算机芯片 |
| C.硝酸具有强氧化性,可用作纺织品漂白 |
| D.NH4Cl溶液呈酸性,可用于去除铁锈 |
您最近一年使用:0次
4 . 下列实验有关离子检验的操作及现象与结论之间对应关系正确的是
| 选项 | 操作及现象 | 结论 |
| A | 向某溶液中加稀盐酸酸化的 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 该溶液中含 |
| B | 向某溶液中加入过量盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中含 |
| C | 向某盐溶液中加入浓NaOH并加热,产生能使湿润的红色石蕊试纸变蓝的气体 | 该盐溶液中含 |
| D | 向某溶液滴加稀盐酸酸化的 溶液,产生白色沉淀 溶液,产生白色沉淀 | 该溶液中含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 氨在人类的生产和生活中有着广泛的应用。某化学兴趣小组为了制取并探究氨气的性质,用下列装置(部分夹持装置已略去)进行实验。 装置,则该反应的化学方程式为
装置,则该反应的化学方程式为___________ 。
(2)B装置中的干燥剂可选用___________ (填名称)。
(3)气体通过C、D装置时,试纸颜色会发生变化的是___________ (填“C”或“D”)装置。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___________ ,发生该反应的化学方程式为___________ 。
(5)F装置中倒置漏斗的作用是___________ ,与F有相同作用的装置为___________ (填序号)。
(6)氨的用途很广,如:①用氨处理二氧化氮: ,该反应中氨体现
,该反应中氨体现___________ (填“氧化性”或“还原性”);②工业上用氨气制硝酸,首先将氨气催化氧化,写出氨气催化氧化的化学方程式___________ 。
(7)氨气极易溶于水,会形成喷泉实验,实验装置如图所示。下列可以产生类似现象的组合为___________ 。

 装置,则该反应的化学方程式为
装置,则该反应的化学方程式为(2)B装置中的干燥剂可选用
(3)气体通过C、D装置时,试纸颜色会发生变化的是
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)F装置中倒置漏斗的作用是
|
|
|
| Ⅰ | Ⅱ | Ⅲ |
(6)氨的用途很广,如:①用氨处理二氧化氮:
 ,该反应中氨体现
,该反应中氨体现(7)氨气极易溶于水,会形成喷泉实验,实验装置如图所示。下列可以产生类似现象的组合为

| 圆底烧瓶(干燥气体) | 烧杯及胶头滴管(液体) | |
| A | NO | 水 |
| B |  | 4mol/L NaOH溶液 |
| C |  | 饱和NaCl溶液 |
| D |  | 1mol/L盐酸 |
您最近一年使用:0次
2024-06-05更新
|
207次组卷
|
2卷引用:新疆乌鲁木齐市第十一中学2023-2024学年高一下学期期中测试化学试卷
解题方法
6 . 以菱锰矿(主要成分为MnCO3,还含有铁、镍的碳酸盐以及SiO2杂质)为原料生产次锰酸钠(Na3MnO4)的工艺流程如图:
(1)次锰酸钠中Mn的化合价为___________ ;滤渣1的主要成分为MnO2和___________ (填化学式)。
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为___________ 。___________ 。
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)。反应的平衡常数K=___________ 。
(5)“母液1”中主要溶质的用途___________ 。
(6)煅烧产物MnO2在“共熔”过程中,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为___________ 。
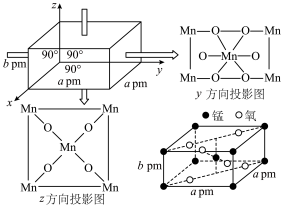
(7)某MnxO,四方晶胞结构及其投影如图所示,该晶胞由O2-和Mn3+构成。___________ ,Mn与Mn之间最近(顶点和体心)距离为___________ pm。(用含a、b的代数式表示)

| 物质 | MnS | NiS |
| Ksp | 2.0×10-13 | 1.0×10-21 |
(1)次锰酸钠中Mn的化合价为
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为
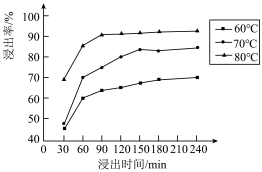
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)。反应的平衡常数K=
(5)“母液1”中主要溶质的用途
(6)煅烧产物MnO2在“共熔”过程中,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为
(7)某MnxO,四方晶胞结构及其投影如图所示,该晶胞由O2-和Mn3+构成。
您最近一年使用:0次
解题方法
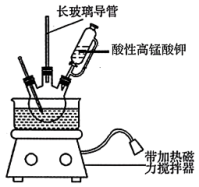
7 . 3,4-亚甲二氧基苯甲酸是一种用途广泛的有机合成中间体,微溶于水。实验室可用KMnO4氧化3,4-亚甲二氧基苯甲醛(油状液体)制备,实验装置如下图(夹持仪器已省略),其反应方程式为:
步骤1:向三颈烧瓶中加入3,4-亚甲二氧基苯甲醛11.2mL(约15.0g)和一定量水,缓慢开启搅拌器并加热。于70~80℃滴加稍过量的酸性KMnO4溶液,反应结束后,加入KOH溶液至碱性。
步骤2:趁热过滤,洗涤滤渣。合并滤液和洗涤液,向其中加入硫酸至水层不再产生沉淀。
步骤3:抽滤,洗涤,干燥,得3,4-亚甲二氧基苯甲酸固体12.2g。
回答下列问题:
(1)盛酸性KMnO4溶液的仪器的名称是___________ ;实验装置中长玻璃导管可用___________ 代替(填仪器名称)。
(2)反应结束后,加入KOH溶液前需向溶液中加入H2C2O4溶液在酸性条件下处理,发生反应的离子方程式为___________ 。
(3)步骤1中加入KOH溶液至碱性的目的是___________ 。
(4)步骤2中趁热过滤除去的物质是___________ (填化学式)。
(5)步骤3中检验产品是否洗净的操作为___________ 。
(6)写出步骤2中加入H2SO4发生的化学方程式___________ 。
(7)本实验3,4-亚甲二氧基苯甲酸的产率约为___________ %(保留两位小数)
3 +2KMnO4→2
+2KMnO4→2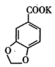 +
+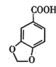 +2MnO2↓+H2O
+2MnO2↓+H2O
步骤1:向三颈烧瓶中加入3,4-亚甲二氧基苯甲醛11.2mL(约15.0g)和一定量水,缓慢开启搅拌器并加热。于70~80℃滴加稍过量的酸性KMnO4溶液,反应结束后,加入KOH溶液至碱性。
步骤2:趁热过滤,洗涤滤渣。合并滤液和洗涤液,向其中加入硫酸至水层不再产生沉淀。
步骤3:抽滤,洗涤,干燥,得3,4-亚甲二氧基苯甲酸固体12.2g。
回答下列问题:
(1)盛酸性KMnO4溶液的仪器的名称是
(2)反应结束后,加入KOH溶液前需向溶液中加入H2C2O4溶液在酸性条件下处理,发生反应的离子方程式为
(3)步骤1中加入KOH溶液至碱性的目的是
(4)步骤2中趁热过滤除去的物质是
(5)步骤3中检验产品是否洗净的操作为
(6)写出步骤2中加入H2SO4发生的化学方程式
(7)本实验3,4-亚甲二氧基苯甲酸的产率约为
您最近一年使用:0次
解题方法
8 . 化学在生产、生活中有着重要用途,下列物质的用途或成分正确的有
①过氧化钠可作潜水艇供氧剂②铁红常用作红色油漆③ 可制造耐火材料④
可制造耐火材料④ 水溶液俗称水玻璃可用作木材防火剂⑤硅单质可用作计算机芯片⑥二氧化硅可用作光导纤维⑦明矾可用于净水⑧青铜主要成分是铜锌合金⑨小苏打可作发酵粉⑩烧碱可用作治疗胃酸过多的药
水溶液俗称水玻璃可用作木材防火剂⑤硅单质可用作计算机芯片⑥二氧化硅可用作光导纤维⑦明矾可用于净水⑧青铜主要成分是铜锌合金⑨小苏打可作发酵粉⑩烧碱可用作治疗胃酸过多的药
①过氧化钠可作潜水艇供氧剂②铁红常用作红色油漆③
 可制造耐火材料④
可制造耐火材料④ 水溶液俗称水玻璃可用作木材防火剂⑤硅单质可用作计算机芯片⑥二氧化硅可用作光导纤维⑦明矾可用于净水⑧青铜主要成分是铜锌合金⑨小苏打可作发酵粉⑩烧碱可用作治疗胃酸过多的药
水溶液俗称水玻璃可用作木材防火剂⑤硅单质可用作计算机芯片⑥二氧化硅可用作光导纤维⑦明矾可用于净水⑧青铜主要成分是铜锌合金⑨小苏打可作发酵粉⑩烧碱可用作治疗胃酸过多的药| A.7个 | B.8个 | C.9个 | D.10个 |
您最近一年使用:0次
9 . 黄铁矿(FeS2)在工业上有着重要的用途,黄铁矿在空气中煅烧的反应为:4FeS2+11O2 2Fe2O3+8SO2,生成的SO2可用于生产Na2SO3和H2SO4。FeS2立方晶胞如图,其晶胞边长为a nm。下列有关说法不正确的是
2Fe2O3+8SO2,生成的SO2可用于生产Na2SO3和H2SO4。FeS2立方晶胞如图,其晶胞边长为a nm。下列有关说法不正确的是
 2Fe2O3+8SO2,生成的SO2可用于生产Na2SO3和H2SO4。FeS2立方晶胞如图,其晶胞边长为a nm。下列有关说法不正确的是
2Fe2O3+8SO2,生成的SO2可用于生产Na2SO3和H2SO4。FeS2立方晶胞如图,其晶胞边长为a nm。下列有关说法不正确的是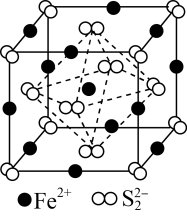
| A.FeS2中存在非极性共价键 |
B. 的空间构型为三角锥形 的空间构型为三角锥形 |
| C.SO2能使酸性高锰酸钾溶液褪色,说明SO2具有漂白性 |
D.晶胞中Fe2+位于S2-所形成的正八面体的体心,该正八面体的边长为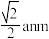 |
您最近一年使用:0次
解题方法
10 . 磁性氧化铁是生产颜料、抛光剂、录音磁带和电讯器材的重要原料。以高硫铝土矿(主要含Al2O3、Fe2O3、SiO2和少量的FeS2等)提取氧化铝和磁性氧化铁的流程如图:
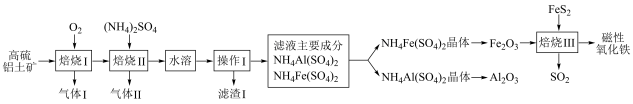
(1)基态Fe原子价层电子的轨道表示式(电子排布图)为______ ;基态Al原子电子占据最高能级的电子云轮廓图为______ 形;
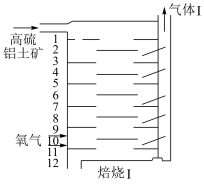
(2)“焙烧Ⅰ”过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是:______ (任答一点)。
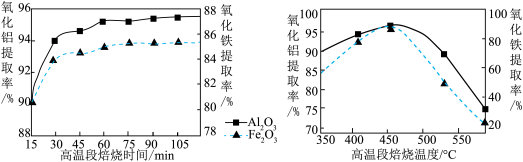
(3)焙烧Ⅱ由氧化铝、氧化铁制得可溶性的NH4Al(SO4)2、NH4Fe(SO4)2.提取率随温度、时间变化曲线如图所示,最佳的焙烧时间与温度是______ 。写出由氧化铝制得可溶性的NH4Al(SO4)2相关的化学反应方程式为______ 。
(4)写出“滤渣I”主要成分的一种用途______ 。
(5)“焙烧Ⅲ”在隔绝空气的条件下进行反应,理论上完全反应时参加反应的n(FeS2):n(Fe2O3)=______ 。
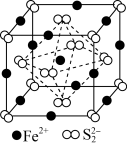
(6)FeS2晶体的晶胞结构如图所示。晶胞参数为apm,FeS2晶体的密度为ρg•cm−3,阿伏加德罗常数的值为NA,则FeS2的摩尔质量M=______ g⋅mol﹣1(用含a、ρ、NA的代数式表示)。

(1)基态Fe原子价层电子的轨道表示式(电子排布图)为
(2)“焙烧Ⅰ”过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是:

(3)焙烧Ⅱ由氧化铝、氧化铁制得可溶性的NH4Al(SO4)2、NH4Fe(SO4)2.提取率随温度、时间变化曲线如图所示,最佳的焙烧时间与温度是

(4)写出“滤渣I”主要成分的一种用途
(5)“焙烧Ⅲ”在隔绝空气的条件下进行反应,理论上完全反应时参加反应的n(FeS2):n(Fe2O3)=
(6)FeS2晶体的晶胞结构如图所示。晶胞参数为apm,FeS2晶体的密度为ρg•cm−3,阿伏加德罗常数的值为NA,则FeS2的摩尔质量M=

您最近一年使用:0次






