1 . 针对表中10种元素及由这些元素形成的单质和化合物,用元素符号或者化学式填写以下空格。
(1)最活泼的金属元素是___________ ,最活泼的非金属元素是___________ ,最不活泼的元素是___________ 。
(2)碱性最强的最高价氧化物对应水化物是___________ ,酸性最强的最高价氧化物对应水化物是___________ ,最稳定的气态氢化物是___________ 。
(3)在④与⑤中,还原性较强的是___________ ,在⑧与⑨的单质中,氧化性较强的是___________ 。
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:___________ ;用电子式表示④和⑧形成的化合物的形成过程___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)碱性最强的最高价氧化物对应水化物是
(3)在④与⑤中,还原性较强的是
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近一年使用:0次
名校
解题方法
2 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
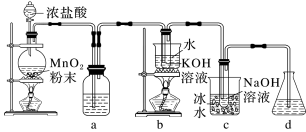
回答下列问题:
(1)浓盐酸在反应过程中表现出来的性质有:___________ (填字母)。
a.酸性 b.氧化性 c.还原性 d.碱性 e.易挥发性
(2)a中的试剂为___________ 。b中发生的化学反应的离子方程式是___________ 。
(3)d中可选用试剂___________ (填字母)。
a. 溶液 b.饱和
溶液 b.饱和 溶液 c.石灰乳 d.稀
溶液 c.石灰乳 d.稀
(4)反应结束后,取出b中试管,经冷却结晶,过滤,___________ ,干燥,得到 晶体。
晶体。
(5)取少量 和
和 溶液置于两支试管中,分别滴加一定浓度的中性淀粉
溶液置于两支试管中,分别滴加一定浓度的中性淀粉 溶液。装有
溶液。装有 的试管溶液颜色不变,装有
的试管溶液颜色不变,装有 的试管溶液变为蓝色。由此可知在该条件下,氧化能力
的试管溶液变为蓝色。由此可知在该条件下,氧化能力
___________  (填“大于”或“小于”)。溶液变蓝的试管内发生反应的离子方程式为:
(填“大于”或“小于”)。溶液变蓝的试管内发生反应的离子方程式为:___________ 。
 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
回答下列问题:
(1)浓盐酸在反应过程中表现出来的性质有:
a.酸性 b.氧化性 c.还原性 d.碱性 e.易挥发性
(2)a中的试剂为
(3)d中可选用试剂
a.
 溶液 b.饱和
溶液 b.饱和 溶液 c.石灰乳 d.稀
溶液 c.石灰乳 d.稀
(4)反应结束后,取出b中试管,经冷却结晶,过滤,
 晶体。
晶体。(5)取少量
 和
和 溶液置于两支试管中,分别滴加一定浓度的中性淀粉
溶液置于两支试管中,分别滴加一定浓度的中性淀粉 溶液。装有
溶液。装有 的试管溶液颜色不变,装有
的试管溶液颜色不变,装有 的试管溶液变为蓝色。由此可知在该条件下,氧化能力
的试管溶液变为蓝色。由此可知在该条件下,氧化能力
 (填“大于”或“小于”)。溶液变蓝的试管内发生反应的离子方程式为:
(填“大于”或“小于”)。溶液变蓝的试管内发生反应的离子方程式为:
您最近一年使用:0次
2023-12-21更新
|
132次组卷
|
2卷引用:新疆乌鲁木齐市实验学校2023-2024学年高一上学期1月期末化学试题
名校
3 . 二氧化氯( )具有强氧化性,是一种常用的消毒剂。它是一种易溶于水且不与水反应的黄绿色气体,沸点为11℃,可通过
)具有强氧化性,是一种常用的消毒剂。它是一种易溶于水且不与水反应的黄绿色气体,沸点为11℃,可通过 与酸性
与酸性 溶液反应制备。某化学兴趣小组同学设计了如图所示装置制备
溶液反应制备。某化学兴趣小组同学设计了如图所示装置制备 并探究其性质。
并探究其性质。
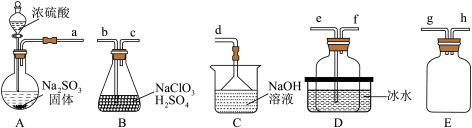
已知:浓硫酸与 固体反应可用来制备
固体反应可用来制备 ,二氧化硫易溶于水,具有还原性,在水溶液中易被氧化成
,二氧化硫易溶于水,具有还原性,在水溶液中易被氧化成 。回答下列问题:
。回答下列问题:
(1)A中盛装浓 的仪器名称是
的仪器名称是_______ 。
(2)通过装置B中反应制备 ,其化学反应方程式为
,其化学反应方程式为_______ 。
(3)欲制备一瓶 ,选择上图中的装置,其接口的连接顺序为a→g→h→
,选择上图中的装置,其接口的连接顺序为a→g→h→_______ 。
(4)装置D盛放冰水的目的是_______ 。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是每克含氯消毒剂的氧化能力相当于多少克 的氧化能力(还原产物均为氯离子)。
的氧化能力(还原产物均为氯离子)。 的有效氯含量为
的有效氯含量为_______ g。(计算结果保留一位小数)
 )具有强氧化性,是一种常用的消毒剂。它是一种易溶于水且不与水反应的黄绿色气体,沸点为11℃,可通过
)具有强氧化性,是一种常用的消毒剂。它是一种易溶于水且不与水反应的黄绿色气体,沸点为11℃,可通过 与酸性
与酸性 溶液反应制备。某化学兴趣小组同学设计了如图所示装置制备
溶液反应制备。某化学兴趣小组同学设计了如图所示装置制备 并探究其性质。
并探究其性质。
已知:浓硫酸与
 固体反应可用来制备
固体反应可用来制备 ,二氧化硫易溶于水,具有还原性,在水溶液中易被氧化成
,二氧化硫易溶于水,具有还原性,在水溶液中易被氧化成 。回答下列问题:
。回答下列问题:(1)A中盛装浓
 的仪器名称是
的仪器名称是(2)通过装置B中反应制备
 ,其化学反应方程式为
,其化学反应方程式为(3)欲制备一瓶
 ,选择上图中的装置,其接口的连接顺序为a→g→h→
,选择上图中的装置,其接口的连接顺序为a→g→h→(4)装置D盛放冰水的目的是
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是每克含氯消毒剂的氧化能力相当于多少克
 的氧化能力(还原产物均为氯离子)。
的氧化能力(还原产物均为氯离子)。 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
2022-12-22更新
|
91次组卷
|
2卷引用:新疆乌鲁木齐市高级中学2023-2024学年高三上学期1月月考化学试题
名校
解题方法
4 . 某小组为验证SO2的性质设计如图所示的实验装置,下列说法错误的是
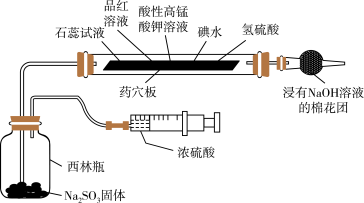

| A.一段时间后石蕊溶液和品红溶液均褪色,说明SO2有漂白性 |
| B.一段时间后酸性高锰酸钾溶液、碘水褪色,说明SO2有还原性 |
| C.一段时间后氢硫酸溶液中有淡黄色沉淀生成,说明SO2有氧化性 |
| D.该装置能体现实验的微型化和绿色化 |
您最近一年使用:0次
名校
解题方法
5 . 部分短周期主族元素的原子半径和主要化合价的关系如图所示,其中E、G、T位于同一周期。回答下列问题:

(1)B位于第_______ 周期第______ 族。
(2)FDB的电子式为_______ ;T的原子结构示意图为_______ 。
(3)设计简单实验证明D的非金属性比C的强:________ 。
(4)A和D的简单氢化物相遇产生“白烟”,其生成物的化学式是_______ 。
(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式,下同),碱性最强的是_______ ;上述非金属元素的简单氢化物中,沸点最高的是_______ ,还原性最强的是_______ 。
(6)G、D的最高价氧化物对应的水化物之间发生反应的化学方程式为_______ 。

(1)B位于第
(2)FDB的电子式为
(3)设计简单实验证明D的非金属性比C的强:
(4)A和D的简单氢化物相遇产生“白烟”,其生成物的化学式是
(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是
(6)G、D的最高价氧化物对应的水化物之间发生反应的化学方程式为
您最近一年使用:0次
2023-10-27更新
|
175次组卷
|
2卷引用:新疆乌鲁木齐市实验学校2023-2024学年高一上学期1月期末化学试题
6 . 完成下列问题。
如图所示,某兴趣小组研究铜与浓硫酸的反应。___________ ,这一过程中浓硫酸体现___________ 。
(2)若试管②中盛放品红试液,可以验证的 性质是
性质是___________ 。
(3)若要验证 的还原性,试管②中应盛放
的还原性,试管②中应盛放 ___________ 溶液。
(4)试管③的作用是___________ 发生的离子反应方程式为___________ 。
(5)浓硫酸具有: 脱水性;
脱水性;  酸性;
酸性;  强氧化性;
强氧化性;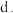 吸水性;下列各项分别表现浓硫酸的什么性质,请将字母填于空白处:
吸水性;下列各项分别表现浓硫酸的什么性质,请将字母填于空白处:
①盛有浓硫酸的烧杯敞口放置一段时间后,质量增加___________ 。
②浓硫酸与铜共热,浓硫酸表现的性质是___________ 。
③浓硫酸与红热木炭反应,浓硫酸表现的性质是___________ 。
④蔗糖中倒入浓硫酸,蔗糖变黑,体积膨胀,且有刺激性气味的气体产生,浓硫酸表现的性质是___________ 。
如图所示,某兴趣小组研究铜与浓硫酸的反应。

(2)若试管②中盛放品红试液,可以验证的
 性质是
性质是(3)若要验证
 的还原性,试管②中应盛放
的还原性,试管②中应盛放 (4)试管③的作用是
(5)浓硫酸具有:
 脱水性;
脱水性;  酸性;
酸性;  强氧化性;
强氧化性; 吸水性;下列各项分别表现浓硫酸的什么性质,请将字母填于空白处:
吸水性;下列各项分别表现浓硫酸的什么性质,请将字母填于空白处:①盛有浓硫酸的烧杯敞口放置一段时间后,质量增加
②浓硫酸与铜共热,浓硫酸表现的性质是
③浓硫酸与红热木炭反应,浓硫酸表现的性质是
④蔗糖中倒入浓硫酸,蔗糖变黑,体积膨胀,且有刺激性气味的气体产生,浓硫酸表现的性质是
您最近一年使用:0次
名校
解题方法
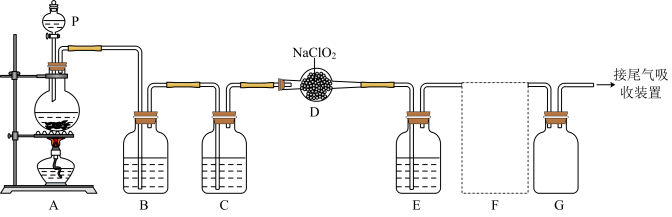
7 . ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2,成为自来水的消毒剂。已知ClO2是一种易溶于水的气体,实验室制备ClO2的原理是用亚氯酸钠固体与氯气反应:2NaClO2+Cl2=2C1O2+2NaCl,下图是实验室用于制备和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品已省略),其中E用于除去ClO2中的未反应的Cl2。___________ 。
(2)写出装置A中烧瓶内发生反应的离子方程式:___________ 。
(3)B装置中所盛试剂是___________ 。
(4)F为ClO2收集装置,应选用的装置是___________ (填序号),其中与E装置导管相连的导管口是___________ (填接口字母)。
①请写出该反应的化学方程式:___________ ,每消耗319.5gNaClO3,生成___________ L氯气(标况下)。(M(NaClO3)=106.5)。
②浓盐酸在该反应中表现出来的性质是___________ (填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)写出装置A中烧瓶内发生反应的离子方程式:
(3)B装置中所盛试剂是
(4)F为ClO2收集装置,应选用的装置是

①请写出该反应的化学方程式:
②浓盐酸在该反应中表现出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
您最近一年使用:0次
2024-02-02更新
|
148次组卷
|
3卷引用:新疆生产建设兵团第三师图木舒克市第二中学2023-2024学年高一下学期开学考试化学试题
名校
8 . 电子工业中,人们常用FeCl3溶液腐蚀附在绝缘板上的铜箔,制造印刷电路板。
(1)请用化学方程式表示制造印刷电路板的反应原理_________________ 。
为了从腐蚀废液中回收铜并重新获得FeCl3溶液,可采用以下步骤:
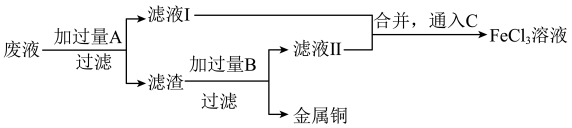
(2)写出回收铜并重新获得FeCl3溶液的过程中加入的有关物质的化学式:
A________ ,B________ ,C________ 。
(3)滤液Ⅰ中的阳离子既有氧化性又有还原性,判断的依据是_________________ 。为检验该金属阳离子,可设计的实验操作及实验现象为_________________ (可选择的试剂为“锌片”、KSCN溶液、“酸性H2O2”、“酸性KMnO4溶液”或“NaOH溶液”),且该过程发生的氧化还原反应离子方程式为_______________ 。
(4)上述步骤中,通入C发生反应的离子方程式为___________________ 。
(1)请用化学方程式表示制造印刷电路板的反应原理
为了从腐蚀废液中回收铜并重新获得FeCl3溶液,可采用以下步骤:

(2)写出回收铜并重新获得FeCl3溶液的过程中加入的有关物质的化学式:
A
(3)滤液Ⅰ中的阳离子既有氧化性又有还原性,判断的依据是
(4)上述步骤中,通入C发生反应的离子方程式为
您最近一年使用:0次
2024-01-09更新
|
67次组卷
|
2卷引用:新疆乌鲁木齐市实验学校2023-2024学年高一上学期1月期末化学试题
名校
解题方法
9 . 下列实验设计能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 酸性条件下,氧化性:H2O2>Fe3+ | 向 溶液中滴加用硫酸化的 溶液中滴加用硫酸化的 溶液,溶液变黄色 溶液,溶液变黄色 |
| B | 干燥的氯气没有漂白性 | 将一片鲜花花瓣放入盛有干燥氯气的集气瓶中 |
| C | 酸性:CH3COOH>HClO | 用pH试纸分别测定同浓度的CH3COOH溶液和HClO溶液的pH |
| D | 还原性:Fe2+>Br- | 将少量的氯水滴入FeBr2溶液中,再滴加CCl4振荡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-02更新
|
149次组卷
|
2卷引用:新疆乌鲁木齐市第十二中学2023-2024学年高三上学期1月月考化学试题
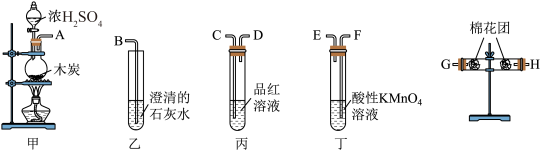
10 . 用如图所示的装置设计一个实验,验证浓硫酸与木炭粉在加热条件下反应产生的各种产物。___________ 。再此反应中硫酸显___________ 性。
如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):A接G,H接C,D接F,E接C,D接B。
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?乙中___________ ,第二次使用的丙中 ___________ ;
(3)丁中酸性KMnO4溶液的作用是___________ ;
(4)硫酸有很多的性质,将下列性质对应的字母填入各小题后面对应的横线上:
A.脱水性 B.酸性 C.强氧化性 D.吸水性
Ⅰ.在化学实验中,浓硫酸可干燥剂。___________ 。
Ⅱ.Cu与浓H2SO4反应,可生成CuSO4和SO2。___________ 。
Ⅲ.向滤纸上滴加浓H2SO4,滤纸变黑。___________ 。
Ⅳ.在冷浓H2SO4中放入铁片没明显现象。___________ 。
如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):A接G,H接C,D接F,E接C,D接B。
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?乙中
(3)丁中酸性KMnO4溶液的作用是
(4)硫酸有很多的性质,将下列性质对应的字母填入各小题后面对应的横线上:
A.脱水性 B.酸性 C.强氧化性 D.吸水性
Ⅰ.在化学实验中,浓硫酸可干燥剂。
Ⅱ.Cu与浓H2SO4反应,可生成CuSO4和SO2。
Ⅲ.向滤纸上滴加浓H2SO4,滤纸变黑。
Ⅳ.在冷浓H2SO4中放入铁片没明显现象。
您最近一年使用:0次



