江苏省南通市名校联盟2024届高三上学期12月学业质量联合监测化学试卷
江苏
高三
阶段练习
2024-01-01
938次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、物质结构与性质、化学实验基础、化学反应原理
江苏省南通市名校联盟2024届高三上学期12月学业质量联合监测化学试卷
江苏
高三
阶段练习
2024-01-01
938次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、物质结构与性质、化学实验基础、化学反应原理
一、单选题 添加题型下试题
单选题
|
较易(0.85)
解题方法
1. 材料科学是一门与工程技术密不可分的应用科学。下列有关相关物质的材料的说法,正确的一项是
| A.石墨烯和石墨炔都是新型的有机高分子材料 |
| B.太阳能电池板的核心材料是晶体硅,属于无机非金属材料 |
| C.“特氟龙”的主要成分聚四氟乙烯的单体属于烃类 |
| D.高压电线的制造主要使用金属铝而不使用铜的原因是铝的导电性更好且密度更低 |
您最近一年使用:0次
单选题
|
适中(0.65)
2. 利用反应 可制备水煤气,下列有关说法正确的是
可制备水煤气,下列有关说法正确的是
 可制备水煤气,下列有关说法正确的是
可制备水煤气,下列有关说法正确的是A. 是极性分子,因此在水中的溶解度较大 是极性分子,因此在水中的溶解度较大 |
B.一个 分子中只含有一个配位键 分子中只含有一个配位键 |
C. 的电子式为 的电子式为 |
D. 比较稳定的原因是可以形成分子间氢键 比较稳定的原因是可以形成分子间氢键 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
3. 2022年9月9日,国家航天局、国家原子能机构联合发布:我国科学家在嫦娥五号月壤样品中发现一种新矿物,命名为“嫦娥石”,英文名称为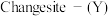 。嫦娥石是一种磷酸盐矿,属于陨磷钠镁钙石
。嫦娥石是一种磷酸盐矿,属于陨磷钠镁钙石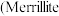 族。
族。 的理想组成为
的理想组成为 ,下列说法正确的是
,下列说法正确的是
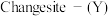 。嫦娥石是一种磷酸盐矿,属于陨磷钠镁钙石
。嫦娥石是一种磷酸盐矿,属于陨磷钠镁钙石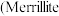 族。
族。 的理想组成为
的理想组成为 ,下列说法正确的是
,下列说法正确的是A.电负性大小: | B.第一电离能大小: |
C.碱性强弱: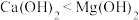 | D.半径大小: |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
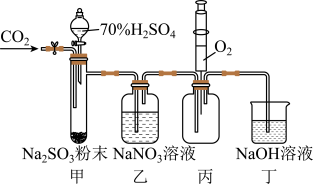
4. 实验室用如下图所示装置探究 与
与 溶液的反应(实验前先通入
溶液的反应(实验前先通入 排除装置中的空气)。下列说法不正确的是
排除装置中的空气)。下列说法不正确的是
 与
与 溶液的反应(实验前先通入
溶液的反应(实验前先通入 排除装置中的空气)。下列说法不正确的是
排除装置中的空气)。下列说法不正确的是
A.用装置甲产生 |
B.装置乙中无明显现象,则 与 与 未发生反应 未发生反应 |
C.装置丙中注入 ,产生红棕色气体,说明装置乙中 ,产生红棕色气体,说明装置乙中 发生了氧化反应 发生了氧化反应 |
| D.装置丁吸收尾气并防止空气进入装置丙 |
【知识点】 二氧化硫与其他强氧化剂的反应解读 物质性质的探究解读
您最近一年使用:0次
2023-03-23更新
|
1345次组卷
|
7卷引用:江苏省苏锡常镇四市2022-2023学年高三下学期教学情况调研(一)(3月)化学试题
单选题
|
适中(0.65)
5. 一种重要有机中间体的合成路线如下,下列说法中正确的是
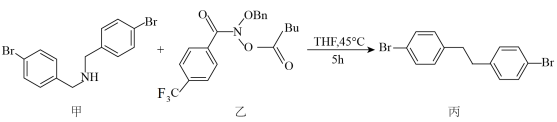

A.物质丙的分子式为 |
| B.物质甲可以发生氧化、取代、水解和消去反应 |
| C.图示反应类型为加成反应 |
| D.物质乙中的原子不可能处于同一平面 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 铁氰化钾(又名六氰合铁酸钾,化学式为 )和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为
)和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为 )是两种灵敏的可用于检验
)是两种灵敏的可用于检验 和
和 的物质:铁氰化钾可在酸性环境下被羟胺
的物质:铁氰化钾可在酸性环境下被羟胺 等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。下列对相关物质的说法,正确的一项是
等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。下列对相关物质的说法,正确的一项是
 )和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为
)和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为 )是两种灵敏的可用于检验
)是两种灵敏的可用于检验 和
和 的物质:铁氰化钾可在酸性环境下被羟胺
的物质:铁氰化钾可在酸性环境下被羟胺 等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。下列对相关物质的说法,正确的一项是
等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。下列对相关物质的说法,正确的一项是A. 的价层电子排布式为 的价层电子排布式为 |
B. 中含有离子键、共价键和配位键 中含有离子键、共价键和配位键 |
C.羟胺分子为平面结构,中心氧原子为 杂化 杂化 |
D.铁的两种常见离子 和 和 相比较, 相比较, 更稳定 更稳定 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
7. 高铁酸钾 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是| A.氢氧化铁胶体具有碱性,可用于净水 |
B. 具有氧化性,可作为特定环境中的抗氧化剂 具有氧化性,可作为特定环境中的抗氧化剂 |
| C.高铁酸钾能溶于水,水溶液呈紫色,可作氧化剂 |
| D.氧化铁呈红棕色且遮盖效果好,可用作红色颜料 |
您最近一年使用:0次
2023-12-31更新
|
251次组卷
|
2卷引用:江苏省南通市名校联盟2024届高三上学期12月学业质量联合监测化学试卷
单选题
|
适中(0.65)
解题方法
8. 高铁酸钾 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水;铁氰化钾(又名六氰合铁酸钾,化学式为
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水;铁氰化钾(又名六氰合铁酸钾,化学式为 )和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为
)和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为 )是两种灵敏的可用于检验
)是两种灵敏的可用于检验 和
和 的物质:铁氰化钾可在酸性环境下被羟胺
的物质:铁氰化钾可在酸性环境下被羟胺 等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。铁铵矾
等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。铁铵矾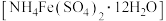 常用于制备高铁酸盐。下列反应的离子方程式正确的是
常用于制备高铁酸盐。下列反应的离子方程式正确的是
 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水;铁氰化钾(又名六氰合铁酸钾,化学式为
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水;铁氰化钾(又名六氰合铁酸钾,化学式为 )和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为
)和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为 )是两种灵敏的可用于检验
)是两种灵敏的可用于检验 和
和 的物质:铁氰化钾可在酸性环境下被羟胺
的物质:铁氰化钾可在酸性环境下被羟胺 等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。铁铵矾
等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。铁铵矾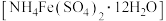 常用于制备高铁酸盐。下列反应的离子方程式正确的是
常用于制备高铁酸盐。下列反应的离子方程式正确的是A.羟胺还原铁氰化钾: |
B.在强碱溶液中,铁铵矾与次氯酸钠反应生成 : : |
C.抗坏血酸 还原铁氰化钾(含铁微粒产物与羟胺还原产物相同): 还原铁氰化钾(含铁微粒产物与羟胺还原产物相同): |
D.氯气氧化亚铁氰化钾: |
【知识点】 离子方程式的正误判断解读
您最近一年使用:0次
单选题
|
适中(0.65)
9. 氮及其化合物的转化具有重要应用。下列说法不正确的是
A.实验室探究稀硝酸与铜反应的气态产物: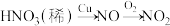 |
B.工业制硝酸过程中的物质转化: |
C.汽车尾气催化转化器中发生的主要反应: |
D.实验室制备少量 的原理: 的原理: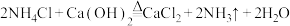 |
您最近一年使用:0次
2023-08-07更新
|
6812次组卷
|
13卷引用:2023年高考江苏卷化学真题
2023年高考江苏卷化学真题(已下线)选择题6-10黑龙江省鹤岗市第一中学2023-2024学年高二上学期开学考试化学试题江苏省建湖高级中学2023-2024学年高三上学期暑期学情检测(一)化学试题江苏省南京市六校联合体2023-2024学年高二上学期期初调研测试化学试题江苏省镇江第一中学2023-2024学年高二上学期期中考试化学试题江苏省常州高级中学2023~2024 学年高二上学期10月阶段检测化学试题江苏省南通市名校联盟2024届高三上学期12月学业质量联合监测化学试卷江苏省马坝高级中学2023-2024学年高三上学期期中考试化学试卷(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)河南省濮阳市第一高级中学2023-2024学年高三上学期第三次质量检测化学试题2024届河北省实验中学高三年级上学期第一次月考化学试题黑龙江省哈尔滨市第九中学校2023-2024学年高一下学期期中学业阶段评价考试化学试卷
单选题
|
较难(0.4)
解题方法
10. 一种双阴极微生物燃料电池装置如图所示。该装置可以同时进行硝化和反硝化脱氮,下列叙述正确的是


A.电池工作时, 的迁移方向:左→右 的迁移方向:左→右 |
B.电池工作时,“缺氧阴极”电极附近的溶液 增大 增大 |
C.“好氧阴极”存在反应: |
D.“厌氧阳极”区质量减少 时,该电极输出电子 时,该电极输出电子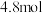 |
您最近一年使用:0次
单选题
|
适中(0.65)
11. 室温下,探究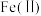 盐溶液的性质,下列实验方案能达到探究目的的是
盐溶液的性质,下列实验方案能达到探究目的的是
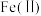 盐溶液的性质,下列实验方案能达到探究目的的是
盐溶液的性质,下列实验方案能达到探究目的的是| 选项 | 探究目的 | 实验方案 |
| A | 溶液中是否含有 | 向 溶液中滴加硝酸酸化后再滴加几滴 溶液中滴加硝酸酸化后再滴加几滴 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 |
| B |  是否有还原性 是否有还原性 | 向 浓溶液中加入酸性 浓溶液中加入酸性 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 |
| C |  是否水解 是否水解 | 向 溶液中滴加 溶液中滴加 滴紫色石蕊试液,观察溶液颜色变化 滴紫色石蕊试液,观察溶液颜色变化 |
| D |  能否催化 能否催化 分解 分解 | 向 溶液中滴加几滴 溶液中滴加几滴 溶液,观察气泡产生情况 溶液,观察气泡产生情况 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
12. H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+c(HC2O )+c(C2O
)+c(C2O )=0.100mol•L﹣1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是
)=0.100mol•L﹣1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是
 )+c(C2O
)+c(C2O )=0.100mol•L﹣1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是
)=0.100mol•L﹣1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是
A.pH=2.5的溶液中:c(H2C2O4)+c(C2O )>c(HC2O )>c(HC2O ) ) |
B.c(Na+)=0.100 mol•L﹣1的溶液中:c(H+)+c(H2C2O4)=c(OH﹣)+c(C2O ) ) |
C.c(HC2O )=c(C2O )=c(C2O )的溶液中:c(Na+)>0.100 mol•L﹣1+c(HC2O )的溶液中:c(Na+)>0.100 mol•L﹣1+c(HC2O ) ) |
D.pH=7的溶液中:c(Na+)< 2c(C2O ) ) |
您最近一年使用:0次
2020-12-10更新
|
484次组卷
|
7卷引用:陕西省咸阳市秦都区咸阳市实验中学2020-2021学年高二上学期第三次月考化学试题
单选题
|
适中(0.65)
解题方法
13. 二氧化碳的资源化利用对实现“双碳”有着重要意义。二氧化碳加氢制甲烷过程中的主要反应为

在密闭容器中, 、
、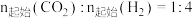 时,
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如题图所示。
实际转化率随温度的变化如题图所示。 的选择性可表示为
的选择性可表示为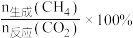 。下列说法正确的是
。下列说法正确的是



在密闭容器中,
 、
、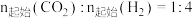 时,
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如题图所示。
实际转化率随温度的变化如题图所示。 的选择性可表示为
的选择性可表示为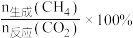 。下列说法正确的是
。下列说法正确的是
A.反应 |
B. 的选择性一定随着温度的升高而增加 的选择性一定随着温度的升高而增加 |
C.用该催化剂催化二氧化碳反应的最佳温度约为 的原因是此温度下 的原因是此温度下 的平衡转化率接近100% 的平衡转化率接近100% |
D. 时,提高 时,提高 的值或增大压强,均能使 的值或增大压强,均能使 平衡转化率达到X点的值 平衡转化率达到X点的值 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
解题方法
14. 金属铜已与人类相伴走过了千年岁月。铜的化合物性质之丰富、种类之多样、应用之广泛一直吸引着人们的目光。
(1)铜与浓硫酸的反应存在多个副反应。将光亮的铜片投入足量浓硫酸并加热,观察到有灰白色沉淀生成。发现该沉淀是Cu2S与另一种盐的混合物。已知反应过程中无气体生成,且亚硫酸铜在浓硫酸环境中极不稳定。请根据以上信息,写出该过程中发生反应的化学方程式:___________ 。
(2)铜能形成多种配合物。一价铜可与Cl-、NH3∙H2O等反应生成稳定性不一的配合物,在化工生产中有广泛应用。
①[Cu(NH3)2]+还原性较强,暴露在空气中可被迅速氧化为深蓝色的[Cu(NH3)4]2+,试写出反应的离子方程式:___________ ;并合理推测[Cu(NH3)2]+的这一性质在气体净化中的一种可能的应用:___________ 。
②CuCl在实验室中的少量制取,通常是在热浓盐酸中用Cu还原CuCl2,反应过程中会生成多种配合物,请写出可能生成的配离子的化学式:___________ (写出2种即可)。
(3)与铜同族的金(Au)性质不活泼,工业提金常利用氰化法。请你设计以金铁共生矿为原料提取金的实验方案:___________ 。
已知:①氰化物有剧毒,易被氧化为无毒的两种气体;
②氰化法发生的主要反应为: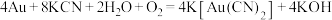 ,金可用Zn还原K[Au(CN)2]得到;
,金可用Zn还原K[Au(CN)2]得到;
③实验中可选用的试剂:KCN溶液,稀硫酸,锌粉,H2O2溶液,BaCl2溶液
④金铁共生矿中的其他杂质不与可选试剂反应
(1)铜与浓硫酸的反应存在多个副反应。将光亮的铜片投入足量浓硫酸并加热,观察到有灰白色沉淀生成。发现该沉淀是Cu2S与另一种盐的混合物。已知反应过程中无气体生成,且亚硫酸铜在浓硫酸环境中极不稳定。请根据以上信息,写出该过程中发生反应的化学方程式:
(2)铜能形成多种配合物。一价铜可与Cl-、NH3∙H2O等反应生成稳定性不一的配合物,在化工生产中有广泛应用。
①[Cu(NH3)2]+还原性较强,暴露在空气中可被迅速氧化为深蓝色的[Cu(NH3)4]2+,试写出反应的离子方程式:
②CuCl在实验室中的少量制取,通常是在热浓盐酸中用Cu还原CuCl2,反应过程中会生成多种配合物,请写出可能生成的配离子的化学式:
(3)与铜同族的金(Au)性质不活泼,工业提金常利用氰化法。请你设计以金铁共生矿为原料提取金的实验方案:
已知:①氰化物有剧毒,易被氧化为无毒的两种气体;
②氰化法发生的主要反应为:
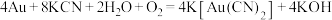 ,金可用Zn还原K[Au(CN)2]得到;
,金可用Zn还原K[Au(CN)2]得到;③实验中可选用的试剂:KCN溶液,稀硫酸,锌粉,H2O2溶液,BaCl2溶液
④金铁共生矿中的其他杂质不与可选试剂反应
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
名校
15. 化合物G是合成镇静剂“利血平”的一个重要的中间体,可以由以下步骤合成。

(1)物质E中的 杂化的碳原子与
杂化的碳原子与 杂化的碳原子的比值为:
杂化的碳原子的比值为:___________ 。
(2)写出A与B反应生成C的反应类型:___________ 。
(3)D→E反应中会生成一个二溴代物的中间体,写出该化合物的结构简式:___________ 。
(4)D的一种同分异构体具有以下性质:
i.化合物中有3种不同化学环境的H原子
ii.该化合物能与 的
的 反应
反应
写出该化合物的结构简式:___________ 。
(5)结合题干信息,写出以乙烯和环戊二烯( )为原料制备产率较高的
)为原料制备产率较高的 的合成路线图
的合成路线图___________ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。

(1)物质E中的
 杂化的碳原子与
杂化的碳原子与 杂化的碳原子的比值为:
杂化的碳原子的比值为:(2)写出A与B反应生成C的反应类型:
(3)D→E反应中会生成一个二溴代物的中间体,写出该化合物的结构简式:
(4)D的一种同分异构体具有以下性质:
i.化合物中有3种不同化学环境的H原子
ii.该化合物能与
 的
的 反应
反应写出该化合物的结构简式:
(5)结合题干信息,写出以乙烯和环戊二烯(
 )为原料制备产率较高的
)为原料制备产率较高的 的合成路线图
的合成路线图【知识点】 有机反应类型 根据要求书写同分异构体解读 有机物的推断
您最近一年使用:0次
2023-12-31更新
|
546次组卷
|
3卷引用:江苏省南通市名校联盟2024届高三上学期12月学业质量联合监测化学试卷
三、填空题 添加题型下试题
填空题
|
适中(0.65)
16. 阅读下面的材料:
2023年8月,日本政府不顾国际社会的强烈反对,公然将核污水排放入海。核污水中含有大量放射性核素,会对海洋生态造成不可挽回的伤害。日本政府排放核污水是一种严重不负责任的行为。排海开始后,也再次引发了人们对于核能安全性的思考。
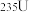 是核反应堆中应用广泛的核燃料,也是铀的一种丰度较低的同位素。在自然界含量最高的铀同位素是
是核反应堆中应用广泛的核燃料,也是铀的一种丰度较低的同位素。在自然界含量最高的铀同位素是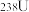 。纯净的铀呈银白色,质软,密度与金相近,化学性质活泼。
。纯净的铀呈银白色,质软,密度与金相近,化学性质活泼。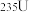 与
与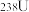 的分离较为困难。为了提取到
的分离较为困难。为了提取到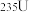 ,工业上利用
,工业上利用 和
和 蒸汽扩散速率的差别进行同位素分离。
蒸汽扩散速率的差别进行同位素分离。 在水中发生强烈水解,不能储存在玻璃器皿中。
在水中发生强烈水解,不能储存在玻璃器皿中。
回答下列问题:
(1) 在
在 溶液中也会发生强烈水解,生成一种黄色化合物重铀酸钠(其结构与重铬酸钾
溶液中也会发生强烈水解,生成一种黄色化合物重铀酸钠(其结构与重铬酸钾 相似),写出反应的化学方程式:
相似),写出反应的化学方程式:___________ 。
(2) 不能储存在玻璃器皿中的原因是:
不能储存在玻璃器皿中的原因是:___________ 。
(3)铀的 价化合物还有
价化合物还有 ,其溶于
,其溶于 生成一种含6个结晶水的黄绿色、发出荧光的固体A.将
生成一种含6个结晶水的黄绿色、发出荧光的固体A.将 加热至
加热至 时分解产生
时分解产生 和
和 ,试通过计算给出A的化学式
,试通过计算给出A的化学式___________ ,写出 溶于
溶于 的化学方程式
的化学方程式___________ 。
(4)通常盐类化合物的溶解度受到阴阳离子大小的影响:离子半径相差越大,溶解度一般也越大。已知重铀酸铵难溶于水,且钾盐铵盐的溶解度相似,根据以上信息并结合所学,推测重铀酸钠的溶解度___________ (选填“大于”或“小于”)重铀酸铵,并简要说明理由:___________ 。
2023年8月,日本政府不顾国际社会的强烈反对,公然将核污水排放入海。核污水中含有大量放射性核素,会对海洋生态造成不可挽回的伤害。日本政府排放核污水是一种严重不负责任的行为。排海开始后,也再次引发了人们对于核能安全性的思考。
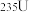 是核反应堆中应用广泛的核燃料,也是铀的一种丰度较低的同位素。在自然界含量最高的铀同位素是
是核反应堆中应用广泛的核燃料,也是铀的一种丰度较低的同位素。在自然界含量最高的铀同位素是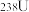 。纯净的铀呈银白色,质软,密度与金相近,化学性质活泼。
。纯净的铀呈银白色,质软,密度与金相近,化学性质活泼。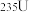 与
与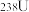 的分离较为困难。为了提取到
的分离较为困难。为了提取到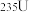 ,工业上利用
,工业上利用 和
和 蒸汽扩散速率的差别进行同位素分离。
蒸汽扩散速率的差别进行同位素分离。 在水中发生强烈水解,不能储存在玻璃器皿中。
在水中发生强烈水解,不能储存在玻璃器皿中。回答下列问题:
(1)
 在
在 溶液中也会发生强烈水解,生成一种黄色化合物重铀酸钠(其结构与重铬酸钾
溶液中也会发生强烈水解,生成一种黄色化合物重铀酸钠(其结构与重铬酸钾 相似),写出反应的化学方程式:
相似),写出反应的化学方程式:(2)
 不能储存在玻璃器皿中的原因是:
不能储存在玻璃器皿中的原因是:(3)铀的
 价化合物还有
价化合物还有 ,其溶于
,其溶于 生成一种含6个结晶水的黄绿色、发出荧光的固体A.将
生成一种含6个结晶水的黄绿色、发出荧光的固体A.将 加热至
加热至 时分解产生
时分解产生 和
和 ,试通过计算给出A的化学式
,试通过计算给出A的化学式 溶于
溶于 的化学方程式
的化学方程式(4)通常盐类化合物的溶解度受到阴阳离子大小的影响:离子半径相差越大,溶解度一般也越大。已知重铀酸铵难溶于水,且钾盐铵盐的溶解度相似,根据以上信息并结合所学,推测重铀酸钠的溶解度
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-原理综合题
|
较难(0.4)
名校
17. 捕集并转化 可以有效实现碳达峰、碳中和。
可以有效实现碳达峰、碳中和。
Ⅰ.工业上利用两种温室气体 和
和 催化重整制取
催化重整制取 和CO,主要反应为
和CO,主要反应为
反应①:
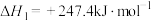
过程中还发生三个副反应:
反应②:

反应③: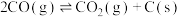
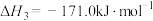
反应④: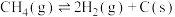

将 与
与 (体积比为1∶1)的混合气体以一定流速通过催化剂,产物中
(体积比为1∶1)的混合气体以一定流速通过催化剂,产物中 与CO的物质的量之比、
与CO的物质的量之比、 的转化率与温度的关系如图所示:
的转化率与温度的关系如图所示:

(1)
___________ 。
(2)500℃时, 比较小,此时发生的副反应以
比较小,此时发生的副反应以___________ (选填②、③、④中一种)为主。升高温度,产物中 与CO的物质的量之比增大的原因是
与CO的物质的量之比增大的原因是___________ 。
Ⅱ.光催化 和
和 生成CO和
生成CO和 催化反应机理如图所示:
催化反应机理如图所示:

(3)上述反应机理中表现出氧化性的粒子有___________ 。
Ⅲ.用光电化学法将 还原为有机物实现碳资源的再生利用,其装置如左图所示,其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如右图所示:
还原为有机物实现碳资源的再生利用,其装置如左图所示,其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如右图所示:
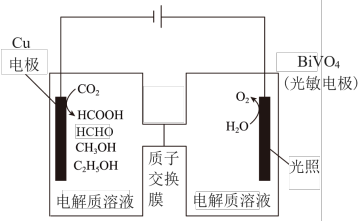

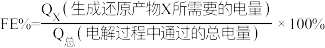 ,其中,
,其中, ,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
(4)当电解电压为U1V时,阴极生成HCHO的电极反应式为___________ 。
(5)当电解电压为U2V时,电解生成的HCOOH和HCHO的物质的量之比为3:2,则生成HCHO的法拉第效率m为___________ 。
 可以有效实现碳达峰、碳中和。
可以有效实现碳达峰、碳中和。Ⅰ.工业上利用两种温室气体
 和
和 催化重整制取
催化重整制取 和CO,主要反应为
和CO,主要反应为反应①:

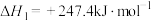
过程中还发生三个副反应:
反应②:


反应③:
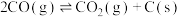
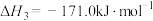
反应④:
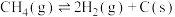

将
 与
与 (体积比为1∶1)的混合气体以一定流速通过催化剂,产物中
(体积比为1∶1)的混合气体以一定流速通过催化剂,产物中 与CO的物质的量之比、
与CO的物质的量之比、 的转化率与温度的关系如图所示:
的转化率与温度的关系如图所示:
(1)

(2)500℃时,
 比较小,此时发生的副反应以
比较小,此时发生的副反应以 与CO的物质的量之比增大的原因是
与CO的物质的量之比增大的原因是Ⅱ.光催化
 和
和 生成CO和
生成CO和 催化反应机理如图所示:
催化反应机理如图所示:
(3)上述反应机理中表现出氧化性的粒子有
Ⅲ.用光电化学法将
 还原为有机物实现碳资源的再生利用,其装置如左图所示,其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如右图所示:
还原为有机物实现碳资源的再生利用,其装置如左图所示,其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如右图所示:

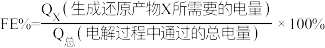 ,其中,
,其中, ,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。(4)当电解电压为U1V时,阴极生成HCHO的电极反应式为
(5)当电解电压为U2V时,电解生成的HCOOH和HCHO的物质的量之比为3:2,则生成HCHO的法拉第效率m为
您最近一年使用:0次
2023-11-20更新
|
680次组卷
|
5卷引用:江苏省南通市海安市2023-2024学年高三上学期11月期中化学试题
江苏省南通市海安市2023-2024学年高三上学期11月期中化学试题(已下线)江苏省南通市海安高级中学2023-2024学年高三上学期期中考试化学试题江苏省南京市金陵中学2023-2024学年高三上学期期中学业质量监测 化学试卷江苏省南通市名校联盟2024届高三上学期12月学业质量联合监测化学试卷江苏省苏州大学附属中学2023-2024学年高二上学期12月月考化学试题
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、物质结构与性质、化学实验基础、化学反应原理
试卷题型(共 17题)
题型
数量
单选题
13
解答题
3
填空题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 硅的物理性质与用途 加聚物的单体、链节及聚合度的确定 化学科学对人类文明发展的意义 新型无机非金属材料 | |
| 2 | 0.65 | 共价化合物的结构及形成过程 简单配合物的成键 极性分子和非极性分子 氢键对物质性质的影响 | |
| 3 | 0.65 | 元素金属性与非金属性递变规律的理解及应用 微粒半径大小的比较方法 电离能变化规律 元素性质与电负性的关系 | |
| 4 | 0.85 | 二氧化硫与其他强氧化剂的反应 物质性质的探究 | |
| 5 | 0.65 | 有机反应类型 根据元素种类、原子个数、有机物类别确定分子式 有机分子中原子共面的判断 卤代烃的消去反应 | |
| 6 | 0.65 | 电子排布式 利用杂化轨道理论判断分子的空间构型 简单配合物的成键 | |
| 7 | 0.85 | 胶体的性质和应用 氧化还原反应在生活、生产中的应用 几种铁的氧化物的物理性质及用途 | |
| 8 | 0.65 | 离子方程式的正误判断 | |
| 9 | 0.65 | 氨气的实验室制法 一氧化氮的化学性质 硝酸的强氧化性 | |
| 10 | 0.4 | 新型电池 | |
| 11 | 0.65 | Fe2+的还原性 Fe3+的检验 盐类水解规律理解及应用 化学实验方案的设计与评价 | |
| 12 | 0.65 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 13 | 0.65 | 盖斯定律与热化学方程式 化学平衡的移动及其影响因素 与转化率变化有关图像的分析 | |
| 二、解答题 | |||
| 14 | 0.65 | 浓硫酸的强氧化性 配合物的结构与性质 配合物的应用 综合实验设计与评价 | 实验探究题 |
| 15 | 0.65 | 有机反应类型 根据要求书写同分异构体 有机物的推断 | 有机推断题 |
| 17 | 0.4 | 盖斯定律及其有关计算 化学平衡的移动及其影响因素 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |
| 三、填空题 | |||
| 16 | 0.65 | 硝酸盐的不稳定性 二氧化硅的化学性质 微粒半径大小的比较方法 元素、核素、同位素 | |



