解题方法
1 . 反应A(g)+3B(s) 2C(g)+2D(g),用不同物质表示的反应速率分别如下,其中反应速率最大的是
2C(g)+2D(g),用不同物质表示的反应速率分别如下,其中反应速率最大的是
 2C(g)+2D(g),用不同物质表示的反应速率分别如下,其中反应速率最大的是
2C(g)+2D(g),用不同物质表示的反应速率分别如下,其中反应速率最大的是| A.v(C)=0.04mol·L-1·s-1 | B.v(A)=0.06mol·L-1·min-1 |
| C.v(A)=0.05mol·L-1·s-1 | D.v(D)=0.01mol·L-1·s-1 |
您最近一年使用:0次
解题方法
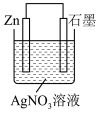
2 . 某兴趣小组为研究原电池原理,设计下图装置。___________ 极(填“正”或“负”),发生___________ 反应(填“氧化”或“还原”),电子的流向___________ ,其电极反应式是___________ ;
(2)溶液中NO 移向
移向___________ (填“Cu”或“Zn”极)。当负极金属溶解13.0g时,通过导线的电子数___________ 。
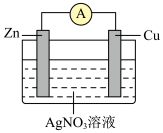
(2)溶液中NO
 移向
移向
您最近一年使用:0次
解题方法
3 . 如下图表示800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,下列结论错误的是
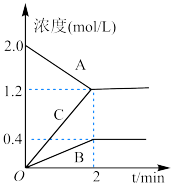
A.该反应的化学方程式是2A B+3C B+3C |
| B.v(A):v(B)=2:1 |
| C.2min时该反应在此条件下达到了最大的限度 |
| D.2min内用A物质表示化学反应速率为0.4mol·L-1·s-1 |
您最近一年使用:0次
解题方法
4 . 反应O2(g)+2SO2(g) 2SO3(g)△H<0,若在恒容密闭容器中发生,下列选项表明该反应一定已达平衡状态的是
2SO3(g)△H<0,若在恒容密闭容器中发生,下列选项表明该反应一定已达平衡状态的是
 2SO3(g)△H<0,若在恒容密闭容器中发生,下列选项表明该反应一定已达平衡状态的是
2SO3(g)△H<0,若在恒容密闭容器中发生,下列选项表明该反应一定已达平衡状态的是| A.容器内气体的密度不再变化 | B.容器内气体的反应速率v正(O2)=2v逆(SO2) |
| C.反应消耗1molO2同时生成2molSO2 | D.容器内气体的浓度c(O2):c(SO2):c(SO3)=1:2:2 |
您最近一年使用:0次
解题方法
5 . 汽车的启动电源常用铅蓄电池,其放电时的原电池反应如下:PbO2+Pb+2H2SO4=2PbSO4+2H2O,根据此反应判断,下列叙述中正确的是
| A.Pb是正极 |
| B.PbO2得电子,被氧化 |
C.负极反应是Pb+ -2e-=PbSO4 -2e-=PbSO4 |
| D.电池放电时,溶液的酸性增强 |
您最近一年使用:0次
解题方法
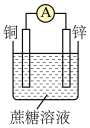
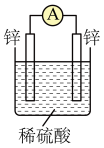
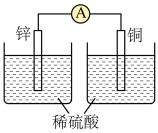
6 . 某化学兴趣小组为了探索电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
(1)实验1和实验2中铝电极的作用是否相同?___________
(2)实验3的总反应方程式为___________ ;
(3)实验4中铝作___________ 极(填“负”或“正”);此电极的反应方程式为___________ ;总反应方程式为___________ 。
| 实验编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 指向铝 |
| 2 | Al、Cu | 稀盐酸 | 偏向铜 |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向镁 |
(2)实验3的总反应方程式为
(3)实验4中铝作
您最近一年使用:0次
解题方法
7 . 化学反应的快慢和限度对人类生产生活有重要的影响。800℃时,A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,回答下列问题:_______ 。
(2)2min内,C的反应速率为_______ 。
(3)该反应的化学方程式为_______ 。
(4)在其他条件下,测得A的反应速率为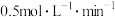 ,此时的反应速率与800℃时相比
,此时的反应速率与800℃时相比_______ 。
A.比800℃时慢 B.比800℃时快 C.和800℃时速率一样
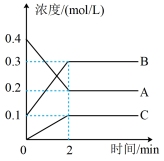
(2)2min内,C的反应速率为
(3)该反应的化学方程式为
(4)在其他条件下,测得A的反应速率为
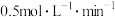 ,此时的反应速率与800℃时相比
,此时的反应速率与800℃时相比A.比800℃时慢 B.比800℃时快 C.和800℃时速率一样
您最近一年使用:0次
8 . 按照要求填空
(1)写出乙醇在空气中燃烧的方程式:_______ 。
(2)写出用乙酸除去水壶中水垢的方程式:_______ 。
(3)写出乙烯和氯气发生加成反应的方程式:_______ 。
(4)写出乙醇催化氧化成乙醛的方程式_______ 。
(1)写出乙醇在空气中燃烧的方程式:
(2)写出用乙酸除去水壶中水垢的方程式:
(3)写出乙烯和氯气发生加成反应的方程式:
(4)写出乙醇催化氧化成乙醛的方程式
您最近一年使用:0次
9 . 可逆反应SO2+O2 2SO3,在混合气体中充入定量的18O2,足够长的时间后18O
2SO3,在混合气体中充入定量的18O2,足够长的时间后18O
 2SO3,在混合气体中充入定量的18O2,足够长的时间后18O
2SO3,在混合气体中充入定量的18O2,足够长的时间后18O| A.只存在于O2中 | B.只存在于O2和SO3 |
| C.只存在于O2和SO3 | D.存在于O2、SO2和SO3 |
您最近一年使用:0次