1 . 下列化学用语正确的是
A.乙烯的球棍模型: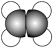 |
B.羟基的电子式为: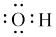 |
| C.1,3-丁二烯的分子式:C4H6 |
D.聚丙烯的结构简式: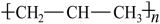 |
您最近一年使用:0次
2 . 羟甲香豆素(丙)是一种治疗胆结石的药物,部分合成路线如图所示。下列说法不正确的是
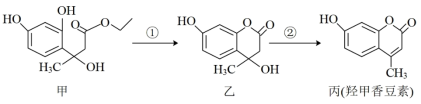
| A.甲分子中的含氧官能团为羟基、酯基 |
| B.丙能使酸性高锰酸钾溶液褪色 |
| C.该有机物遇FeCl3溶液发生显色反应 |
| D.1mol丙与足量溴水反应时,消耗Br2的物质的量为4mol |
您最近一年使用:0次
解题方法
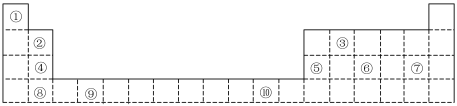
3 . 下表为元素周期表的一部分,其中的编号对应的元素。
(1)表中有___________ 种金属元素,其中属于ds区元素的是___________ (填元素符号)。
(2)表中元素⑥原子的最外电子层上未成对电子数为___________ 个。
(3)元素④的第一电离能___________ 元素⑤的第一电离能(填“>”“=”或“<”,下同);元素⑥的电负性___________ 元素⑦的电负性;元素⑦的简单离子的半径___________ 元素⑧的简单离子的半径。
(4)⑨号元素在周期表种的位置___________ ,位于___________ 区。元素周期表写出元素⑨的价层电子排布式___________ 。
(5)根据对角线规则,②与⑤的氧化物、氢氧化物的性质相似。写出少量②的最高价氧化物与氢氧化钠的水溶液反应所生成的盐的化学式___________ 。
(1)表中有
(2)表中元素⑥原子的最外电子层上未成对电子数为
(3)元素④的第一电离能
(4)⑨号元素在周期表种的位置
(5)根据对角线规则,②与⑤的氧化物、氢氧化物的性质相似。写出少量②的最高价氧化物与氢氧化钠的水溶液反应所生成的盐的化学式
您最近一年使用:0次
解题方法
4 . 前四周期元素X、Y、Z、W、R的原子序数依次增大。X基态原子有3个轨道、且每个轨道上的电子数相同,Y的简单气态氢化物的水溶液呈碱性,Z是地壳中含量最多的元素,W原子是第三周期中原子半径最大的元素,R是第四周期中未成对电子数最多的元素。下列说法正确的是
| A.原子半径:r(R)>r(W)>r(Z)>r(Y)>r(X) |
| B.第一电离能: I(X)<I(Y)<I(Z) |
| C.Y最简单的气态氢化物中,Y原子的杂化方式为sp3杂化 |
D.基态R原子价层电子的轨道表示式: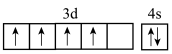 |
您最近一年使用:0次
5 . 下列图像表述的现象与电子的跃迁无关的是
|
|
| A.平面镜成像 | B.霓虹灯广告 |
|
|
| C.蜡烛燃烧 | D.燃放焰火 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 回答下列问题。
(1)利用VSEPR模型推断分子或离子的立体构型。
CS2___________ ;AlBr3(共价分子)___________ 。
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:
平面形分子___________ ,三角锥形分子___________ ,四面体形分子___________ 。
(1)利用VSEPR模型推断分子或离子的立体构型。
CS2
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:

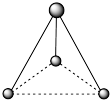
平面形分子
您最近一年使用:0次
解题方法
7 . 以下是一些原子的2p能级和3d能级中电子排布的情况。其中违反了洪特规则的是
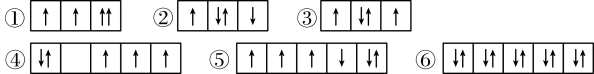
| A.① | B.①③ | C.②④⑤ | D.③④⑤ |
您最近一年使用:0次
解题方法
8 . 根据已学知识,请你回答下列问题:
(1)含有8个质子,10个中子的原子的化学符号___________ 。
(2)最外层电子排布为4s24p1的原子的核电荷数为___________ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4,该元素的名称是___________ 。
(4)根据VSEPR模型,H3O+的分子立体结构为:___________ 。
(5)周期表中最活泼的非金属元素原子的轨道表示式为___________ 。
(1)含有8个质子,10个中子的原子的化学符号
(2)最外层电子排布为4s24p1的原子的核电荷数为
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4,该元素的名称是
(4)根据VSEPR模型,H3O+的分子立体结构为:
(5)周期表中最活泼的非金属元素原子的轨道表示式为
您最近一年使用:0次
解题方法
9 . 按要求填空。
(1)基态铝原子核外电子共有___________ 种不同能级的电子,最高能级的电子云有___________ 种不同的伸展方向,有___________ 种不同运动状态的电子。
(2)S的基态原子核外有___________ 个未成对电子,Si的基态原子核外电子排布式为___________ 。基态Si原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________ ,电子数为___________ 。
(3)可正确表示原子轨道的是___________(填字母)。
(4)基态Fe原子有___________ 个未成对电子,Fe3+的电子排布式为___________ ;Cu+基态核外电子排布式为___________ 。
(5)某元素的原子最外层电子排布式为nsnnpn+2,则n=___________ ;原子中能量最高的是___________ 能级电子。
(6)第四周期中最外层仅有1个电子的所有基态原子的电子排布式为___________ ,第四周期中,3d轨道半充满的元素符号是___________ 。
(1)基态铝原子核外电子共有
(2)S的基态原子核外有
(3)可正确表示原子轨道的是___________(填字母)。
| A.2s | B.2d | C.3p | D.3f |
(5)某元素的原子最外层电子排布式为nsnnpn+2,则n=
(6)第四周期中最外层仅有1个电子的所有基态原子的电子排布式为
您最近一年使用:0次
解题方法
10 . 某元素基态原子最外层的电子排布式如下,其中能表示该元素一定为主族元素的是
| A.2s22p6 | B.ns1 | C.4s24p1 | D.4s1 |
您最近一年使用:0次