名校
1 . 南开大学研究团队证实在高压条件下He可以与Na形成稳定的化合物 ,为高压化学和物质在极端条件下的行为提供了新的见解。下列说法正确的是
,为高压化学和物质在极端条件下的行为提供了新的见解。下列说法正确的是
 ,为高压化学和物质在极端条件下的行为提供了新的见解。下列说法正确的是
,为高压化学和物质在极端条件下的行为提供了新的见解。下列说法正确的是| A.He是第ⅡA族元素 | B.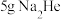 中电子的物质的量为 中电子的物质的量为 |
C.常温下Na被 氧化为淡黄色固体 氧化为淡黄色固体 | D.Na原子结构示意图为: |
您最近一年使用:0次
昨日更新
|
23次组卷
|
2卷引用:福建省三明市沙县区第一中学2023-2024学年高一下学期期中考试 化学试题
名校
2 . 下面叙述中,正确的是
| A.H2O分子比H2S分子稳定是因为前者分子间存在氢键 |
| B.各1mol的金刚石与SiO2中所含的共价键的数目相同 |
| C.共价晶体的原子间只存在共价键,而分子晶体内只存在范德华力 |
| D.熔点:SiC>NaCl>C60 |
您最近一年使用:0次
3 . 下列描述正确的是
A.在中性条件下可用KSCN溶液检验补铁剂中是否含有 |
| B.可用核磁共振法测定出青蒿素的相对分子质量 |
| C.液晶属于晶体的一种,可用于制造液晶显示器 |
D. 、石墨烯、碳纳米管都是碳的同素异形体,是纳米材料中的“明星” 、石墨烯、碳纳米管都是碳的同素异形体,是纳米材料中的“明星” |
您最近一年使用:0次
名校
4 . 对于物质的结构与性质描述中,前者大于后者的是
| 结构与性质 | 前者 | 后者 | |
| A | 熔点 | 碳化硅 | 晶体硅 |
| B | 沸点 |
|
|
| C | 分子的极性 |  |  |
| D | 在水中的溶解度 |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 工业上用 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。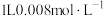 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。
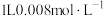 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
A.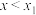 时, 时, 主要被氧化为 主要被氧化为 |
B.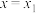 时,生成的 时,生成的 的物质的量为 的物质的量为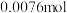 |
C.生成硝氮的离子方程式: |
D. 时,分批加入 时,分批加入 可以降低总氮残余率 可以降低总氮残余率 |
您最近一年使用:0次
名校
解题方法
6 . 石油醚通常是指由戊烷、己烷和环烷烃等物质的混合物,在化学、制药和工业领域中有着广泛的应用,某些成分的结构如图所示。下列叙述错误的是
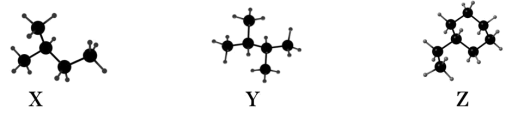
| A.化合物X和Y是同系物 | B.新戊烷与Y是同分异构体 |
| C.Z的一氯代物有6种 | D.X、Y、Z均不能使酸性 溶液褪色 溶液褪色 |
您最近一年使用:0次
名校
7 . 一种从海水中提取溴的工艺流程如图所示。下列叙述错误的是
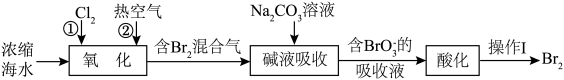
| A.“氧化”时,通入氯气前需要将海水酸化 |
B.吸收液中大量存在的离子为: 、 、 、 、 、 、 |
C.“酸化”时发生反应的离子方程式: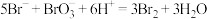 |
D. 极易挥发,所以操作Ⅰ为蒸馏 极易挥发,所以操作Ⅰ为蒸馏 |
您最近一年使用:0次
名校
解题方法
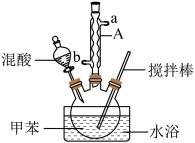
8 . 某同学设计如图所示装置制备一硝基甲苯。
③甲苯的密度0.866g/ml,沸点110.6℃,硝基苯的密度1.20g/ml,沸点210.9℃。
实验步骤如下:
①配制浓硫酸和浓硝酸(按体积比1:3)的混合物(混酸)
②在三颈瓶里装15ml甲苯
③装好其它药品,并组装好仪器
④向三颈烧瓶中加入混酸,并不断搅拌
⑤控制温度,大约反应10min至三颈烧瓶底有大量液体(淡黄色油状)出现
⑥分离出一硝基甲苯。
请回答下列问题:
(1)本实验的关键是控制温度在30℃左右,如果温度过高,产生的后果是_______ 。
(2)仪器A的名称_______ ,浓硫酸的作用_______ ;
(3)三颈烧瓶中甲苯与混酸反应生成间硝基甲苯的化学方程式_______ 。
(4)分离产品方案如下图所示_______ 、______ 。
②操作2的名称是_______ 。
A.过滤 B.蒸馏 C.重结晶 D.萃取
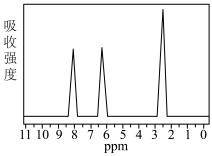
(5)经测定,产品1为一硝基甲苯,其中一种的核磁共振氢谱如图所示,该有机物的结构简式为___ 。
已知:①一硝基甲苯可能的结构简式为 、
、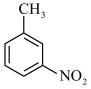 、
、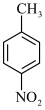 。
。
③甲苯的密度0.866g/ml,沸点110.6℃,硝基苯的密度1.20g/ml,沸点210.9℃。
实验步骤如下:
①配制浓硫酸和浓硝酸(按体积比1:3)的混合物(混酸)
②在三颈瓶里装15ml甲苯
③装好其它药品,并组装好仪器
④向三颈烧瓶中加入混酸,并不断搅拌
⑤控制温度,大约反应10min至三颈烧瓶底有大量液体(淡黄色油状)出现
⑥分离出一硝基甲苯。
请回答下列问题:
(1)本实验的关键是控制温度在30℃左右,如果温度过高,产生的后果是
(2)仪器A的名称
(3)三颈烧瓶中甲苯与混酸反应生成间硝基甲苯的化学方程式
(4)分离产品方案如下图所示

②操作2的名称是
A.过滤 B.蒸馏 C.重结晶 D.萃取
(5)经测定,产品1为一硝基甲苯,其中一种的核磁共振氢谱如图所示,该有机物的结构简式为
您最近一年使用:0次
名校
解题方法
9 . 用磷铁渣(含Fe、FeP、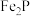 及少量杂质)制备磷酸铁晶体(
及少量杂质)制备磷酸铁晶体( )的工艺流程如下:
)的工艺流程如下:___________ 。
(2)“浸取”时,硝酸浓度过高会较多分解,化学方程式是___________ 。
(3)废气中含有 、NO,直接排放产生的危害主要有
、NO,直接排放产生的危害主要有___________ (写出两项),加入活性炭的目的是吸附氮氧化物;若用NaOH溶液吸收,物质的量比为 的
的 、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为
、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为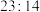 ,其化学式是
,其化学式是___________ 。
(4)若HNO₃的还原产物为NO,与1molFe2P完全反应而生成的NO有___________ mol。
(5)实验室完成操作X中用到的玻璃仪器有:烧杯、___________ 。
(6)“调pH”时,碱性过高产物中含铁量会增大,其原因有可能为___________ 。
(7)最终产品应洗涤,检验是否洗净的试剂是___________ 。
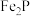 及少量杂质)制备磷酸铁晶体(
及少量杂质)制备磷酸铁晶体( )的工艺流程如下:
)的工艺流程如下:
(2)“浸取”时,硝酸浓度过高会较多分解,化学方程式是
(3)废气中含有
 、NO,直接排放产生的危害主要有
、NO,直接排放产生的危害主要有 的
的 、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为
、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为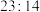 ,其化学式是
,其化学式是(4)若HNO₃的还原产物为NO,与1molFe2P完全反应而生成的NO有
(5)实验室完成操作X中用到的玻璃仪器有:烧杯、
(6)“调pH”时,碱性过高产物中含铁量会增大,其原因有可能为
(7)最终产品应洗涤,检验是否洗净的试剂是
您最近一年使用:0次
名校
解题方法
10 . 物质结构的知识被科学家应用于各个科学领域,如医药、材料、染料等,造福着人类。下列说法不正确的是
| A.微波炉的工作原理是微波对食物中的极性分子产生作用 |
| B.石墨的导电性具有一定的方向性 |
| C.DNA的双螺旋结构靠大量氢键相连而稳定存在于生命体中 |
D.铁血红素分子中都以 与原卟啉环形成配合物的形式存在 与原卟啉环形成配合物的形式存在 |
您最近一年使用:0次