名校
1 . 我国科学家将聚酰亚胺(组成元素为H、C、N、O等)介电聚合物与高绝缘纳米氧化镁(MgO)填料混合,成功制得聚酰亚胺/纳米氧化镁复合材料。该复合材料特点为具有高击穿强度、宽温度范围和低介电损耗。结合所学知识,回答下列问题。
(1)基态Mg原子的电子排布式为_________ 。
(2)C、N、O第一电离能由大到小的顺序为_________ ;C、N、O电负性由大到小的顺序为_________ ,理由是________________ 。
(3) 三种分子的空间结构和相应的键角如图1所示。
三种分子的空间结构和相应的键角如图1所示。 中O的未成对电子所在原子轨道的形状为
中O的未成对电子所在原子轨道的形状为_________ ; 的沸点比
的沸点比 的高,其主要原因是
的高,其主要原因是__________ ; 的键角大于
的键角大于 的键角,其原因是
的键角,其原因是________ 。
(1)基态Mg原子的电子排布式为
(2)C、N、O第一电离能由大到小的顺序为
(3)
 三种分子的空间结构和相应的键角如图1所示。
三种分子的空间结构和相应的键角如图1所示。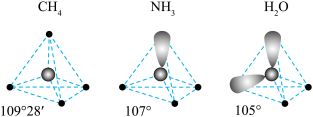
 中O的未成对电子所在原子轨道的形状为
中O的未成对电子所在原子轨道的形状为 的沸点比
的沸点比 的高,其主要原因是
的高,其主要原因是 的键角大于
的键角大于 的键角,其原因是
的键角,其原因是
您最近一年使用:0次
名校
2 . 回答下列问题
(1)利用 与
与 反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
________ (填“大于”“小于”或“等于”) 。
。
②碳化硅晶体中每个Si原子周围距离最近的C原子数目为________ 。
③碳化硅的晶胞参数为a pm,晶胞密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
_______ (用含a和ρ的计算式表示)
④碳化硅的硬度_________ (填“大于”“小于”或“等于”)氮化硅的硬度,原因是_____________ 。
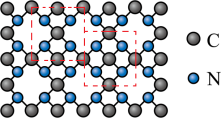
(2)氮化碳比氮化硅的硬度更大,其中β—氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知氮化碳的二维晶体结构如图,图中线框内表示晶胞结构。______________ 晶体。
②氮化碳的化学式为______________ 。
(3)三氧化铼 晶胞如图所示,其中O原子的配位数为
晶胞如图所示,其中O原子的配位数为________ ,已知该晶胞的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Re与O的最近距离为
,则Re与O的最近距离为________ cm。
(1)利用
 与
与 反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。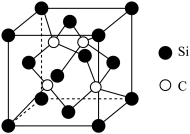

 。
。②碳化硅晶体中每个Si原子周围距离最近的C原子数目为
③碳化硅的晶胞参数为a pm,晶胞密度为
 ,则阿伏加德罗常数
,则阿伏加德罗常数
④碳化硅的硬度
(2)氮化碳比氮化硅的硬度更大,其中β—氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知氮化碳的二维晶体结构如图,图中线框内表示晶胞结构。
②氮化碳的化学式为
(3)三氧化铼
 晶胞如图所示,其中O原子的配位数为
晶胞如图所示,其中O原子的配位数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Re与O的最近距离为
,则Re与O的最近距离为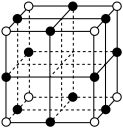
您最近一年使用:0次
7日内更新
|
70次组卷
|
2卷引用:甘肃省酒泉市四校联考2023-2024学年高二下学期5月期中考试化学试题
名校
3 . 常温下,随着溶液酸碱性变化,K2Cr2O7溶液的主要粒子成分也会发生变化。下列说法错误的是

A.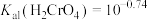 |
B.水的电离程度: |
C.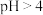 时 时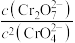 随着 随着 增大而减小 增大而减小 |
D. 时, 时,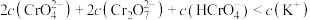 |
您最近一年使用:0次
名校
4 . 丙烯是石油化工的基本原料之一,在精细化学品合成、环保、医学科学和基础研究等领域应用广泛。回答下列问题:
(1)丙烷脱氢制丙烯过程的主反应为:
反应①:
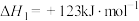 。
。
副反应有:
反应②:
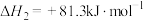
反应③: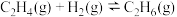
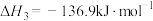
反应④: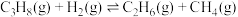

则
___________  。
。
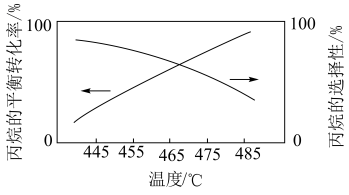
(2)已知:在纤维状BPO4/SiO2催化剂作用下,丙烷在一定温度下会发生(1)中反应①和反应②。丙烷的平衡转化率和丙烯的选择性随温度的变化如图所示,随着温度升高,丙烯的选择性降低的可能原因有___________ (答一条即可);丙烷的平衡转化率增大的原因是___________ 。 下,向
下,向 恒容密闭容器中充入
恒容密闭容器中充入 ,发生反应
,发生反应 ,经过
,经过 达到平衡状态,测得平衡时气体压强是开始时的1.2倍。
达到平衡状态,测得平衡时气体压强是开始时的1.2倍。
①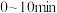 内丙烯的平均反应速率
内丙烯的平均反应速率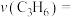
___________  。
。
②保持其他条件不变,反应达平衡后再向容器中充入少量 ,则
,则 的平衡转化率
的平衡转化率___________ (填“增大”“减小”或“不变”)。
③已知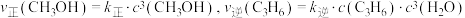 ,其中
,其中 、
、 为速率常数,只与温度有关,则
为速率常数,只与温度有关,则 时,
时,
___________ (结果保留两位有效数字)。
(4)在 、压强恒定为
、压强恒定为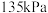 时,向有催化剂的密闭容器中按体积比
时,向有催化剂的密闭容器中按体积比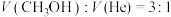 充入
充入 和
和 ,发生反应
,发生反应 ,达到平衡状态时
,达到平衡状态时 的转化率为
的转化率为 ,则该温度下,反应的平衡常数
,则该温度下,反应的平衡常数
___________  (用平衡分压代替平衡浓度计算,分压=总压
(用平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。
(1)丙烷脱氢制丙烯过程的主反应为:
反应①:

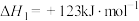 。
。副反应有:
反应②:

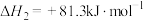
反应③:
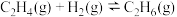
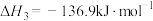
反应④:
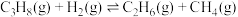

则

 。
。(2)已知:在纤维状BPO4/SiO2催化剂作用下,丙烷在一定温度下会发生(1)中反应①和反应②。丙烷的平衡转化率和丙烯的选择性随温度的变化如图所示,随着温度升高,丙烯的选择性降低的可能原因有
 下,向
下,向 恒容密闭容器中充入
恒容密闭容器中充入 ,发生反应
,发生反应 ,经过
,经过 达到平衡状态,测得平衡时气体压强是开始时的1.2倍。
达到平衡状态,测得平衡时气体压强是开始时的1.2倍。①
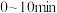 内丙烯的平均反应速率
内丙烯的平均反应速率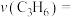
 。
。②保持其他条件不变,反应达平衡后再向容器中充入少量
 ,则
,则 的平衡转化率
的平衡转化率③已知
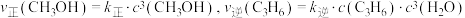 ,其中
,其中 、
、 为速率常数,只与温度有关,则
为速率常数,只与温度有关,则 时,
时,
(4)在
 、压强恒定为
、压强恒定为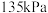 时,向有催化剂的密闭容器中按体积比
时,向有催化剂的密闭容器中按体积比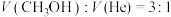 充入
充入 和
和 ,发生反应
,发生反应 ,达到平衡状态时
,达到平衡状态时 的转化率为
的转化率为 ,则该温度下,反应的平衡常数
,则该温度下,反应的平衡常数
 (用平衡分压代替平衡浓度计算,分压=总压
(用平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。
您最近一年使用:0次
解题方法
5 . 镁锰电池的结构如图所示,放电时总反应为 ,如果给镁锰电池充电,则会发生爆炸.下列说法错误的是
,如果给镁锰电池充电,则会发生爆炸.下列说法错误的是
 ,如果给镁锰电池充电,则会发生爆炸.下列说法错误的是
,如果给镁锰电池充电,则会发生爆炸.下列说法错误的是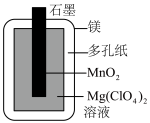
| A.负极为镁 | B.工作时,电子由镁电极流出,经过 溶液后进入石墨电极 溶液后进入石墨电极 |
| C.镁锰电池为一次电池 | D. 溶液中有自由移动的离子 溶液中有自由移动的离子 |
您最近一年使用:0次
2024-06-07更新
|
70次组卷
|
2卷引用:甘肃省白银市2023-2024学年高一下学期期中考试化学试题
名校
解题方法
6 . 电池在许多领域中扮演着重要角色,从移动设备到太空探索,从医疗设备到军事科技,无处不在.
(1)伏打电池是意大利教授伏打发明的电池组,开创了电学发展的新时代.一种伏打电池结构如图1所示,银片和锌片间隔有浸渍 溶液的纸板.伏打电池的正极为
溶液的纸板.伏打电池的正极为_________ (填“a”或“b”),若将银片换成__________ (填标号),则电流计中没有电子流过.
A.陶瓷片 B.锌片 C.铜片 D.镁片
(2)1859年,法国物理学家普兰特发明了铅酸蓄电池,其结构如图2所示.放电时,负极的质量________ (填“增大”“减小”或“不变”),正极上的电极反应式为________________ .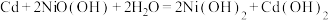 ,下列说法正确的是_______(填标号).
,下列说法正确的是_______(填标号).
(4)近年来,采用非贵重金属作为催化剂的节能环保的熔融碳酸盐燃料电池备受青睐,其工作原理如图4.该电池负极上的电极反应式为_______ ,相同条件下,正、负极消耗的气体的体积之比为_______ .
(1)伏打电池是意大利教授伏打发明的电池组,开创了电学发展的新时代.一种伏打电池结构如图1所示,银片和锌片间隔有浸渍
 溶液的纸板.伏打电池的正极为
溶液的纸板.伏打电池的正极为A.陶瓷片 B.锌片 C.铜片 D.镁片
(2)1859年,法国物理学家普兰特发明了铅酸蓄电池,其结构如图2所示.放电时,负极的质量
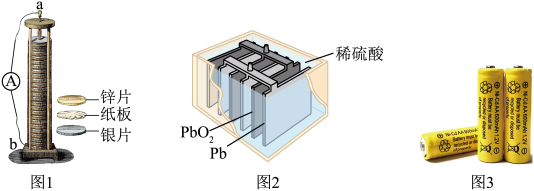
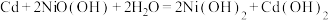 ,下列说法正确的是_______(填标号).
,下列说法正确的是_______(填标号).| A.镍镉电池充电时,化学能转化为电能 | B.放电时,负极发生了氧化反应 |
| C.电解质溶液为稀硫酸 | D.镍镉电池为二次电池 |
(4)近年来,采用非贵重金属作为催化剂的节能环保的熔融碳酸盐燃料电池备受青睐,其工作原理如图4.该电池负极上的电极反应式为
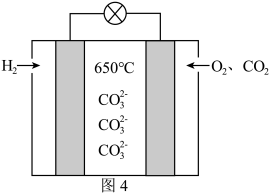
您最近一年使用:0次
2024-06-07更新
|
116次组卷
|
3卷引用:甘肃省白银市2023-2024学年高一下学期期中考试化学试题
解题方法
7 . 一定条件下,向2L恒容密闭容器中充入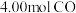 和
和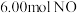 ,发生反应仅生成两种无毒气体。容器内两种气体的浓度随时间变化如图1所示,反应至
,发生反应仅生成两种无毒气体。容器内两种气体的浓度随时间变化如图1所示,反应至 时,仅改变某一反应条件,反应速率变化如图2所示.下列说法错误的是
时,仅改变某一反应条件,反应速率变化如图2所示.下列说法错误的是
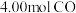 和
和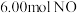 ,发生反应仅生成两种无毒气体。容器内两种气体的浓度随时间变化如图1所示,反应至
,发生反应仅生成两种无毒气体。容器内两种气体的浓度随时间变化如图1所示,反应至 时,仅改变某一反应条件,反应速率变化如图2所示.下列说法错误的是
时,仅改变某一反应条件,反应速率变化如图2所示.下列说法错误的是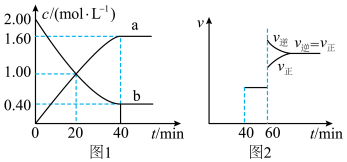
A.a表示 的浓度随时间的变化曲线 的浓度随时间的变化曲线 |
B. 时, 时, |
C.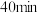 时,混合气体中CO的体积分数约为9.5% 时,混合气体中CO的体积分数约为9.5% |
D.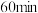 时,改变的条件可能是往容器内再充入 时,改变的条件可能是往容器内再充入 |
您最近一年使用:0次
8 . 甘肃像一块瑰丽的宝玉,镶嵌在中国中部的黄土高原、青藏高原和内蒙古高原上.下列甘肃博物馆的馆藏文物的材质属于无机硅酸盐材料的是
|
|
| A.鱼纹彩陶盆 | B.父癸铜卣 |
|
|
| C.四鸟纹金饰片 | D.彩绘木鸡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 .  是一种重要的化工原料,可用于制化肥、农药,炸药、染料等.工业制硝酸的流程如图所示.下列说法错误的是
是一种重要的化工原料,可用于制化肥、农药,炸药、染料等.工业制硝酸的流程如图所示.下列说法错误的是
 是一种重要的化工原料,可用于制化肥、农药,炸药、染料等.工业制硝酸的流程如图所示.下列说法错误的是
是一种重要的化工原料,可用于制化肥、农药,炸药、染料等.工业制硝酸的流程如图所示.下列说法错误的是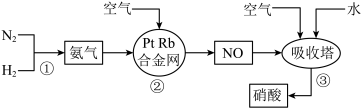
| A.反应①②③均属于氧化还原反应 |
B.若有 完全转化为 完全转化为 ,理论上共需要消耗 ,理论上共需要消耗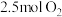 |
C.吸收塔内反应的化学方程式为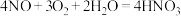 |
D.浓硝酸在光照下会逐渐变黄,原因是浓硝酸光照时分解生成了 |
您最近一年使用:0次
2024-06-07更新
|
143次组卷
|
2卷引用:甘肃省白银市2023-2024学年高一下学期期中考试化学试题
名校
解题方法
10 . 某化学兴趣小组利用图1装置(加热和夹持装置已省略)制备氨气并进行喷泉实验.
i.氨气的制备:打开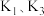 ,关闭
,关闭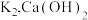 和
和 固体在甲处试管内反应生成
固体在甲处试管内反应生成 .
.
ⅱ.氨气的喷泉实验:当丁中溶液变蓝后,停止制备 ,关闭
,关闭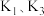 ,打开
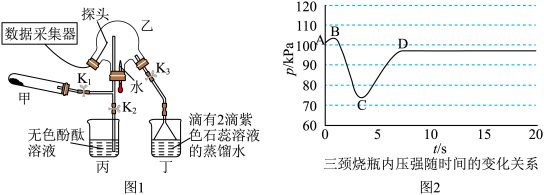
,打开 ,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.
,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.
请回答下列问题:___________________ ;丁处倒置漏斗的作用是______________ ;氨水中含有的分子有 、
、______________ .
(2)C→D过程中,三颈烧瓶中的现象为_____________ ; 能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为
能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为_____________ .
(3)该兴趣小组利用如图3所示装置进行另外一种喷泉实验.__________________________ .
②烧杯中发生反应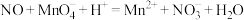 (未配平),该反应的氧化剂为
(未配平),该反应的氧化剂为__________ (填化学式),氧化产物和还原产物的物质的量之比为__________ (填最简整数比).
i.氨气的制备:打开
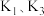 ,关闭
,关闭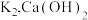 和
和 固体在甲处试管内反应生成
固体在甲处试管内反应生成 .
.ⅱ.氨气的喷泉实验:当丁中溶液变蓝后,停止制备
 ,关闭
,关闭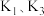 ,打开
,打开 ,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.
,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.请回答下列问题:
 、
、(2)C→D过程中,三颈烧瓶中的现象为
 能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为
能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为(3)该兴趣小组利用如图3所示装置进行另外一种喷泉实验.
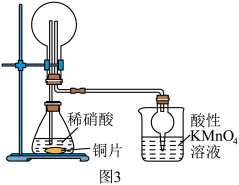
②烧杯中发生反应
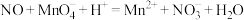 (未配平),该反应的氧化剂为
(未配平),该反应的氧化剂为
您最近一年使用:0次
2024-06-06更新
|
107次组卷
|
3卷引用:甘肃省白银市2023-2024学年高一下学期期中考试化学试题







