1 . 下列化学用语正确的是
A. 的电子式: 的电子式: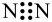 | B.丙烷的结构式: |
C. 分子的空间填充模型: 分子的空间填充模型: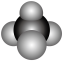 | D.羟基的电子式: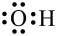 |
您最近一年使用:0次
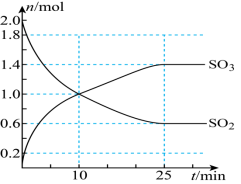
2 . 在2L恒温恒容密闭容器中投入2molSO2和1molO2在一定条件下充分反应,如图是SO2和SO3随时间的变化曲线。
(1)前10minSO3的平均反应速率为___________ ;平衡时,SO2的转化率为___________ 。
(2)下列叙述能判断该反应达到平衡状态的是___________ (填序号)。
②容器中气体密度不再改变
③SO3的质量不再改变
④O2的物质的量浓度不再改变
⑤SO2的消耗速率和SO3的生成速率相等
(3)以下操作会引起化学反应速率变快的是___________ (填字母)。
A.向容器中通入氦气 B.升高温度 C.扩大容器的容积 D.向容器中通入O2 E.使用催化剂
(4)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:___________ 。(填“正极”或“负极”)
②电解质溶液中OH-离子向___________ 移动(填“电极a”或“电极b”)。
③电极b的电极反应式为___________ 。
(1)前10minSO3的平均反应速率为
(2)下列叙述能判断该反应达到平衡状态的是
②容器中气体密度不再改变
③SO3的质量不再改变
④O2的物质的量浓度不再改变
⑤SO2的消耗速率和SO3的生成速率相等
(3)以下操作会引起化学反应速率变快的是
A.向容器中通入氦气 B.升高温度 C.扩大容器的容积 D.向容器中通入O2 E.使用催化剂
(4)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
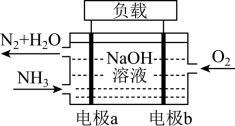
②电解质溶液中OH-离子向
③电极b的电极反应式为
您最近一年使用:0次
3 . 碘化亚铁( )在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收
)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收 )
)___________ ,若无此装置,写出铁粉参与的副反应的化学方程式:___________ 。
(2)硬质玻璃管直接接入收集器而不用导管的原因是___________ ,收集器浸泡在冷水中的原因是___________ 。
(3)试剂a的作用是___________ 。
(4)已知氧化性: 。往含
。往含 的溶液中通入
的溶液中通入 标准状况下的氯气,充分反应,请写出该反应的离子方程式:
标准状况下的氯气,充分反应,请写出该反应的离子方程式:___________ 。
 )在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收
)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收 )
)
(2)硬质玻璃管直接接入收集器而不用导管的原因是
(3)试剂a的作用是
(4)已知氧化性:
 。往含
。往含 的溶液中通入
的溶液中通入 标准状况下的氯气,充分反应,请写出该反应的离子方程式:
标准状况下的氯气,充分反应,请写出该反应的离子方程式:
您最近一年使用:0次
4 . 神舟十八号载人飞船成功发射,展现了中国航天事业的强大实力和技术水平。下列叙述不正确的是
| A.飞船使用的Si3N4隔热层属于新型无机非金属材料 |
| B.为空间站提供能量的砷化镓太阳能电池材料也可用SiO2代替 |
| C.电解熔融状态的氧化铝制得单质铝时,可加入些冰晶石来缩短加热时间 |
| D.火箭壳体采用的碳纤维缠绕复合材料强度高、密度小,可提高火箭的射程及运载能力 |
您最近一年使用:0次
解题方法
5 . 钛(Ti)和钛合金被广泛应用于火箭、导弹、航天飞机等领域。工业上以钛铁矿(FeTiO3,其中Ti为+4价)为主要原料制备金属钛的工艺流程如下图所示:
下列说法错误 的是

下列说法
| A.步骤①的反应过程元素的化合价没有发生变化 |
| B.步骤③的操作名称是加热或高温煅烧 |
C.步骤④的反应方程式TiO2+2C+2Cl2 TiCl4+2CO TiCl4+2CO |
| D.由TiCl4制备Ti的过程中,可以加入氮气做保护气体 |
您最近一年使用:0次
7日内更新
|
244次组卷
|
3卷引用:福建省部分优质高中2023-2024 学年高一第二学期期末模拟考试化学试卷
福建省部分优质高中2023-2024 学年高一第二学期期末模拟考试化学试卷湖南省部分校联考2024届高三下学期5月模拟考试化学试题(已下线)第05讲 氧化还原反应方程式的配平、书写及计算(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
6 . 下列各组离子在指定溶液中一定能大量共存的是
A.加入Al粉能产生 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B. (酸性)的溶液中: (酸性)的溶液中: 、 、 、 、 、 、 |
C.滴加硫氰化钾变为血红色的溶液中: 、 、 、 、 、 、 |
D.能使蓝色石蕊试纸变红的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-06-11更新
|
362次组卷
|
2卷引用:福建省部分优质高中2023-2024 学年高一第二学期期末模拟考试化学试卷
名校
7 . 下列过程中的化学反应,相应的离子方程式正确的是
A.用淀粉 溶液和醋酸检验加碘盐中的 溶液和醋酸检验加碘盐中的 : : |
B. 溶液中通入少量 溶液中通入少量 : :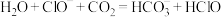 |
C.氯化亚铁溶液中加入酸性的 溶液: 溶液: |
D. 固体与氢碘酸反应: 固体与氢碘酸反应: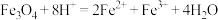 |
您最近一年使用:0次
2024-06-11更新
|
323次组卷
|
2卷引用:福建省部分优质高中2023-2024 学年高一第二学期期末模拟考试化学试卷
名校
8 . 糖类、油脂和蛋白质是非常重要的营养物质,下列说法正确的是
| A.淀粉和纤维素是天然有机高分子,且两者互为同分异构体 |
B.在试管中加入2mL 10% CuSO4溶液,滴加5滴5% NaOH溶液,得到新制的 。再加入2mL 10%葡萄糖溶液,加热,可以产生砖红色沉淀 。再加入2mL 10%葡萄糖溶液,加热,可以产生砖红色沉淀 |
C.一分子甘氨酸 和一分子苯丙氨酸( 和一分子苯丙氨酸(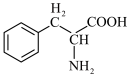 )可能形成两种二肽 )可能形成两种二肽 |
| D.油脂可以看作是高级脂肪酸与乙二醇通过酯化反应生成的酯 |
您最近一年使用:0次
2024-06-11更新
|
614次组卷
|
2卷引用:福建省部分优质高中2023-2024 学年高一第二学期期末模拟考试化学试卷
9 . 锰酸锂( )是锂电池的正极材料,有望取代
)是锂电池的正极材料,有望取代 。一种以废旧电池正极材料(主要成分为
。一种以废旧电池正极材料(主要成分为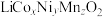 ,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备
,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下:
(1)Ni位于元素周期表中___________ 区;基态Mn原子的价层电子轨道表示式为___________ 。
(2)“灼烧”的目的是___________ 。
(3)根据“酸浸”前后物质价态的变化,推测双氧水的作用是___________ 。
(4)“沉锰”过程中,溶液先变为紫红色,一段时间后紫红色褪去。溶液变为紫红色的原因是___________ (用离子方程式表示,加入 溶液之前,锰以
溶液之前,锰以 形式存在)。“紫红色褪去”后,还可能有的实验现象是
形式存在)。“紫红色褪去”后,还可能有的实验现象是___________ 。
(5)“合成”在600~750℃下进行,写出发生反应的化学方程式:___________ 。
(6) 材料在脱锂过程中形成的某种晶体为六方晶系,结构如图,晶胞底面边长为a nm、高为b nm,
材料在脱锂过程中形成的某种晶体为六方晶系,结构如图,晶胞底面边长为a nm、高为b nm, ,
,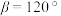 ,设
,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。___________ 。
②该晶体的密度为___________  。
。
 )是锂电池的正极材料,有望取代
)是锂电池的正极材料,有望取代 。一种以废旧电池正极材料(主要成分为
。一种以废旧电池正极材料(主要成分为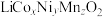 ,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备
,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下: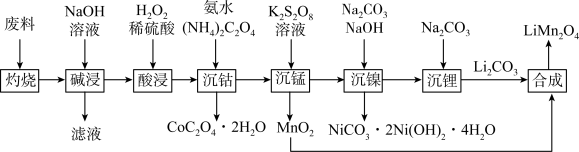
(1)Ni位于元素周期表中
(2)“灼烧”的目的是
(3)根据“酸浸”前后物质价态的变化,推测双氧水的作用是
(4)“沉锰”过程中,溶液先变为紫红色,一段时间后紫红色褪去。溶液变为紫红色的原因是
 溶液之前,锰以
溶液之前,锰以 形式存在)。“紫红色褪去”后,还可能有的实验现象是
形式存在)。“紫红色褪去”后,还可能有的实验现象是(5)“合成”在600~750℃下进行,写出发生反应的化学方程式:
(6)
 材料在脱锂过程中形成的某种晶体为六方晶系,结构如图,晶胞底面边长为a nm、高为b nm,
材料在脱锂过程中形成的某种晶体为六方晶系,结构如图,晶胞底面边长为a nm、高为b nm, ,
,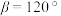 ,设
,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
②该晶体的密度为
 。
。
您最近一年使用:0次
10 . 废旧锌锰干电池内部的黑色物质A主要含有 、MnOOH、
、MnOOH、 、
、 、碳单质,用黑色物质A制备高纯
、碳单质,用黑色物质A制备高纯 的流程如图:
的流程如图: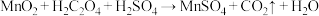 (未配平)。
(未配平)。
(1)第Ⅰ步操作是为了除去可溶性的__________ (填化学式)。
(2)第Ⅰ步后在空气中灼烧的目的有两个,一个是将MnOOH转化为 ,另一个是
,另一个是__________ 为灼烧时,MnOOH与空气中的氧气反应的化学方程式为____________________________ 。
(3)已知: 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第Ⅳ步中的多步操作可按如图步骤进行:
沉淀。第Ⅳ步中的多步操作可按如图步骤进行: 溶滴调节溶液pH的过程中有
溶滴调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为____________ ,你认为操作③中检测的方法及现象是________________ 时可继续进行操作④:操作④中用无水乙醇洗涤的目的是_________________________ (答一条即可)。
 、MnOOH、
、MnOOH、 、
、 、碳单质,用黑色物质A制备高纯
、碳单质,用黑色物质A制备高纯 的流程如图:
的流程如图: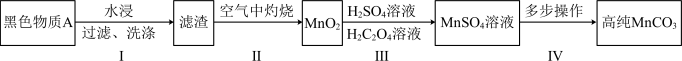
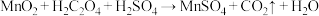 (未配平)。
(未配平)。(1)第Ⅰ步操作是为了除去可溶性的
(2)第Ⅰ步后在空气中灼烧的目的有两个,一个是将MnOOH转化为
 ,另一个是
,另一个是(3)已知:
 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第Ⅳ步中的多步操作可按如图步骤进行:
沉淀。第Ⅳ步中的多步操作可按如图步骤进行:
 溶滴调节溶液pH的过程中有
溶滴调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次
2024-05-08更新
|
192次组卷
|
2卷引用:福建省部分优质高中2023-2024 学年高一第二学期期末模拟考试化学试卷



