名校
1 . 简要回答下列问题
(1)氢氧化铝是典型且常用的抗酸药,具有抗酸、吸着、局部止血和保护溃疡面等作用。请用化学方程式表示其治疗胃酸过多的原理:___________ 。
(2)写出Cu在Cl2中燃烧的化学方程式:___________ 。
(3)如何用化学方法辨别溶液中是否含氯离子:___________ 。
(4)实验室浓硝酸应保存在棕色试剂瓶中并放置在阴凉处,其原因是______ (用化学方程式表示)。

(1)氢氧化铝是典型且常用的抗酸药,具有抗酸、吸着、局部止血和保护溃疡面等作用。请用化学方程式表示其治疗胃酸过多的原理:
(2)写出Cu在Cl2中燃烧的化学方程式:
(3)如何用化学方法辨别溶液中是否含氯离子:
(4)实验室浓硝酸应保存在棕色试剂瓶中并放置在阴凉处,其原因是
您最近一年使用:0次
名校
解题方法
2 . 下列各装置,能构成原电池的是
A.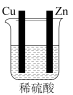 | B. | C.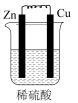 | D.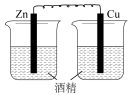 |
您最近一年使用:0次
名校
解题方法
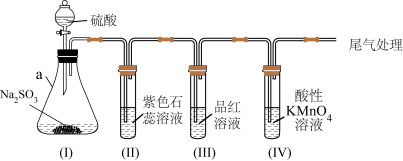
3 . 某化学兴趣小组利用如图装置制取并探究二氧化疏的性质。
(已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,部分夹持仪器已略去)
【实验探究】
(1)装置(I)仪器a的名称是___________ 。
(2)实验进行一段时间后:
①装置(II)中观察到紫色石蕊试液颜色变为___________ ,写出相关的化学方程式___________ 。
②装置(III)中品红溶液________ ,原因是________ ,加热后,溶液又恢复_________ ,可用于检验SO2。
③装置(IV)中酸性KMnO4溶液褪色,证明SO2具有___________ (填“氧化性”或“还原性”)。
(3)为防止SO2污染空气,尾气可用NaOH溶液吸收,写出该反应的离子方程式___________ 。
(4)用25.2gNa2SO3固体与足量硫酸反应,理论上可生成标准状况下SO2的体积为___________ L。(已知Na2SO3的摩尔质量为126g•mol-1)
【实验拓展】
(5)将装置(IV)中酸性KMnO4溶液换成Na2S溶液,可观察到溶液中出现浑浊,补充完整该反应的离子方程式:SO2+2___________ +4H+=3S↓+2H2O。
【知识应用】
(6)二氧化硫可作为食品添加剂。
查阅资料:国家食品添加剂使用标准中二氧化硫最大使用量
说明在严格控制用量的情况下,二氧化硫可被添加到食品中作为漂白剂、防腐剂和___________ (填“氧化剂”或“抗氧化剂”)。
(已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,部分夹持仪器已略去)

【实验探究】
(1)装置(I)仪器a的名称是
(2)实验进行一段时间后:
①装置(II)中观察到紫色石蕊试液颜色变为
②装置(III)中品红溶液
③装置(IV)中酸性KMnO4溶液褪色,证明SO2具有
(3)为防止SO2污染空气,尾气可用NaOH溶液吸收,写出该反应的离子方程式
(4)用25.2gNa2SO3固体与足量硫酸反应,理论上可生成标准状况下SO2的体积为
【实验拓展】
(5)将装置(IV)中酸性KMnO4溶液换成Na2S溶液,可观察到溶液中出现浑浊,补充完整该反应的离子方程式:SO2+2
【知识应用】
(6)二氧化硫可作为食品添加剂。
查阅资料:国家食品添加剂使用标准中二氧化硫最大使用量
| 食品名称 | 食糖 | 葡萄酒 | 水果干类 |
| SO2最大使用量 | 0.1g∙kg-1 | 0.25g∙kg-1 | 1g∙kg-1 |
您最近一年使用:0次
名校
解题方法
4 . Mg、Al和Cu是生活中常见的化学物质。用其组成的混合物进行如图所示实验,填写下列空白:

(1)步骤I和步骤II都涉及的实验操作是___________ ,实验所需的玻璃仪器有漏斗、烧杯和___________ 。
(2)气体X为___________ ,固体Z为___________ 。
(3)滤液Y中除H+外,还含有的阳离子为Al3+和___________ 。
(4)固体M为___________ ,由滤液Y生成固体M的化学反应方程式为___________ 。

(1)步骤I和步骤II都涉及的实验操作是
(2)气体X为
(3)滤液Y中除H+外,还含有的阳离子为Al3+和
(4)固体M为
您最近一年使用:0次
名校
解题方法
5 . 化学元素周期表(Periodictableofelements)是根据元素原子核电荷数从小至大排序的化学元素列表。如表是元素周期表的一部分,根据表中给出的10种元素(其中X、Y、Z分别表示某种化学元素),按要求作答。
(1)Z元素符号是___________ 。
(2)表中元素化学性质最稳定的是___________ (填元素符号)。
(3)地壳中含量最多的元素在元素周期表中的位置是___________ 。
(4)写出Na的原子结构示意图___________ 。
(5)主要用来制作高纯半导体、耐高温材料、光导纤维通信材料的元素名称是___________ 。
(6)卤族元素之一,属周期系VIIA族,在元素周期表中位于第二周期的元素是___________ 。
(7)O2与S单质相比,更难与H2化合的是___________ 。
(8)写出N元素的气态氢化物的化学式___________ ,该物质与水反应的化学方程式:___________ 。
(9)Cl2与水反应的生成物中具有漂白作用的是___________ (填化学式),写出Cl2与NaOH溶液反应的离子方程式:___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | X | N | O | F | Y | |||
| 3 | Na | Z | Al | Si | S | Cl |
(2)表中元素化学性质最稳定的是
(3)地壳中含量最多的元素在元素周期表中的位置是
(4)写出Na的原子结构示意图
(5)主要用来制作高纯半导体、耐高温材料、光导纤维通信材料的元素名称是
(6)卤族元素之一,属周期系VIIA族,在元素周期表中位于第二周期的元素是
(7)O2与S单质相比,更难与H2化合的是
(8)写出N元素的气态氢化物的化学式
(9)Cl2与水反应的生成物中具有漂白作用的是
您最近一年使用:0次
名校
解题方法
6 . 反应速率会受到许多因素的共同影响。在下列四个容积相同的密闭容器中,在一定条件下发生反应:N2+3H2⇌2NH3,其中生成NH3的反应速率最大的是
| 容器 | N2浓度/mol·L-1 | H2浓度/mol·L-1 | 温度/℃ | 催化剂 |
| A | 2 | 3 | 400 | 无 |
| B | 2 | 3 | 500 | 无 |
| C | 1 | 6 | 500 | 无 |
| D | 2 | 6 | 500 | 有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 溴水一般指溴单质溶于水形成的混合物,它与许多物质发生反应会改变其颜色。将下列物质分别加入溴水中,溴水的颜色不发生变化的是
| A.NaI固体 | B.NaOH固体 | C.CCl4液体 | D.KCl固体 |
您最近一年使用:0次
8 . 下列实验现象描述正确的是
| A.KOH溶液中滴加酚酞试液,一段时间后溶液呈无色 |
| B.新制Cu(OH)2悬浊液中加入葡萄糖溶液并加热,产生砖红色沉淀 |
| C.FeCl3溶液中滴入KSCN溶液,溶液呈蓝色 |
| D.H2在Cl2中燃烧,发出黄色火焰 |
您最近一年使用:0次
9 . 如图是某有机物的比例模型,该有机物的分子式是


| A.CH4 | B.C2H4 | C.C3H6 | D.C6H6 |
您最近一年使用:0次
名校
解题方法
10 . 以下反应中,水作还原剂的是
| A.2F2+2H2O=4HF+O2 | B.SO2+H2O=H2SO3 |
| C.2K+2H2O=2KOH+H2↑ | D.Cl2+H2O=HCl+HCIO |
您最近一年使用:0次



