名校
1 . 冠醚是一种超分子,它是由多个二元醇分子之间脱水形成的环状化合物。18—冠—6可用作相转移催化其与 形成的螯合离子结构如图所示。下列说法正确的是
形成的螯合离子结构如图所示。下列说法正确的是
 形成的螯合离子结构如图所示。下列说法正确的是
形成的螯合离子结构如图所示。下列说法正确的是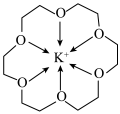
| A.该螯合离子形成的晶体类型为分子晶体 |
B.与二甲醚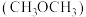 相比,该整合离子中“C-O-C”键角更大 相比,该整合离子中“C-O-C”键角更大 |
| C.该螯合离子中碳原子与氧原子杂化类型不同 |
| D.该螯合离子中所有非氢原子可以位于同一平面 |
您最近一年使用:0次
名校
2 . 一种抗癫痫药物的合成中间体的结构如图所示,下列关于该有机物的说法正确的是
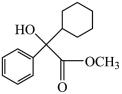
| A.属于芳香烃 | B.分子式为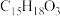 |
| C.苯环上的一氯代物有3种 | D.分子中含有2个手性碳原子 |
您最近一年使用:0次
3 . 为了方便和环保,煤应综合利用,干馏是较易实现的成熟方式。如下叙述不正确的是
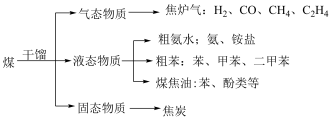
| A.煤的干馏属于化学变化,由粗苯获得甲苯属于物理变化 |
| B.煤的主要成分是炭和苯等 |
| C.粗氨水可以用于制化肥 |
| D.焦炭可用于炼铁 |
您最近一年使用:0次
名校
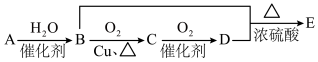
4 . 有机物A-E有如下转化关系,A是最简单的不饱和烃,B和D可做食品调味剂,E有浓郁香味。回答下列问题,___________ 。
(2)B的官能团名称是___________ 。
(3)A至E中属于电解质的物质的电离方程式是___________ 。
(4)以下物质与B溶液、D溶液作用有明显不同现象的是___________。
(5)如上转化中涉及多种反应类型,写出属于取代反应的化学方程式___________ 。
(6)E有较多的同分异构体,写出其中一种含有 和
和 的结构简式
的结构简式___________ 。
(7)A与苯反应生成乙苯: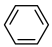

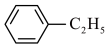 ,反应类型是
,反应类型是___________ 。
(2)B的官能团名称是
(3)A至E中属于电解质的物质的电离方程式是
(4)以下物质与B溶液、D溶液作用有明显不同现象的是___________。
| A.NaOH溶液 | B.NaHCO3溶液 | C.紫色石蕊试液 | D.苯 |
(5)如上转化中涉及多种反应类型,写出属于取代反应的化学方程式
(6)E有较多的同分异构体,写出其中一种含有
 和
和 的结构简式
的结构简式(7)A与苯反应生成乙苯:


 ,反应类型是
,反应类型是
您最近一年使用:0次
名校
解题方法
5 . 实验室可用浓硫酸和乙醇加热制取乙烯: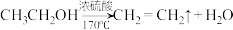 ,实验中会同170℃时生成炭而显黑色。下列叙述正确的是
,实验中会同170℃时生成炭而显黑色。下列叙述正确的是
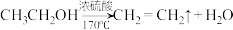 ,实验中会同170℃时生成炭而显黑色。下列叙述正确的是
,实验中会同170℃时生成炭而显黑色。下列叙述正确的是| A.如上反应属于加成反应 |
| B.可用双氧水制氧气的反应装置来发生如上反应 |
| C.生成炭的反应中,浓硫酸表现强氧化性 |
| D.乙烯密度比空气小,可用向下排空气法收集 |
您最近一年使用:0次
名校
6 . 如表所示是元素周期表的一部分,有关说法正确的是
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 二 | c | d | |||||
| 三 | a | b | e | f |
| A.e的简单氢化物比d的简单氢化物稳定 |
| B.a、b、e三种元素的原子半径:e>b>a |
| C.六种元素中,b元素的金属性最强 |
| D.c、e、f的最高价氧化物对应的水化物的酸性依次增强 |
您最近一年使用:0次
名校
7 . 阿伏加德罗常数的值为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.1mol丙烯(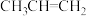 )分子中共面的原子数最多 )分子中共面的原子数最多 |
B.常温常压下,4.6g乙醇中C—H键的数目为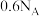 |
C.标况下,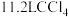 含共用电子对的数目为 含共用电子对的数目为 |
D.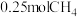 和 和 充分反应后的分子总数等于 充分反应后的分子总数等于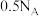 |
您最近一年使用:0次
名校
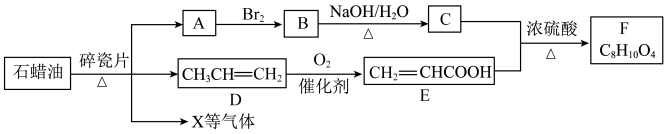
8 . A是米自石油的重要有机化工原料,其产量迫常用来衡量一个国家的石油化工发展水平,F是一种油状液体,转化关系如下图所示(部分反应条件、产物省略)。回答下列问题: RCH2OH
RCH2OH
(1)A的电子式为___________ 。
(2)A→B的化学反应方程式为___________ ,B的名称是___________ 。
(3)下列有关D的说法正确的是___________ (填字母)。
a.在水和四氯化碳中均易溶解 b能使酸性高锰酸钾溶液褪色
c.分子中最多有7个原子共平面 d.与HCl加成只生成一种产物
(4)根据上述已知信息,分析有机物C的结构简式是___________ 。
(5)E可用于制取聚丙烯酸树脂漆,聚丙烯酸的结构简式为___________ 。
 RCH2OH
RCH2OH(1)A的电子式为
(2)A→B的化学反应方程式为
(3)下列有关D的说法正确的是
a.在水和四氯化碳中均易溶解 b能使酸性高锰酸钾溶液褪色
c.分子中最多有7个原子共平面 d.与HCl加成只生成一种产物
(4)根据上述已知信息,分析有机物C的结构简式是
(5)E可用于制取聚丙烯酸树脂漆,聚丙烯酸的结构简式为
您最近一年使用:0次
9 . 下列关于物质结构的说法错误的是
| A.晶格能:NaF>NaCl>NaBr |
| B.基态碳原子核外有6种运动状态的电子 |
C.CH4和 都是正四面体结构,键角均为109°28′ 都是正四面体结构,键角均为109°28′ |
| D.甲醛(HCHO)的键角约为120°,分子之间存在氢键 |
您最近一年使用:0次
名校
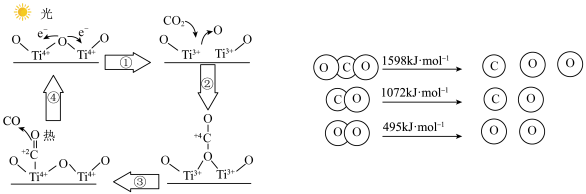
10 . 随着“碳达峰”、“碳中和”战略的提出,大气中CO2含量的控制和回收利用已成为当今化学研究的主题。
(1)科学家以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。______ 转化为______ 。过程①中TiO2发生了______ 反应(填“氧化”或“还原”)。根据数据计算,分解2molCO2需吸收______ kJ的能量。
(2)利用光解海水产生的H2将CO2转化为甲醇有利于减少温室气体二氧化碳排放,反应的化学方程式:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是
CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是______ (填标号)。
(3)某温度下,向2L的恒容密闭容器充入6molCO2和8molH2,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。
CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。______ mol•L-1•min-1;4min时,v正(H2)______ (填“>”“<”或“=”)v逆(H2)。
②能作为反应达到平衡状态的依据的是______ (填序号)。
a.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
b.容器内混合气体的密度不再改变
c.容器内总压强不再改变
d.单位时间内断裂3mol的H-H键,同时生成1mol的C=O键
(1)科学家以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
(2)利用光解海水产生的H2将CO2转化为甲醇有利于减少温室气体二氧化碳排放,反应的化学方程式:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是
CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是| A.减小容器体积 | B.升高温度 |
| C.使用合适催化剂 | D.恒容条件下充入He |
(3)某温度下,向2L的恒容密闭容器充入6molCO2和8molH2,发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。
CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。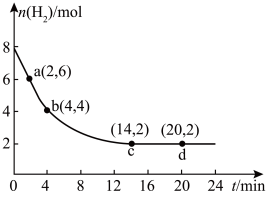
②能作为反应达到平衡状态的依据的是
a.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
b.容器内混合气体的密度不再改变
c.容器内总压强不再改变
d.单位时间内断裂3mol的H-H键,同时生成1mol的C=O键
您最近一年使用:0次



