名校
1 . 下列离子方程式书写正确的是
A.铁与硫酸铜溶液反应: |
B.氨水与盐酸反应: |
C.二氧化氮与水反应: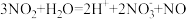 |
D.铁和稀硝酸反应: |
您最近一年使用:0次
名校
2 . 如图为元素周期表的一部分,参照元素①~⑩在表中的位置,回答下列问题:
(1)写出元素镁在元素周期表中的位置_______________ 。
(2)第三周期中非金属性最强的元素的原子形成简单离子的结构示意图为________________ 。
(3)③⑦⑩最高价氧化物对应水化物酸性由强到弱的顺序为(填化学式)______________ 。
(4)写出②的单质在足量④的单质中燃烧产物的电子式______________ 。
(5)④和⑨的单质均能与 反应生成
反应生成 型化合物,请判断这两种
型化合物,请判断这两种 型化合物的热稳定性(填化学式)
型化合物的热稳定性(填化学式)______________ 。
(6)由表中①、③、④、⑥、⑩元素形成的常见物质Z、M、N可发生以下反应:___________ (填字母)。
a.离子键 b.极性共价键 c.非极性共价键
ⅱ.Z→N的化学方程式_______________ 。
族周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
(1)写出元素镁在元素周期表中的位置
(2)第三周期中非金属性最强的元素的原子形成简单离子的结构示意图为
(3)③⑦⑩最高价氧化物对应水化物酸性由强到弱的顺序为(填化学式)
(4)写出②的单质在足量④的单质中燃烧产物的电子式
(5)④和⑨的单质均能与
 反应生成
反应生成 型化合物,请判断这两种
型化合物,请判断这两种 型化合物的热稳定性(填化学式)
型化合物的热稳定性(填化学式)(6)由表中①、③、④、⑥、⑩元素形成的常见物质Z、M、N可发生以下反应:
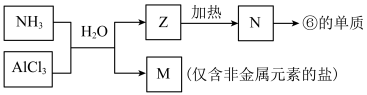
a.离子键 b.极性共价键 c.非极性共价键
ⅱ.Z→N的化学方程式
您最近一年使用:0次
名校
3 . 结构是预测物质性质的重要依据。下列说法错误的是
| A.电负性:Cl>S>P | B.热稳定性: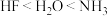 |
| C.第一电离能:N>O>C | D.酸性: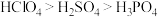 |
您最近一年使用:0次
4 . X、Y、Z、W为原子序数依次增大的四种元素, 和
和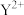 具有相同的电子构型,Z、W为同周期元素,Z核外电子总数是其最外层电子数的3倍,W最外层有一个未成对电子。下列说法正确的是
具有相同的电子构型,Z、W为同周期元素,Z核外电子总数是其最外层电子数的3倍,W最外层有一个未成对电子。下列说法正确的是
 和
和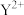 具有相同的电子构型,Z、W为同周期元素,Z核外电子总数是其最外层电子数的3倍,W最外层有一个未成对电子。下列说法正确的是
具有相同的电子构型,Z、W为同周期元素,Z核外电子总数是其最外层电子数的3倍,W最外层有一个未成对电子。下列说法正确的是| A.Z的最高价氧化物的熔点高于Y的最高价氧化物的熔点 |
| B.W和Y的氢化物所属的晶体类型分别为分子晶体和离子晶体 |
| C.基态X原子的核外电子有8种不同的空间运动状态 |
D.工业上常采用电解熔融化合物 的方式制备单质Y 的方式制备单质Y |
您最近一年使用:0次
名校
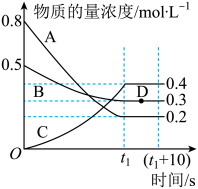
5 . 如图表示在一定的温度下,容积固定的密闭容器中,A、B、C三种气体的物质的量浓度随时间变化的情况。
(1)该反应的化学方程式为___________ 。
(2)0~t1s内气体B的平均反应速率为___________ 。
(3)(t1+10)s时,B的物质的量分数为___________ (结果保留一位小数)。
(4)能判断该反应在一定温度下达到化学平衡状态的依据是___________ (填字母)。
a.容器中压强不变 b.混合气体中 不变
不变
c.容器中气体密度不变 d.
(5)容器中(t1+10)s时的压强与起始时的压强之比为___________ 。
(1)该反应的化学方程式为
(2)0~t1s内气体B的平均反应速率为
(3)(t1+10)s时,B的物质的量分数为
(4)能判断该反应在一定温度下达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中
 不变
不变c.容器中气体密度不变 d.

(5)容器中(t1+10)s时的压强与起始时的压强之比为
您最近一年使用:0次
名校
解题方法
6 . 下列化学用语中正确的是
A.聚丙烯的结构简式: |
B. 的电子式: 的电子式: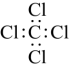 |
C. 分子的空间填充模型: 分子的空间填充模型: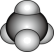 |
D.异丁烷的结构简式: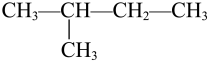 |
您最近一年使用:0次
名校
解题方法
7 . 依据 几种烃分子的结构示意图填空。
几种烃分子的结构示意图填空。___________ 。
(2)B的名称是___________ 。工业制乙醇的化学方程式为___________ 。
(3)D的分子式是___________ 。
(4) 、
、 的关系是
的关系是___________ (填“同系物”“同分异构体”或“同一种物质”)。
(5) 表示的物质中,属于不饱和烃的物质是
表示的物质中,属于不饱和烃的物质是___________ (填序号)。
(6)分子式比 多2个CH2的饱和链状烷烃的结构有
多2个CH2的饱和链状烷烃的结构有___________ 种,其一氯代物只有一种的同分异构体的结构简式为___________ 。
(7)分子中含有30个氢原子的饱和链状烷烃的分子式为___________ 。
 几种烃分子的结构示意图填空。
几种烃分子的结构示意图填空。
(2)B的名称是
(3)D的分子式是
(4)
 、
、 的关系是
的关系是(5)
 表示的物质中,属于不饱和烃的物质是
表示的物质中,属于不饱和烃的物质是(6)分子式比
 多2个CH2的饱和链状烷烃的结构有
多2个CH2的饱和链状烷烃的结构有(7)分子中含有30个氢原子的饱和链状烷烃的分子式为
您最近一年使用:0次
8 . 硅单质及其化合物应用广泛。请回答下列问题:
(1)硅元素在元素周期表的位置是_______ 。
(2)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:_______ 。
该生产过程中可以循环使用的物质是_______ 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式_______ 。
(3)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下:
3SiO2+6C+2N2 Si3N4+6CO。若消耗24g C时,反应过程中转移的电子为
Si3N4+6CO。若消耗24g C时,反应过程中转移的电子为_______ mol。
(4)实验室装氢氧化钠溶液的玻璃试剂瓶,不选择玻璃塞,请用化学方程式表明原因:_______ 。
(1)硅元素在元素周期表的位置是
(2)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:
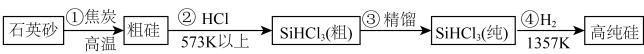
该生产过程中可以循环使用的物质是
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式
(3)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下:
3SiO2+6C+2N2
 Si3N4+6CO。若消耗24g C时,反应过程中转移的电子为
Si3N4+6CO。若消耗24g C时,反应过程中转移的电子为(4)实验室装氢氧化钠溶液的玻璃试剂瓶,不选择玻璃塞,请用化学方程式表明原因:
您最近一年使用:0次
名校
9 . 如图是关于反应A2(g)+3B2(g)⇌2C(g) ΔH<0的平衡移动图像,影响平衡移动的原因可能是

| A.升高温度,同时增大压强 |
| B.降低温度同时减小压强 |
| C.增大B2的浓度,同时使用催化剂 |
| D.增大A2的浓度,同时减小C的浓度 |
您最近一年使用:0次
名校
10 . N2(g)和O2(g)反应生成NO(g)过程中能量变化情况如下图a所示,下列说法正确的是
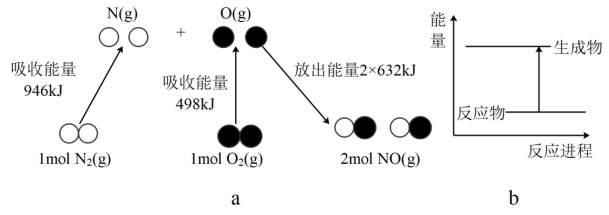
| A.N2(g)和O2 (g)的反应过程中,断开化学键吸收的总能量小于形成化学键释放的总能量 |
| B.等物质的量的N2(g)、N2(l)具有的能量前者较高 |
| C.图b表示的反应为放热反应 |
| D.N2(g)+ O2(g)=2 NO(g) △H=+1444 kJ/mol |
您最近一年使用:0次



