名校
解题方法
1 . 下列关于反应能量的说法正确的是
| A.化学反应中的能最变化,全都表现为热量的变化 |
| B.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C.需要加热才能进行的反应一定是吸热反应、放热反应不需要加热 |
| D.相同条件下1mol氢原子所具有的能量为E1,1mol氢分子的能量为E2,则2E1=E2 |
您最近一年使用:0次
名校
解题方法
2 . 中国化学家研究出一种新型复合光催化剂(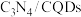 ),可以利用太阳光高效分解水其原理如图所示。下列说法错误的是
),可以利用太阳光高效分解水其原理如图所示。下列说法错误的是
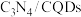 ),可以利用太阳光高效分解水其原理如图所示。下列说法错误的是
),可以利用太阳光高效分解水其原理如图所示。下列说法错误的是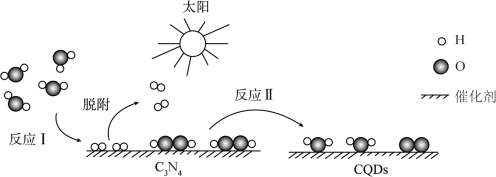
| A.反应Ⅰ是放热反应 |
| B.反应Ⅰ涉及极性键的断裂与非极性键的形成 |
C. 是中间产物, 是中间产物,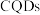 能催化其分解 能催化其分解 |
| D.整个过程实现了太阳能向化学能转化 |
您最近一年使用:0次
3 . 几种晶体的晶胞(或晶体结构)如图所示,下列说法正确的是
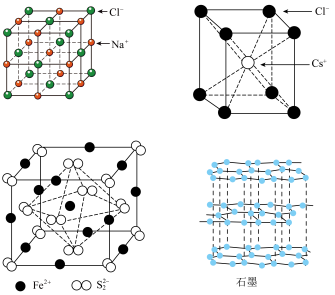
A. 中 中 的配位数大于干冰中 的配位数大于干冰中 分子的配位数 分子的配位数 |
B. 晶胞中,若 晶胞中,若 作顶点,则 作顶点,则 应在面心处 应在面心处 |
C.若 的晶胞边长为apm,其中S原子的半径为 的晶胞边长为apm,其中S原子的半径为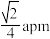 |
| D.石墨晶体层内作用力是共价键,层间作用力是范德华力,所以石墨是一种混合型晶体 |
您最近一年使用:0次
名校
4 . 化学反应中的能量变化,通常表现为热量的变化,研究化学反应中的热量变化具有重要的意义。
(1)下列变化属于吸热反应的是_______ (填序号)。
①液态水气化;②胆矾加热变成白色粉末;③浓硫酸稀释;④氢气还原氧化铜;⑤盐酸和碳酸氢钠反应;⑥氢氧化钾和稀硫酸反应;⑦灼热的木炭与 的反应;⑧
的反应;⑧ 晶体与
晶体与 晶体的反应;⑨甲烷在空气中燃烧的反应
晶体的反应;⑨甲烷在空气中燃烧的反应
(2)已知:
 ;
;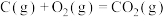
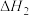
则
_______ 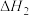 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)若
 ,则
,则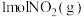 置于密闭容器中充分反应放出的热量
置于密闭容器中充分反应放出的热量_______ 28.45kJ(填“>”、“<”或“=”)。
(4)①已知:
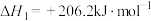

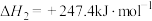
则 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为_______ 。
(5)用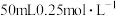 稀
稀 与
与 溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题:
溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题:_______ 。
②实验中若用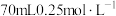 稀
稀 与
与 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”或“不相等”)。
③已知:中和反应后生成的溶液的比热容 为
为 ,溶液的密度均为
,溶液的密度均为 ,某学习小组三次实验测得温度平均升高3.4℃。则生成
,某学习小组三次实验测得温度平均升高3.4℃。则生成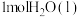 时放出的热量为
时放出的热量为_______ kJ。(结果保留一位小数)
④若上述实验所测中和热数值偏小,产生偏差的原因可能是_______ 。
a.实验装置保温、隔热效果差
b.量筒量取溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定 溶液的温度
溶液的温度
(1)下列变化属于吸热反应的是
①液态水气化;②胆矾加热变成白色粉末;③浓硫酸稀释;④氢气还原氧化铜;⑤盐酸和碳酸氢钠反应;⑥氢氧化钾和稀硫酸反应;⑦灼热的木炭与
 的反应;⑧
的反应;⑧ 晶体与
晶体与 晶体的反应;⑨甲烷在空气中燃烧的反应
晶体的反应;⑨甲烷在空气中燃烧的反应(2)已知:

 ;
;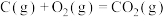
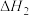
则

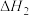 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)若

 ,则
,则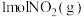 置于密闭容器中充分反应放出的热量
置于密闭容器中充分反应放出的热量(4)①已知:

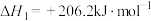

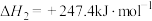
则
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(5)用
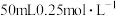 稀
稀 与
与 溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题:
溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题: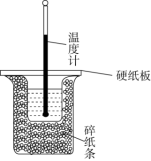
②实验中若用
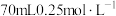 稀
稀 与
与 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量③已知:中和反应后生成的溶液的比热容
 为
为 ,溶液的密度均为
,溶液的密度均为 ,某学习小组三次实验测得温度平均升高3.4℃。则生成
,某学习小组三次实验测得温度平均升高3.4℃。则生成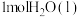 时放出的热量为
时放出的热量为④若上述实验所测中和热数值偏小,产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.量筒量取溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定
 溶液的温度
溶液的温度
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题。
(1)下列化学反应可以设计成原电池的是_______。
(2)观察图,回答问题。_______ 能。
②Zn电极是_______ 极(填“正”或“负”)极,正极反应为_______ (填“氧化反应”或“还原反应”),电极反应式_______ 。
③电子移动方向_______ ,溶液中氢离子向_______ (填“正”或“负”)极移动。
④标准状况下,若反应过程中溶解了6.5g锌,则正极生成的产物的体积为_______ L。
(1)下列化学反应可以设计成原电池的是_______。
A. | B. |
C. | D. |
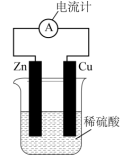
②Zn电极是
③电子移动方向
④标准状况下,若反应过程中溶解了6.5g锌,则正极生成的产物的体积为
您最近一年使用:0次
6 . 向恒温、体积为 的真空容器中通入
的真空容器中通入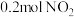 ,在
,在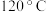 时发生反应
时发生反应
 ,测得平衡时
,测得平衡时 为
为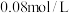 。各物质的消耗速率存在关系:
。各物质的消耗速率存在关系: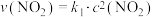 ,
,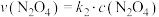 ,且消耗速率随浓度变化的如下图所示,下列有关说法正确的是
,且消耗速率随浓度变化的如下图所示,下列有关说法正确的是
 的真空容器中通入
的真空容器中通入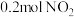 ,在
,在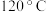 时发生反应
时发生反应
 ,测得平衡时
,测得平衡时 为
为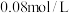 。各物质的消耗速率存在关系:
。各物质的消耗速率存在关系: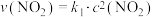 ,
,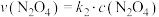 ,且消耗速率随浓度变化的如下图所示,下列有关说法正确的是
,且消耗速率随浓度变化的如下图所示,下列有关说法正确的是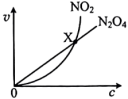
A.图中 点处在平衡状态 点处在平衡状态 |
B.在温度 时,若 时,若 ,则 ,则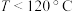 |
C.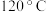 ,在 ,在 真空容器中通入 真空容器中通入 ,则平衡转化率为 ,则平衡转化率为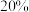 |
D.向上述容器再通入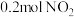 ,达新平衡时 ,达新平衡时 的体积分数将增大 的体积分数将增大 |
您最近一年使用:0次
7 . 某同学利用下列装置(加热和夹持装置已省略)分离CH2Cl2(沸点为39.8℃)和CCl4(沸点为76.5℃),下列说法错误的是
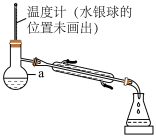
| A.仪器a的名称为蒸馏烧瓶 |
| B.冷凝水从下口进 |
| C.实验中可以用水浴进行加热,且温度计的水银球应靠近支管口 |
| D.可以用球形冷凝管代替直形冷凝管进行实验 |
您最近一年使用:0次
8 . 下列化学用语或有机物的命名正确的是
A. 的系统命名为2,4-二乙基戊烷 的系统命名为2,4-二乙基戊烷 |
B.甲烷的空间填充模型为 |
C.新戊烷的结构简式为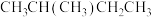 |
D.化学式为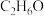 且核磁共振氢谱有三组峰的物质的结构式为 且核磁共振氢谱有三组峰的物质的结构式为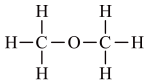 |
您最近一年使用:0次
解题方法
9 . 四乙氧基硅烷Si(OC2H5)4具有广泛工业用途。某小组用SiCl4和C2H5OH反应制备Si(OC2H5)4,并探究影响产率的因素。相关物质的沸点和水解性如下:
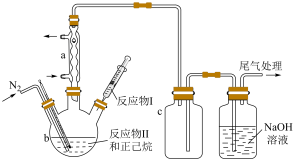
实验装置示意简图如图所示(加热及夹持装置略)。
(1)制备Si(OC2H5)4
①仪器a的名称是___________ ;c瓶的作用是___________ 。
②b中生成Si(OC2H5)4的化学方程式为___________ 。
③反应过程中有H2O和C2H5Cl生成,但混合物中未检出H2O的原因是___________ ;滤液质谱图中也无C2H5Cl的特征峰的原因是___________ 。
④当馏出液为产品时,蒸馏温度应控制在___________ ℃。
(2)影响产率的因素
①控制变量法可用于探究影响产率的因素,在设计实验时需要考虑的变量有___________ 。
A.反应温度 B.溶剂类型 C.加料顺序 D.滴加速率
②N2流速对产率也有影响,随着N2流速增大,产率先增大后减小,主要原因是___________ 。
| 物质 | SiCl4 | C2H5OH | Si(OC2H5)4 | 正己烷 | C2H5Cl |
| 沸点/℃ | 58 | 78 | 168 | 68 | 12 |
| 水解性 | 易水解 | — | 易水解 | 一 | — |
(1)制备Si(OC2H5)4
①仪器a的名称是
②b中生成Si(OC2H5)4的化学方程式为
③反应过程中有H2O和C2H5Cl生成,但混合物中未检出H2O的原因是
④当馏出液为产品时,蒸馏温度应控制在
(2)影响产率的因素
①控制变量法可用于探究影响产率的因素,在设计实验时需要考虑的变量有
A.反应温度 B.溶剂类型 C.加料顺序 D.滴加速率
②N2流速对产率也有影响,随着N2流速增大,产率先增大后减小,主要原因是
您最近一年使用:0次
解题方法
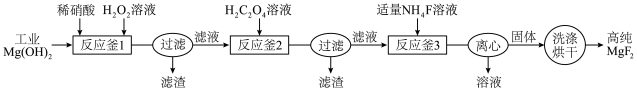
10 . 高纯MgF2在光子晶体等领域应用广泛。一种利用工业Mg(OH)2(含少量Ca、Fe、Mn等元素的氧化物)制备高纯MgF2的工艺如下。
回答下列问题:
(1)基态F的电子排布式为___________ , 的空间结构为
的空间结构为___________ 。
(2)反应釜1中,加入稀硝酸溶解后,调节pH至7.5,生成的沉淀主要是___________ ,再加入H2O2,除去的金属元素是___________ 。
(3)反应釜2中,为使Ca2+沉淀完全, 浓度应大于
浓度应大于___________ mol/L(CaC2O4的Ksp=2.0×10-9)。
(4)反应釜3中,反应的离子方程式为___________ 。
(5)离心后的溶液经浓缩结晶,所得固体的主要成分是___________ ;现称取一定量该固体配成溶液,取20.00mL,加入足量HCHO,反应为:4 +6HCHO=(CH2)6N4H++3H++6H2O,(CH2)6N4H+的酸性与醋酸接近,以酚酞作指示剂,用0.2000mol/LNaOH标准溶液滴定,消耗24.00mL,则所配溶液的
+6HCHO=(CH2)6N4H++3H++6H2O,(CH2)6N4H+的酸性与醋酸接近,以酚酞作指示剂,用0.2000mol/LNaOH标准溶液滴定,消耗24.00mL,则所配溶液的 浓度为
浓度为___________ mol/L。
| 离子 | Mg2+ | Ca2+ | Fe2+ | Fe3+ | Mn2+ |
| 完全沉淀的pH | 10.6 | 13.9 | 9.0 | 2.8 | 10.1 |
(1)基态F的电子排布式为
 的空间结构为
的空间结构为(2)反应釜1中,加入稀硝酸溶解后,调节pH至7.5,生成的沉淀主要是
(3)反应釜2中,为使Ca2+沉淀完全,
 浓度应大于
浓度应大于(4)反应釜3中,反应的离子方程式为
(5)离心后的溶液经浓缩结晶,所得固体的主要成分是
 +6HCHO=(CH2)6N4H++3H++6H2O,(CH2)6N4H+的酸性与醋酸接近,以酚酞作指示剂,用0.2000mol/LNaOH标准溶液滴定,消耗24.00mL,则所配溶液的
+6HCHO=(CH2)6N4H++3H++6H2O,(CH2)6N4H+的酸性与醋酸接近,以酚酞作指示剂,用0.2000mol/LNaOH标准溶液滴定,消耗24.00mL,则所配溶液的 浓度为
浓度为
您最近一年使用:0次



