解题方法
1 . 发生化学反应时,物质变化的同时常常伴随有能量变化。
(1)将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为___________ 能。
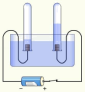
(2)原电池是直接把化学能转化为电能的装置,如图所示。___________ 、___________ 、___________ (字母序号)
A.电极反应物 B. 失电子场所 C.得电子场所 D. 离子导体
②请分析该装置中电流形成的原因___________ 。(用化学用语及文字表述)
(3)已知:键能是指气态分子中,1 mol化学键解离成气态原子所吸收的能量。
当H2和O2化合生成2 mol H2O(g)时,___________ (填“吸收”或“放出”)能量___________ kJ。下列能从化学键角度 正确表示该过程的能量变化示意图的是___________ (填字母)。_________ ;正极材料________ ;离子导体_______ 。
(1)将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为
(2)原电池是直接把化学能转化为电能的装置,如图所示。
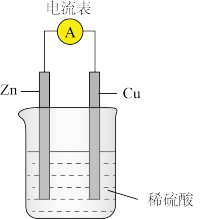
A.电极反应物 B. 失电子场所 C.得电子场所 D. 离子导体
②请分析该装置中电流形成的原因
(3)已知:键能是指气态分子中,1 mol化学键解离成气态原子所吸收的能量。
| 化学键 | 氢氢键 | 氧氧键 | 氢氧键 |
| 键能/kJ·mol-1 | 436 | 498 | 463 |
A. 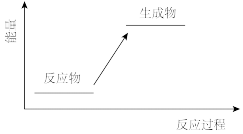 B.
B.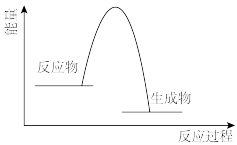 C.
C. 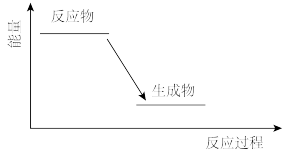 D.
D.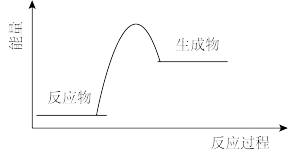

您最近一年使用:0次
解题方法
2 . 下列关于物质用途的表述不正确 的是
| A | B | C | D |
纯碱 | 84消毒液(有效成分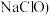 | 过氧化钠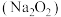 | 铁红 |
| 食用碱 | 杀灭细菌 | 供氧剂 | 磁铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 某元素的原子结构示意图为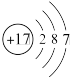 。下列关于该元素的说法中,
。下列关于该元素的说法中,
| A.元素符号是Cl | B.属于短周期元素 |
| C.原子在化学反应中易失去电子 | D.最高正化合价是 价 价 |
您最近一年使用:0次
4 . 下表为元素周期表的一部分,请参照①~⑧在表中的位置,回答下列问题。
(1)元素①的原子结构示意图:___________ 。
(2)元素③和⑦可形成化合物,用电子式表示其形成过程:___________ 。
(3)比较元素②、③的离子半径大小:___________ (用离子符号表示)。
(4)元素③、④、⑤组成的单质中,与水反应最剧烈的是___________ (用元素符号表示),该反应的离子方程式:___________ 。
(5)③的最高价氧化物对应的水化物中含有的化学键类型为___________ ,形成化合物的类型:___________ (填“离子化合物”或“共价化合物”)。
(6)比较元素⑥、⑦形成的单质的氧化性强弱:___________ (用化学式表示),请从原子结构的角度解释原因:___________ 。从实验证据的角度列举能证明其氧化性强弱关系的反应___________ (写化学方程式或离子方程式)。
(7)已知硒(34Se)与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质:___________ 。
a. Se的最低负化合价为-2价 b. SeO2既有氧化性又有还原性
c.Se的气态氢化物的稳定性比⑥的强 d.最高价氧化物对应的水化物为H2SeO3
| 族 周期 | IA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ||||
| 4 | ⑧ | ||||||||
(2)元素③和⑦可形成化合物,用电子式表示其形成过程:
(3)比较元素②、③的离子半径大小:
(4)元素③、④、⑤组成的单质中,与水反应最剧烈的是
(5)③的最高价氧化物对应的水化物中含有的化学键类型为
(6)比较元素⑥、⑦形成的单质的氧化性强弱:
(7)已知硒(34Se)与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质:
a. Se的最低负化合价为-2价 b. SeO2既有氧化性又有还原性
c.Se的气态氢化物的稳定性比⑥的强 d.最高价氧化物对应的水化物为H2SeO3
您最近一年使用:0次
5 . 硫酸钡(BaSO4)是一种用于胃肠道造影检查的辅助用药。钡(56Ba)与镁(12Mg)是同族元素,关于钡的性质的判断正确的是
| A.Ba是第五周期第ⅡA族元素 | B.碱性:Ba(OH)2 > Mg(OH)2 |
| C.金属性:Ca > Ba | D.离子半径:Cs+ < Ba2+ |
您最近一年使用:0次
6 . 下列化学用语或图示表达不正确 的是
| A.Cl的最高价氧化物化学式:Cl2O7 |
B.硫元素的原子结构示意图: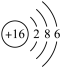 |
C.水分子的空间结构示意图: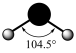 |
D.CO2的电子式: |
您最近一年使用:0次
解题方法
7 . 下列描述中涉及将化学能转化为电能的是
|
|
|
|
| A.水力发电 | B.汽车的燃料电池 | C.甲烷燃烧 | D. 电解水制氢气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 下列性质的比较中,不正确的是
A.电负性: | B.第一电离能: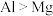 |
C.微粒半径: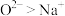 | D.酸性: |
您最近一年使用:0次
9 . 下列有关乙醛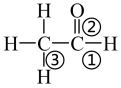 的说法
的说法
| A.可与酸性KMnO4溶液发生氧化反应,断①键 |
| B.②为不饱和键,可与H2发生加成反应 |
| C.由电负性大小推断,与NH3加成生成CH3CH2ONH2 |
| D.受醛基影响,极性键③易断,可发生取代反应 |
您最近一年使用:0次
解题方法
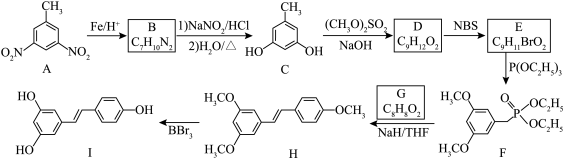
10 . 葡萄、桑葚等水果含较多白藜芦醇(化合物Ⅰ)。白藜芦醇是一种天然的抗氧化剂,具有抗菌、抗炎、抗过敏、抗血栓作用。以下是某课题组合成化合物Ⅰ的路线。
(1)由A生成B的反应类型为___________ 。
(2)I中官能团名称为___________ 。
(3)由E生成F的化学方程式为___________ 。
(4)已知G可以发生银镜反应,G的结构简式为___________ 。
(5)由C生成D,再由H生成I,上述过程的目的是___________ 。
(6)白藜芦醇苯环上的一氯代物有___________ 种同分异构体,写出其中两种同分异构体的结构简式:___________ 、___________ 。
(1)由A生成B的反应类型为
(2)I中官能团名称为
(3)由E生成F的化学方程式为
(4)已知G可以发生银镜反应,G的结构简式为
(5)由C生成D,再由H生成I,上述过程的目的是
(6)白藜芦醇苯环上的一氯代物有
您最近一年使用:0次