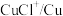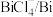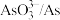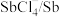名校
1 . 甲硝唑主要用作治疗或预防厌氧菌引起的系统或局部感染,结构简式如图所示,杂环中存在大 键。下列说法错误的是
键。下列说法错误的是
 键。下列说法错误的是
键。下列说法错误的是
A.该分子中①号 更易和盐酸形成盐,增大药物水溶性 更易和盐酸形成盐,增大药物水溶性 |
| B.该分子可发生加成反应、消去反应 |
| C.该分子中含有两种含氧官能团 |
| D.该分子是极性分子 |
您最近一年使用:0次
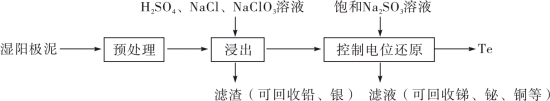
2 . 碲(Te)是一种重要的稀有分散元素,广泛应用于冶金、石油、化工、航空、电子等领域。以某冶炼厂的湿阳极泥(含水26%,主要含锑、砷、铅、铋、银和少量铜、碲等)为原料回收碲的流程如下:
请回答下列问题:
(1)52Te的基态原子的电子排布式为___________ 。
(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是_______________ ;氧化后的原料还需粉碎、过筛,目的是_________________ 。
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为___________ 、___________ ;添加 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式________________ 。
(4)电解时为防止除Te以外的单质生成,需控制电位的范围为___________ ;加入饱和Na2SO3溶液还原 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成_____________ (填化学式)。
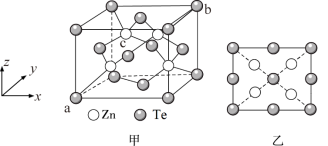
(5)将碲与锌一起加热,然后升华可制得碲化锌。碲化锌是一种重要的半导体材料,图甲为它的一种立方晶胞结构,图乙为该晶胞沿z轴投影图。已知a点的坐标为(0,0,0),b点的坐标为(1,1,1),则c点的坐标为_______________ ,设ZnTe的摩尔质量为M,阿伏加德罗常数的值为NA,密度为dg/cm3,则Zn与Te最近距离为___________ nm(列出计算式即可)。
物质 |
|
|
|
|
|
氧化还原电位(E)/V | 0.342 | 0.568 | 0.16 | 小于0.16 | 小于0.16 |
(1)52Te的基态原子的电子排布式为
(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为
 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式(4)电解时为防止除Te以外的单质生成,需控制电位的范围为
 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成(5)将碲与锌一起加热,然后升华可制得碲化锌。碲化锌是一种重要的半导体材料,图甲为它的一种立方晶胞结构,图乙为该晶胞沿z轴投影图。已知a点的坐标为(0,0,0),b点的坐标为(1,1,1),则c点的坐标为
您最近一年使用:0次
7日内更新
|
56次组卷
|
2卷引用:福建省永春一中2023-2024学年高三化学最后一卷试卷
名校
3 . 常温下,下列各组粒子在指定溶液中能大量共存的是
A. 碳酸钠溶液 碳酸钠溶液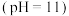 中: 中: 、 、 、 、 |
B.加入苯酚显紫色的溶液中能大量共存的离子: 、 、 、 、 、 、 |
C. 酸性 酸性 溶液中: 溶液中: 、 、 、 、 、 、 |
D.常温下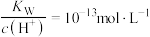 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
4 . 我国明代李时珍《本草纲目》中记载豆腐制作过程:“凡黑豆…皆可为之。水浸,硙碎。滤去渣,煎成。以卤汁或山鞋叶或酸浆醋淀,就釜收之”。制作过程不涉及的操作及现象是
| A.溶解 | B.过滤 | C.聚沉 | D.蒸馏 |
您最近一年使用:0次
名校
5 . 一种具有消炎止痛功效的有机化合物的结构简式如图所示(虚楔形线、实楔形线分别表示共价键由纸平面向内、向外伸展)。下列说法正确的是
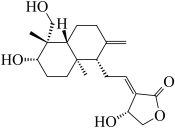
| A.利用质谱仪可测得该分子中官能团的种类有3种 |
| B.该物质可以发生消去反应、取代反应和还原反应 |
| C.该物质的同分异构体中不存在含有酯基、醛基的芳香族化合物 |
| D.1 mol该物质与足量溴的四氯化碳溶液反应,最多可消耗3 mol Br2 |
您最近一年使用:0次
名校
6 . 合成氨反应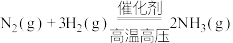 是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:
是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:
(1)合成氨反应在催化作用的化学吸附及初步表面反应历程如下:
①写出N2参与化学吸附的反应方程式:_____________ 。
②以上历程须克服的最大能垒为______ eV。
(2)t℃、0.9MPa的条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体系中气体的含量与时间变化关系如图所示:
______  ,该反应的
,该反应的
______ (用数字表达式表示,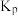 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
②下列叙述能说明该条件下反应达到平衡状态的是______ (填标号)。
a.氨气的体积分数保持不变
b.容器中氢氮比保持不变
c.N2和NH3的平均反应速率之比为1∶2
d.气体密度保持不变
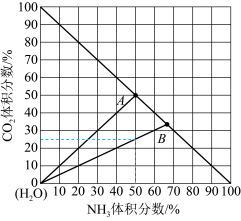
(3)如图是20℃时,NH3-CO2-H2O三元体系相图。纵坐标代表CO2的体积分数,横坐标代表NH3的体积分数,坐标原点代表液态纯水。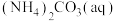 与
与 ,也可选择无水体系反应得到
,也可选择无水体系反应得到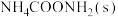 。
。
①20℃时,利用NH3(g)、CO2(g)和H2O(l)制备NH4HCO3(aq)的最佳曲线是______ (填“A-H2O”或“B-H2O”)。
②B点可得到的产品是______ (填化学式)。
(4)钌系催化剂是目前合成氨最先进的催化剂。一种钌的化合物晶胞结构如图。该晶胞中与 等距最近的
等距最近的 有
有______ 个,若该晶胞边长为a pm,该晶体的密度为______  (
(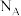 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
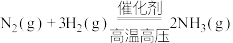 是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:
是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:(1)合成氨反应在催化作用的化学吸附及初步表面反应历程如下:

①写出N2参与化学吸附的反应方程式:
②以上历程须克服的最大能垒为
(2)t℃、0.9MPa的条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体系中气体的含量与时间变化关系如图所示:


 ,该反应的
,该反应的
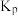 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。②下列叙述能说明该条件下反应达到平衡状态的是
a.氨气的体积分数保持不变
b.容器中氢氮比保持不变
c.N2和NH3的平均反应速率之比为1∶2
d.气体密度保持不变
(3)如图是20℃时,NH3-CO2-H2O三元体系相图。纵坐标代表CO2的体积分数,横坐标代表NH3的体积分数,坐标原点代表液态纯水。
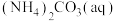 与
与 ,也可选择无水体系反应得到
,也可选择无水体系反应得到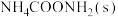 。
。①20℃时,利用NH3(g)、CO2(g)和H2O(l)制备NH4HCO3(aq)的最佳曲线是
②B点可得到的产品是
(4)钌系催化剂是目前合成氨最先进的催化剂。一种钌的化合物晶胞结构如图。该晶胞中与
 等距最近的
等距最近的 有
有 (
(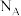 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
名校
7 . “零碳甲醇”是符合“碳中和”属性的绿色能源。请回答下列有关问题。
(1)已知: ;
; ,
, (a>0,b>0)假设该反应的焓变和熵变不随温度的改变而改变,则该反应能自发进行温度范围
(a>0,b>0)假设该反应的焓变和熵变不随温度的改变而改变,则该反应能自发进行温度范围_____ K(用含a、b的代数式表示)。
(2)某温度下,用 溶液吸收一定量的
溶液吸收一定量的 后,
后, ,则该溶液pOH=
,则该溶液pOH=_____ (该温度下 的
的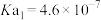 、
、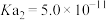 、
、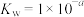 ,用含a的代数式表示)。
,用含a的代数式表示)。
(3)合成甲醇有两种方法。
直接法:
Ⅰ.
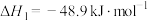
间接法: 和
和 通过逆水煤气反应,先合成CO后,CO和
通过逆水煤气反应,先合成CO后,CO和 再合成甲醇。
再合成甲醇。
Ⅱ.
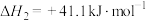
Ⅲ.
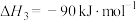
①若利用间接工艺法合成甲醇,反应的决速步为逆水煤气反应,下列示意图中能体现上述反应体系能量变化的是_____ (填字母)。_____ 。
③一定温度、50bar(1bar=100kPa)恒压下,按进料气含a% 、3a%
、3a% (体积分数,杂质气体不反应)合成甲醇,仅发生反应Ⅰ.平衡时二氧化碳转化率为90%,则
(体积分数,杂质气体不反应)合成甲醇,仅发生反应Ⅰ.平衡时二氧化碳转化率为90%,则
_____ bar,反应的平衡常数
_____  (用含a的代数式表示)。
(用含a的代数式表示)。
(4)甲醇、乙醇、正丙醇三种物质在温度传感器尖头处蒸发时的温度变化曲线如图,根据曲线下降的幅度和速率的快慢,可以比较分子间作用力的大小。请判断表示甲醇的曲线是_____ ,理由是_____ 。
(1)已知:
 ;
; ,
, (a>0,b>0)假设该反应的焓变和熵变不随温度的改变而改变,则该反应能自发进行温度范围
(a>0,b>0)假设该反应的焓变和熵变不随温度的改变而改变,则该反应能自发进行温度范围(2)某温度下,用
 溶液吸收一定量的
溶液吸收一定量的 后,
后, ,则该溶液pOH=
,则该溶液pOH= 的
的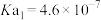 、
、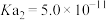 、
、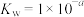 ,用含a的代数式表示)。
,用含a的代数式表示)。(3)合成甲醇有两种方法。
直接法:
Ⅰ.

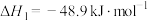
间接法:
 和
和 通过逆水煤气反应,先合成CO后,CO和
通过逆水煤气反应,先合成CO后,CO和 再合成甲醇。
再合成甲醇。Ⅱ.

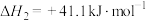
Ⅲ.

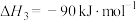
①若利用间接工艺法合成甲醇,反应的决速步为逆水煤气反应,下列示意图中能体现上述反应体系能量变化的是


③一定温度、50bar(1bar=100kPa)恒压下,按进料气含a%
 、3a%
、3a% (体积分数,杂质气体不反应)合成甲醇,仅发生反应Ⅰ.平衡时二氧化碳转化率为90%,则
(体积分数,杂质气体不反应)合成甲醇,仅发生反应Ⅰ.平衡时二氧化碳转化率为90%,则

 (用含a的代数式表示)。
(用含a的代数式表示)。(4)甲醇、乙醇、正丙醇三种物质在温度传感器尖头处蒸发时的温度变化曲线如图,根据曲线下降的幅度和速率的快慢,可以比较分子间作用力的大小。请判断表示甲醇的曲线是

您最近一年使用:0次
名校
8 . 氯化磷酸三钠熔点67℃,常温下较稳定,受热易分解,具有良好的消杀、漂白作用,广泛用于医药、餐饮行业。某小组设计如下流程制备氯化磷酸三钠。下列叙述错误的是
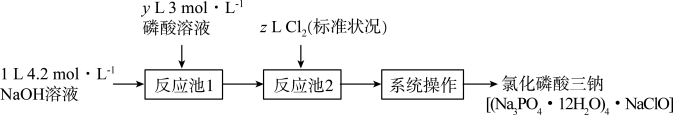
| A.理论上制得的氯化磷酸三钠不超过0.3mol |
B.“反应池1”中最少应加入400mL3 磷酸溶液 磷酸溶液 |
| C.“系列操作”包括蒸发浓缩、降温结晶、过滤、洗涤和高温烘干 |
| D.氧化磷酸三钠因含NaClO而具有消杀、漂白作用 |
您最近一年使用:0次
名校
9 . 高纯镓广泛用于半导体、光电材料等领域。可以利用炼锌渣(主要含ZnO、CuO、 、FeO和一定量的
、FeO和一定量的 、不溶性杂质)为原料制备高纯镓,同时获得ZnS,流程如图所示:
、不溶性杂质)为原料制备高纯镓,同时获得ZnS,流程如图所示:
①电解制取镓时,溶液中的氯离子会影响镓的析出。
②溶液中存在反应: 。
。
③室温时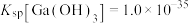 ;
;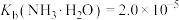 。
。
④黄钠铁矾晶体颗粒大,易沉降易过滤。
(1) 的价层电子排布式为
的价层电子排布式为_____ ,1mol 中含有σ键的物质的量为
中含有σ键的物质的量为_____ 。
(2)黄钠铁矾的化学式为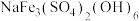 ,写出“沉铁”时的离子方程式
,写出“沉铁”时的离子方程式_____ 。
(3)不采用调节pH的方式沉铁,可能的原因是:①直接调pH沉铁易生成 胶体,不容易过滤;②
胶体,不容易过滤;②_____ ;③_____ 。
(4)“还原除杂”时先向溶液中加入一定量的铜粉,反应一段时间后再向溶液中加入稍过量Zn粉,加入铜粉的目的是_____ 。
(5) 与
与 的各物种的分布分数随pH的变化如图所示。“调节pH=8.2”时,pH不能过高的原因是
的各物种的分布分数随pH的变化如图所示。“调节pH=8.2”时,pH不能过高的原因是_____ 。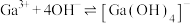 ,
,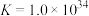 。通过计算探究氨水能否溶解
。通过计算探究氨水能否溶解 ,反应
,反应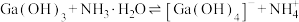 的平衡常数为
的平衡常数为_____ 。
(7)在沉铁前可以加入铁氰化钾检验 是否被完全氧化,若有
是否被完全氧化,若有 则会观察到蓝色沉淀。该蓝色沉淀是一种铁配合物
则会观察到蓝色沉淀。该蓝色沉淀是一种铁配合物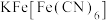 (其摩尔质量为M
(其摩尔质量为M ),其晶胞的
),其晶胞的 如图[
如图[ 未标出,占据四个互不相你的小方体晶胞的
未标出,占据四个互不相你的小方体晶胞的 部分)的体心。若该晶体的密度为
部分)的体心。若该晶体的密度为 ,则
,则 和
和 的最短距离为
的最短距离为_____ cm(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 、FeO和一定量的
、FeO和一定量的 、不溶性杂质)为原料制备高纯镓,同时获得ZnS,流程如图所示:
、不溶性杂质)为原料制备高纯镓,同时获得ZnS,流程如图所示: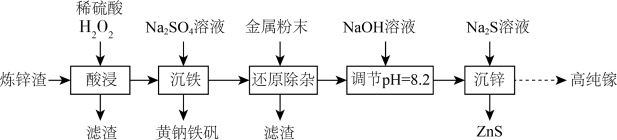
①电解制取镓时,溶液中的氯离子会影响镓的析出。
②溶液中存在反应:
 。
。③室温时
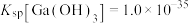 ;
;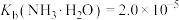 。
。④黄钠铁矾晶体颗粒大,易沉降易过滤。
(1)
 的价层电子排布式为
的价层电子排布式为 中含有σ键的物质的量为
中含有σ键的物质的量为(2)黄钠铁矾的化学式为
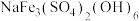 ,写出“沉铁”时的离子方程式
,写出“沉铁”时的离子方程式(3)不采用调节pH的方式沉铁,可能的原因是:①直接调pH沉铁易生成
 胶体,不容易过滤;②
胶体,不容易过滤;②(4)“还原除杂”时先向溶液中加入一定量的铜粉,反应一段时间后再向溶液中加入稍过量Zn粉,加入铜粉的目的是
(5)
 与
与 的各物种的分布分数随pH的变化如图所示。“调节pH=8.2”时,pH不能过高的原因是
的各物种的分布分数随pH的变化如图所示。“调节pH=8.2”时,pH不能过高的原因是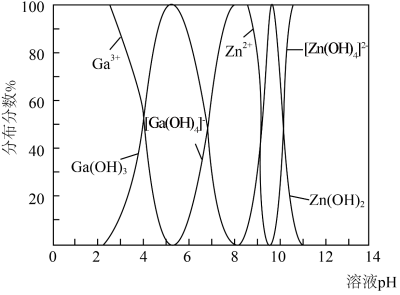
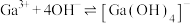 ,
,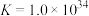 。通过计算探究氨水能否溶解
。通过计算探究氨水能否溶解 ,反应
,反应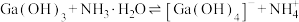 的平衡常数为
的平衡常数为(7)在沉铁前可以加入铁氰化钾检验
 是否被完全氧化,若有
是否被完全氧化,若有 则会观察到蓝色沉淀。该蓝色沉淀是一种铁配合物
则会观察到蓝色沉淀。该蓝色沉淀是一种铁配合物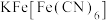 (其摩尔质量为M
(其摩尔质量为M ),其晶胞的
),其晶胞的 如图[
如图[ 未标出,占据四个互不相你的小方体晶胞的
未标出,占据四个互不相你的小方体晶胞的 部分)的体心。若该晶体的密度为
部分)的体心。若该晶体的密度为 ,则
,则 和
和 的最短距离为
的最短距离为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。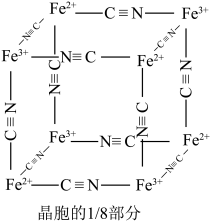
您最近一年使用:0次
名校
10 . 化合物Ⅷ是一种用于制备神经抑制剂的中间体,其合成路线如下:
(1)化合物Ⅰ的分子式是________ 。化合物Ⅷ中的非含氧官能团的名称是________ 。
(2)化合物Ⅰ的沸点高于化合物Ⅱ,其原因是____________ 。
(3)反应①是原子利用率100%的反应,则a为________ 。
(4)反应②的反应类型为________ 。
(5)化合物Ⅲ有多种同分异构体,其中含 结构的有
结构的有________ 种(不计Ⅲ),其中核磁共振氢谱的峰面积比为6∶1∶1的结构简式为________ (写出其中一种)。
(6)写出以 和乙醇为原料合成化合物
和乙醇为原料合成化合物 的单体的合成路线(无机试剂任用)
的单体的合成路线(无机试剂任用)_______________ 。

(1)化合物Ⅰ的分子式是
(2)化合物Ⅰ的沸点高于化合物Ⅱ,其原因是
(3)反应①是原子利用率100%的反应,则a为
(4)反应②的反应类型为
(5)化合物Ⅲ有多种同分异构体,其中含
 结构的有
结构的有(6)写出以
 和乙醇为原料合成化合物
和乙醇为原料合成化合物 的单体的合成路线(无机试剂任用)
的单体的合成路线(无机试剂任用)
您最近一年使用:0次