名校
解题方法
1 . 某实验小组探究过量甲醛与新制氢氧化铜的反应。
提出猜想:
已知:ⅰ.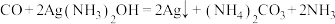
ⅱ.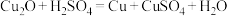
下列说法不正确 的是
提出猜想:

已知:ⅰ.
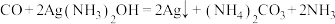
ⅱ.

实验步骤 | 实验装置及内容 | 实验现象 |
步骤1 | 如上图装置 | 反应结束后,A中生成红色固体,C无明显变化 |
步骤2 | 将A中混合物过滤,洗涤所得固体,取少量固体于试管中,加入稀硫酸,振荡 | 无明显现象 |
步骤3 | 取步骤2中的滤液于试管中,加入足量稀盐酸 | 无明显现象 |
A.配制银氨溶液时,应向稀 溶液中加入稀氨水,至产生的沉淀恰好溶解 溶液中加入稀氨水,至产生的沉淀恰好溶解 |
B.步骤3目的是检验反应后溶液中是否存在 |
| C.装置B的主要作用是除去挥发的甲酸,防止干扰CO的检验 |
D.该实验中,过量甲醛与新制氢氧化铜可能发生的反应为: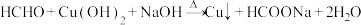 |
您最近一年使用:0次
昨日更新
|
165次组卷
|
3卷引用:北京市东直门中学2023-2024学年高三下学期开学考化学试卷
2 . “高山流水觅知音”。下列中国古乐器中,主要由硅酸盐材料制成的是
|
|
| A.九霄环佩木古琴 | B.裴李岗文化骨笛 |
|
|
| C.商朝后期陶埙 | D.曾侯乙青铜编钟 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 用高分子吸附树脂提取卤水中的碘(主要以 形式存在)的工艺流程如下:
形式存在)的工艺流程如下:
 形式存在)的工艺流程如下:
形式存在)的工艺流程如下: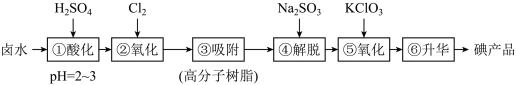
A.经①和④所得溶液中,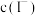 后者小于前者 后者小于前者 |
| B.④的作用是将吸附的碘还原而脱离高分子树脂 |
C.若②和⑤中分别得到等量 ,则消耗的 ,则消耗的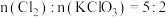 |
| D.由⑥能得到碘产品是因为碘分子为极性分子,与溶液中的其他微粒间的作用力较弱 |
您最近一年使用:0次
7日内更新
|
86次组卷
|
3卷引用:北京市海淀区第一零一中学2023-2024学年高三下学期三模化学试题
北京市海淀区第一零一中学2023-2024学年高三下学期三模化学试题 北京市第一○一中学2023-2024学年高三下学期三模化学 试题(已下线)第05讲 氧化还原反应方程式的配平、书写及计算(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
4 . 金属铁(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产铁的方法之一是将金红石( )转化为
)转化为 ,再进一步还原得到铁。
,再进一步还原得到铁。 转化为
转化为 有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式如下:
有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式如下:
(ⅰ)直接氯化:

(ⅱ)碳氯化: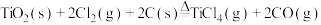
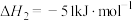
在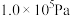 ,将
,将 、C、
、C、 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
 )转化为
)转化为 ,再进一步还原得到铁。
,再进一步还原得到铁。 转化为
转化为 有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式如下:
有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式如下:(ⅰ)直接氯化:


(ⅱ)碳氯化:
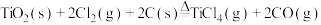
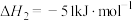
在
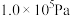 ,将
,将 、C、
、C、 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。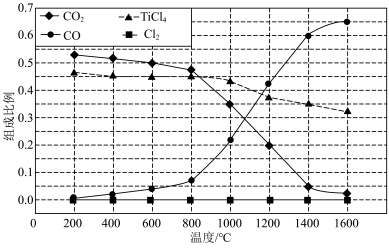
A.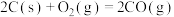 为吸热反应 为吸热反应 |
B.反应 的 的 |
C.随温度升高,1400℃时 在平衡混合物中的比例下降,主要原因是碳氯化反应为放热反应,随温度升高平衡常数减小,反应程度降低 在平衡混合物中的比例下降,主要原因是碳氯化反应为放热反应,随温度升高平衡常数减小,反应程度降低 |
| D.综合考虑反应速率和平衡,进行碳氯化反应合适的生产温度为1000~1200℃之间 |
您最近一年使用:0次
名校
5 . 在恒温恒容密闭容器中充入一定量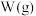 ,发生如下反应:
,发生如下反应: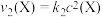 和
和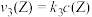 ,其中
,其中 、
、 分别为反应②和③的速率常数,反应③的活化能大于反应②。测得
分别为反应②和③的速率常数,反应③的活化能大于反应②。测得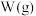 的浓度随时间的变化如下表。
的浓度随时间的变化如下表。
下列说法正确的是
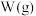 ,发生如下反应:
,发生如下反应: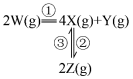
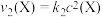 和
和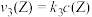 ,其中
,其中 、
、 分别为反应②和③的速率常数,反应③的活化能大于反应②。测得
分别为反应②和③的速率常数,反应③的活化能大于反应②。测得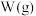 的浓度随时间的变化如下表。
的浓度随时间的变化如下表。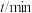 | 0 | 1 | 2 | 3 | 4 | 5 |
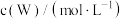 | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 | 0.028 |
A.0~2min内,W的平均反应速率为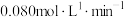 |
| B.若增大容器容积,平衡时Z的产率增大 |
C.若 ,平衡时 ,平衡时 |
D.若升高温度,平衡时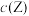 减小 减小 |
您最近一年使用:0次
2024-06-14更新
|
116次组卷
|
2卷引用:北京市第二中学2023-2024学年高三下学期三模化学试题
名校
解题方法
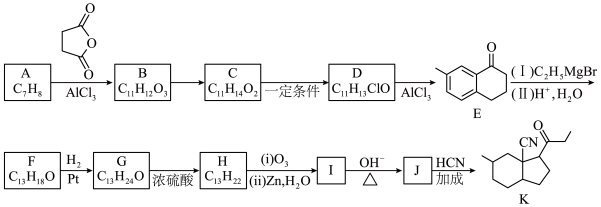
6 . 有机物K是药物合成中间体,其合成路线如下:_______ ,B的官能团是_______ 。
(2)C的结构简式是_______ 。
(3)下列关于E、F说法正确的是_______ 。
A.E、F都存在遇 显紫色的同分异构体
显紫色的同分异构体
B.核磁共振氢谱和红外光谱能区分E和F
C.在加热和Cu催化条件下,F能被氧气氧化
(4)写出G→H的化学方程式_______ 。
(5)I→J的过程中还可能生成两种副产物,与J互为同分异构体,写出一种副产物的结构简式_______ 。
(6)由K合成化合物P_______ 。
②综合分析合成过程,K→Q的目的是_______ 。
已知:ⅰ.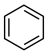
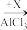
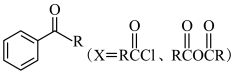 。
。
ⅱ.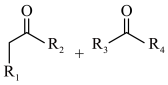

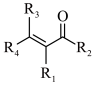 。
。
ⅲ.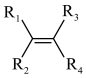

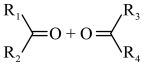 。
。
(2)C的结构简式是
(3)下列关于E、F说法正确的是
A.E、F都存在遇
 显紫色的同分异构体
显紫色的同分异构体B.核磁共振氢谱和红外光谱能区分E和F
C.在加热和Cu催化条件下,F能被氧气氧化
(4)写出G→H的化学方程式
(5)I→J的过程中还可能生成两种副产物,与J互为同分异构体,写出一种副产物的结构简式
(6)由K合成化合物P
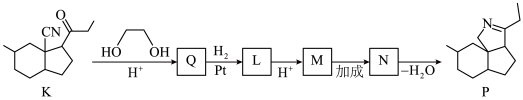
已知: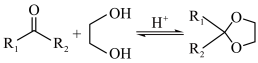
②综合分析合成过程,K→Q的目的是
您最近一年使用:0次
7 . 某小组同学探究高铁酸钾(K2FeO4)的制备条件及性质。
资料:K2FeO4为紫色固体,有强氧化性,酸性条件下分解放出气体,微溶于KOH溶液。
Ⅰ:K2FeO4的制备(夹持和加热装置已略)___________ 。
(2)C中得到紫色固体和紫色溶液,写出C中Cl2发生的反应: 和
和___________ 。
(3)实验表明:C中 和KOH的用量对K2FeO4的产率有影响。
和KOH的用量对K2FeO4的产率有影响。
注:上述实验中,溶液总体积、 的物质的量、Cl2的通入量均相同。
的物质的量、Cl2的通入量均相同。
结合电极反应式,分析实验ⅰ和实验ⅱ现象不同的原因可能是___________ 。
Ⅱ:探究K2FeO4的性质
实验ⅲ:取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a。
取少量a,滴加KSCN溶液至过量,溶液呈红色。
(4)根据气体中有Cl2生成,得出:氧化性K2FeO4>Cl2,是否合理?理由是___________ 。
(5)a溶液变红可知a中含有 离子,但该离子的产生不能判断一定是K2FeO4将
离子,但该离子的产生不能判断一定是K2FeO4将 氧化,还可能由
氧化,还可能由___________ 产生(用离子方程式表示)。
(6)实验ⅳ:用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量b,滴加盐酸,有Cl2产生。该方案可证明K2FeO4氧化了 。用KOH溶液洗涤的目的是
。用KOH溶液洗涤的目的是___________ 。
(7)实验反思
①实验一中装置B的作用是___________ 。
②实验一中得到紫色溶液后,持续通入Cl2,观察到溶液紫色变浅。解释可能原因___________ 。
资料:K2FeO4为紫色固体,有强氧化性,酸性条件下分解放出气体,微溶于KOH溶液。
Ⅰ:K2FeO4的制备(夹持和加热装置已略)
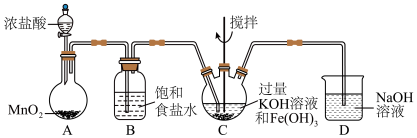
(2)C中得到紫色固体和紫色溶液,写出C中Cl2发生的反应:
 和
和(3)实验表明:C中
 和KOH的用量对K2FeO4的产率有影响。
和KOH的用量对K2FeO4的产率有影响。| 实验序号 | 试剂 | C中实验现象 |
| ⅰ |  和少量KOH 和少量KOH | 无明显现象 |
| ⅱ |  和过量KOH 和过量KOH | 得到紫色溶液和紫色固体 |
 的物质的量、Cl2的通入量均相同。
的物质的量、Cl2的通入量均相同。结合电极反应式,分析实验ⅰ和实验ⅱ现象不同的原因可能是
Ⅱ:探究K2FeO4的性质
实验ⅲ:取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a。
取少量a,滴加KSCN溶液至过量,溶液呈红色。
(4)根据气体中有Cl2生成,得出:氧化性K2FeO4>Cl2,是否合理?理由是
(5)a溶液变红可知a中含有
 离子,但该离子的产生不能判断一定是K2FeO4将
离子,但该离子的产生不能判断一定是K2FeO4将 氧化,还可能由
氧化,还可能由(6)实验ⅳ:用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量b,滴加盐酸,有Cl2产生。该方案可证明K2FeO4氧化了
 。用KOH溶液洗涤的目的是
。用KOH溶液洗涤的目的是(7)实验反思
①实验一中装置B的作用是
②实验一中得到紫色溶液后,持续通入Cl2,观察到溶液紫色变浅。解释可能原因
您最近一年使用:0次
名校
8 . 下列化学用语或模型正确的是
A. 的电子式: 的电子式: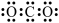 |
B. 的空间结构: 的空间结构: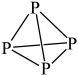 |
C. 的结构示意图: 的结构示意图: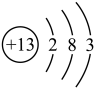 |
D. 的空间填充模型: 的空间填充模型: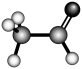 |
您最近一年使用:0次
名校
解题方法
9 . 探究草酸(H2C2O4)性质,进行如下实验。
已知:室温下,H2C2O4的 ,
,
H2CO3的 ,
,
由上述实验所得草酸性质所对应的方程式不正确 的是
| 实验 | 装置 | 试剂a | 现象 |
| ① |
|  溶液(含酚酞) 溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
| ② | 足量NaHCO3溶液 | 产生气泡 | |
| ③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
| ④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
 ,
,
H2CO3的
 ,
,
由上述实验所得草酸性质所对应的方程式
A.H2C2O4有酸性,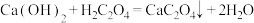 |
B.酸性: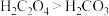 , , |
C.H2C2O4有还原性, |
D.H2C2O4可发生酯化反应, |
您最近一年使用:0次
名校
解题方法
10 . 下列生活中的现象与物质结构关联不正确 的是
|
|
|
|
| A | B | C | D |
| A.激光的产生与电子跃迁有关 |
| B.橡胶老化与碳碳双键有关 |
| C.植物油加氢制硬化油与植物油中含有酯基有关 |
| D.金属可加工成各种形状与金属键有关 |
您最近一年使用:0次