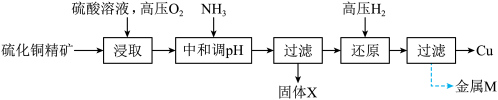
1 . 高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为主要原料制备铜粉的工艺流程如下: 时认为该离子已沉淀完全。可能用到的数据见下表:
时认为该离子已沉淀完全。可能用到的数据见下表:
(1)“浸取”时使用高压O2的优点是_______ ;“浸取”过程有黄色沉淀生成,CuS在“浸取”中发生反应的离子方程式为_______ 。
(2)“中和调pH”需调节pH的范围为_______ 。
(3)固体X的主要成分是_______ 。
(4)还原时,溶液酸性过强不利于Cu的生成,从平衡移动的角度解释原因_______ 。
(5)室温下,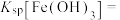
_______ 。
(6)工业上对硫化铜精矿的处理有很多方法,相比于高压氢还原法的“浸取”步骤,在空气中高温焙烧最大的缺点是_______ 。
 时认为该离子已沉淀完全。可能用到的数据见下表:
时认为该离子已沉淀完全。可能用到的数据见下表: |  |  | |
| 开始沉淀pH | 1.9 | 4.2 | 6.2 |
| 沉淀完全pH | 2.7 | 6.7 | 8.2 |
(1)“浸取”时使用高压O2的优点是
(2)“中和调pH”需调节pH的范围为
(3)固体X的主要成分是
(4)还原时,溶液酸性过强不利于Cu的生成,从平衡移动的角度解释原因
(5)室温下,
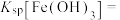
(6)工业上对硫化铜精矿的处理有很多方法,相比于高压氢还原法的“浸取”步骤,在空气中高温焙烧最大的缺点是
您最近一年使用:0次
2 . CO2捕获和转化可减少CO2排放,其原理如图1所示。反应①完成之后,以N2为载气,将CH4以恒定流速通入反应器,单位时间内流出气体中各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到CO2,在催化剂上检测到有积炭。

A. 之后,生成CO的速率为0,是因为反应②不再发生 之后,生成CO的速率为0,是因为反应②不再发生 |
B. 时刻,副反应生成H2的速率大于反应②生成H2的速率 时刻,副反应生成H2的速率大于反应②生成H2的速率 |
C.CaO、CaCO3可循环利用,反应②为 |
D.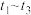 , , 比 比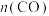 多,且生成的H2速率不变,推测有副反应 多,且生成的H2速率不变,推测有副反应 |
您最近一年使用:0次
3 . 实验测得浓度均为 的
的 溶液和
溶液和 溶液的pH随温度的变化情况如图所示。下列说法正确的是
溶液的pH随温度的变化情况如图所示。下列说法正确的是
 的
的 溶液和
溶液和 溶液的pH随温度的变化情况如图所示。下列说法正确的是
溶液的pH随温度的变化情况如图所示。下列说法正确的是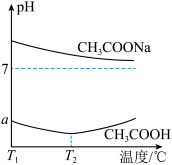
A. 时, 时, 的电离平衡常数约为 的电离平衡常数约为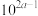 |
B.升高温度, 溶液中 溶液中 增大,pH减小 增大,pH减小 |
C.两溶液等体积混合后的溶液中,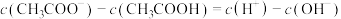 |
D.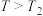 后, 后, 溶液的pH随温度升高而增大的原因可能是水电离的 溶液的pH随温度升高而增大的原因可能是水电离的 增大 增大 |
您最近一年使用:0次
解题方法
4 . 向恒容密闭容器中加入1mol 和一定量
和一定量 ,发生反应:
,发生反应: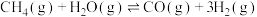 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比 [
[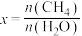 ]随温度的变化曲线如图所示。下列说法正确的是
]随温度的变化曲线如图所示。下列说法正确的是
 和一定量
和一定量 ,发生反应:
,发生反应: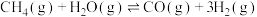 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比 [
[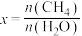 ]随温度的变化曲线如图所示。下列说法正确的是
]随温度的变化曲线如图所示。下列说法正确的是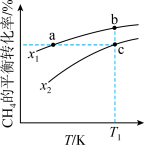
A. |
B.点a、c对应的 的转化率:a>c 的转化率:a>c |
| C.点a、b对应的平均相对分子质量:a>b |
D.点a、b、c对应的平衡常数: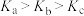 |
您最近一年使用:0次
解题方法
5 . 某低成本储能电池原理如图所示。下列说法正确的是
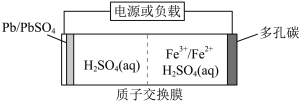
| A.充电时右侧溶液pH不变 |
B.充电时的总反应为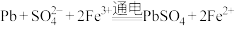 |
| C.放电时电子由铅电极经质子交换膜移向多孔碳电极 |
| D.放电时电路中每转移1mol电子,左侧溶液质量减少49g |
您最近一年使用:0次
解题方法
6 . 下列离子方程式正确的是
A. 水解: 水解: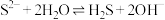 |
B.用惰性电极电解氯化镁溶液: |
C.过量 通入NaClO溶液中: 通入NaClO溶液中: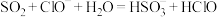 |
D. 通入氨盐水中制 通入氨盐水中制 : :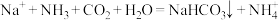 |
您最近一年使用:0次
7 . 锅炉水垢中含有的 常用
常用 溶液浸泡一段时间,放出浸泡液,再用稀盐酸处理。下列说法错误的是[已知
溶液浸泡一段时间,放出浸泡液,再用稀盐酸处理。下列说法错误的是[已知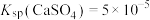 ,
,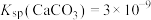 ]
]
 常用
常用 溶液浸泡一段时间,放出浸泡液,再用稀盐酸处理。下列说法错误的是[已知
溶液浸泡一段时间,放出浸泡液,再用稀盐酸处理。下列说法错误的是[已知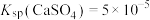 ,
,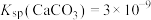 ]
]A.放出的浸泡液中存在 |
| B.将稀盐酸换成同浓度稀硫酸达不到除水垢的目的 |
C.使用 溶液浸泡的过程中,浸泡液pH下降 溶液浸泡的过程中,浸泡液pH下降 |
D. 转化为 转化为 的过程中, 的过程中,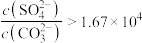 |
您最近一年使用:0次
8 . 一定温度下,在容积为2L的密闭容器中加入固体 ,发生反应:
,发生反应: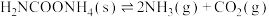
 ,若0~10s内消耗了2mol
,若0~10s内消耗了2mol ,下列说法正确的是
,下列说法正确的是
 ,发生反应:
,发生反应: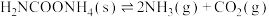
 ,若0~10s内消耗了2mol
,若0~10s内消耗了2mol ,下列说法正确的是
,下列说法正确的是A.0~10s内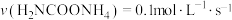 |
B.反应过程中 气体的体积分数均为1/3 气体的体积分数均为1/3 |
| C.升高温度正反应速率加快,逆反应速率减慢 |
D.压缩容器体积,再次达平衡后 增大 增大 |
您最近一年使用:0次
解题方法
9 . 下列事实不能用平衡移动原理解释的是
| A.石灰岩经过千百万年的积聚形成钟乳石、石笋 |
| B.实验室用饱和食盐水除去氯气中混有的少量氯化氢 |
C.工业生产硫酸的过程中使用过量空气以提高 的转化率 的转化率 |
D.反应 达平衡后,加压使混合气体颜色变深 达平衡后,加压使混合气体颜色变深 |
您最近一年使用:0次
10 . 下列实验装置或操作能达到实验目的的是
|
|
| 电解精炼铜 | 测定NaClO溶液的pH |
|
|
| 探究浓度对化学反应速率的影响 | 蒸发 溶液制 溶液制 固体 固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次