名校
1 . 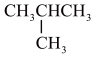 的一氯代物有
的一氯代物有 多一个碳原子的烷烃有
多一个碳原子的烷烃有
您最近一年使用:0次
名校
解题方法
2 . 甲烷燃料电池采用可传导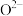 的固体氧化物为电解质,其工作原理如图所示:
的固体氧化物为电解质,其工作原理如图所示:
(2)若该燃料电池工作时消耗空气5.6L(标准状况。假设空气中 体积分数为20%),则理论上需通入甲烷
体积分数为20%),则理论上需通入甲烷_______ mol。
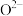 的固体氧化物为电解质,其工作原理如图所示:
的固体氧化物为电解质,其工作原理如图所示:
| A.a极→固体电解质→b极 | B.b极→固体电解质→a极。 |
| C.a极→用电器→b极 | D.b极→用电器→a极 |
(2)若该燃料电池工作时消耗空气5.6L(标准状况。假设空气中
 体积分数为20%),则理论上需通入甲烷
体积分数为20%),则理论上需通入甲烷
您最近一年使用:0次
名校
3 . 乙烯合成PE(聚乙烯)的化学方程式为_______ ,该反应类型属于_______ 。
您最近一年使用:0次
4 . 回答下列问题。
(1)鉴别甲烷和乙烯的方法是_______ ;
(2)除去甲烷中乙烯的方法是_______。
(1)鉴别甲烷和乙烯的方法是
(2)除去甲烷中乙烯的方法是_______。
| A.气体通入盛水的洗气瓶 |
| B.气体通入盛溴水的洗气瓶 |
| C.气体通入盛酸性高锰酸钾溶液的洗气瓶 |
| D.气体通入氢氧化钠溶液的洗气瓶 |
您最近一年使用:0次
5 . 请回答:
(1)硫酸铝的化学式___________ 。
(2) 的电子式
的电子式___________ 。
(3) 溶液中滴加
溶液中滴加 溶液,产生
溶液,产生___________ 色溶液。
(4)以 溶液作“腐蚀剂”制作铜电路板的化学反应方程式
溶液作“腐蚀剂”制作铜电路板的化学反应方程式___________ 。
(1)硫酸铝的化学式
(2)
 的电子式
的电子式(3)
 溶液中滴加
溶液中滴加 溶液,产生
溶液,产生(4)以
 溶液作“腐蚀剂”制作铜电路板的化学反应方程式
溶液作“腐蚀剂”制作铜电路板的化学反应方程式
您最近一年使用:0次
名校
6 . 回答下列问题
(1)写出下列物质的分子式①含有18个氢原子的链状烷烃___________ ;
②含有6个碳原子的单环烷烃___________ ;
(2)用系统命名法命名下列有机化合物___________ 。
(4)画出下列烷烃的键线式
2,5-二甲基-3-乙基庚烷___________ ;1,1,4-三甲基环己烷___________ 。
(1)写出下列物质的分子式①含有18个氢原子的链状烷烃
②含有6个碳原子的单环烷烃
(2)用系统命名法命名下列有机化合物

(4)画出下列烷烃的键线式
2,5-二甲基-3-乙基庚烷
您最近一年使用:0次
7 . Ⅰ.已知:反应aA(g)+bB(g) cC(g),某温度下,在2L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示。___________ ,则该反应的化学方程式为___________ 。
(2)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,反应相同时间后,测得三个容器中的反应速率分别为:甲中:v(A)=0.3mol·L-1·s-1,乙中:v(B)=0.12mol·L-1·s-1,丙中:v(C)=9.6mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为___________ 。
(3)下列条件的改变能加快上述反应的反应速率的是___________ 。
①升高温度 ②保持压强不变,充入He
③保持体积不变,充入He ④增加A的浓度
Ⅱ.同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
(4)本实验待测数据可以是___________ ,实验Ⅰ和实验Ⅱ可以探究___________ 对锌与稀硫酸反应速率的影响。
(5)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中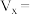
___________ 。
 cC(g),某温度下,在2L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示。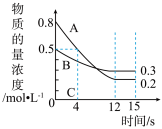
(2)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,反应相同时间后,测得三个容器中的反应速率分别为:甲中:v(A)=0.3mol·L-1·s-1,乙中:v(B)=0.12mol·L-1·s-1,丙中:v(C)=9.6mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为
(3)下列条件的改变能加快上述反应的反应速率的是
①升高温度 ②保持压强不变,充入He
③保持体积不变,充入He ④增加A的浓度
Ⅱ.同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
| 序号 | 纯锌粉/g |  硫酸溶液/mL 硫酸溶液/mL | 温度/℃ | 硫酸铜固体/g | 加入蒸馏水/mL |
| Ⅰ | 2.0 | 50.0 | 25 | 0 | 0 |
| Ⅱ | 2.0 | 40.0 | 25 | 0 | 10.0 |
| Ⅲ | 2.0 | 50.0 | 25 | 0.2 | 0 |
| Ⅳ | 2.0 | 50.0 | 25 | 4.0 | 0 |
(4)本实验待测数据可以是
(5)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积V/mL | ||||
 溶液 溶液 | 水 | KI溶液 |  溶液 溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | 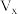 | 4.0 | 4.0 | 2.0 |
您最近一年使用:0次
名校
解题方法
8 . 有机化合物R为无色粘性液体,易溶于水,可由葡萄糖发酵制得。
(1)化合物 的质谱图如图-1所示(图中最右侧的峰表示
的质谱图如图-1所示(图中最右侧的峰表示 所形成的分子离子峰,其质荷比的数值就是
所形成的分子离子峰,其质荷比的数值就是 的相对分子质量)
的相对分子质量)
将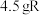 在足量
在足量 中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现二者分别增重
中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现二者分别增重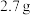 和
和 ,则R的分子式为
,则R的分子式为________ 。
(2)对 进行红外光谱分析,含有官能团
进行红外光谱分析,含有官能团 和
和 ,R的核磁共振氢谱图如图2所示,则R中含有
,R的核磁共振氢谱图如图2所示,则R中含有________ 种氢原子,R的结构简式为________ 。
(3)R在催化剂、加热的条件下发生聚合反应,制得可降解塑料PLA,写出该反应的化学方程式________ 。
(4)某烃的结构如图3所示,若每两个碳原子之间均插入一个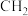 原子团,可以形成金刚烷的结构,金刚烷的分子式为
原子团,可以形成金刚烷的结构,金刚烷的分子式为________ ,其一氯代物有________ 种。
(5)聚碳酸酯(结构如图4)的透光率良好,它可制作车、船、飞机的挡风玻璃,以及眼镜片、光盘、唱片等。它可用绿色化学原料碳酸二甲酯(结构如图5)与另一种原料M在一定条件下反应制得,同时生成甲醇。M的结构简式为________ 。
(1)化合物
 的质谱图如图-1所示(图中最右侧的峰表示
的质谱图如图-1所示(图中最右侧的峰表示 所形成的分子离子峰,其质荷比的数值就是
所形成的分子离子峰,其质荷比的数值就是 的相对分子质量)
的相对分子质量)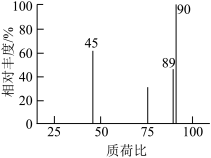
将
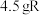 在足量
在足量 中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现二者分别增重
中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现二者分别增重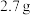 和
和 ,则R的分子式为
,则R的分子式为(2)对
 进行红外光谱分析,含有官能团
进行红外光谱分析,含有官能团 和
和 ,R的核磁共振氢谱图如图2所示,则R中含有
,R的核磁共振氢谱图如图2所示,则R中含有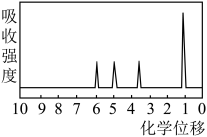
(3)R在催化剂、加热的条件下发生聚合反应,制得可降解塑料PLA,写出该反应的化学方程式
(4)某烃的结构如图3所示,若每两个碳原子之间均插入一个
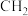 原子团,可以形成金刚烷的结构,金刚烷的分子式为
原子团,可以形成金刚烷的结构,金刚烷的分子式为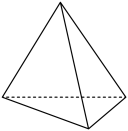
(5)聚碳酸酯(结构如图4)的透光率良好,它可制作车、船、飞机的挡风玻璃,以及眼镜片、光盘、唱片等。它可用绿色化学原料碳酸二甲酯(结构如图5)与另一种原料M在一定条件下反应制得,同时生成甲醇。M的结构简式为

您最近一年使用:0次
解题方法
9 . 绿芦笋中含有天门冬氨酸(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。回答下列问题:_______ (填“σ键”、“π键”),其中N原子的杂化轨道类型为_______ ,图中O—C—C的键角_______ C—C—N的键角(填“大于”或“小于”)。
(2)H2S和H2Se热稳定性较好的是_______ ,从分子结构角度解释其原因:_______ 。
(3)四个主族元素部分简单氢化物沸点随周期序数的变化如图1所示,某些氢键的键能和键长如表。其中表示第VIA族元素简单氢化物沸点变化的是图中曲线_______ (填字母),甲醇、乙醇易溶于水的原因是_______ ,O−H∙∙∙O的键能小于F−H∙∙∙F,但水的沸点高于HF的原因可能是_______ 。

(2)H2S和H2Se热稳定性较好的是
(3)四个主族元素部分简单氢化物沸点随周期序数的变化如图1所示,某些氢键的键能和键长如表。其中表示第VIA族元素简单氢化物沸点变化的是图中曲线

| 氢键X−H∙∙∙Y | 键能/(kJ·mol-1) | 键长/pm | 代表性例子 |
| F−H∙∙∙F | 28.1 | 255 | (HF)n |
| O−H∙∙∙O | 18.8 | 276 | 冰 |
| O−H∙∙∙O | 25.9 | 266 | 甲醇,乙醇 |
| N−H∙∙∙F | 20.9 | 268 | NH4F |
| N−H∙∙∙O | 20.9 | 286 | CH3CONH2 |
| N−H∙∙∙N | 5.4 | 338 | NH3 |
您最近一年使用:0次
名校
10 . 化学材料已经在人们的生活中扮演着不可替代的角色。比如:①镓、锗是重要的半导体材料。②新型碳化硅(SiC)增强铝基复合材料、碳纳米管(一种同轴管状结构的碳原子簇,是纳米级石墨晶体)、石墨炔都是近年来合成的新材料。
(1)与镓同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为___________ 。
(2)与镓同族的铝元素形成的化合物 具有较高的熔点(1040℃),而
具有较高的熔点(1040℃),而 在178℃时升华,原因是
在178℃时升华,原因是___________ 。
(3)二氧化碳的电子式为___________ 。
(4)列举一个事实说明C和Si的非金属性强弱___________ 。
(5)新型碳化硅增强铝基复合材料曾助力“天问一号”成功探火,它不具有的性质是:___________。
(6)下图几种碳单质中,属于共价晶体的是___________ , 晶体中构成物质的微粒间的作用力是
晶体中构成物质的微粒间的作用力是___________ 。
(1)与镓同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为
(2)与镓同族的铝元素形成的化合物
 具有较高的熔点(1040℃),而
具有较高的熔点(1040℃),而 在178℃时升华,原因是
在178℃时升华,原因是(3)二氧化碳的电子式为
(4)列举一个事实说明C和Si的非金属性强弱
(5)新型碳化硅增强铝基复合材料曾助力“天问一号”成功探火,它不具有的性质是:___________。
| A.耐高温 | B.密度大 | C.耐腐蚀 | D.抗磨损 |
(6)下图几种碳单质中,属于共价晶体的是
 晶体中构成物质的微粒间的作用力是
晶体中构成物质的微粒间的作用力是
您最近一年使用:0次



