1 . 请回答:
(1)NH3的电子式是_______ ;乙醛的结构简式_______ 。
(2)向银氨溶液中加入葡萄糖,水浴加热,试管内壁可观察到的现象是_______ 。
(3)工业上用氨的催化氧化法制硝酸。请写出氨气与氧气在催化剂加热条件下的化学方程式_______ 。
(1)NH3的电子式是
(2)向银氨溶液中加入葡萄糖,水浴加热,试管内壁可观察到的现象是
(3)工业上用氨的催化氧化法制硝酸。请写出氨气与氧气在催化剂加热条件下的化学方程式
您最近一年使用:0次
2 . 从下列六种有机物中选择合适的物质,将其标号填在空格上。
A.蛋白质 B.乙醇 C.乙酸
(1)具有酸味,可用做调味剂的是_____
(2)检测是否“酒驾”时,检测的是驾驶者血液里_____ 的含量。
(3)_____ 水解的最终产物是氨基酸。
A.蛋白质 B.乙醇 C.乙酸
(1)具有酸味,可用做调味剂的是
(2)检测是否“酒驾”时,检测的是驾驶者血液里
(3)
您最近一年使用:0次
解题方法
3 . 填空
(1)钠有多种化合物,其中俗称“小苏打”,是发酵粉的主要成分,可用作治疗胃酸过多的物质是_____ (填“ ”或“
”或“ ”);
”);
(2)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是_____ ,(填“ ”、“
”、“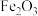 ”或“
”或“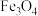 ”);
”);
(3)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装_____ (填“浓硫酸”或“浓盐酸”)。
(1)钠有多种化合物,其中俗称“小苏打”,是发酵粉的主要成分,可用作治疗胃酸过多的物质是
 ”或“
”或“ ”);
”);(2)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是
 ”、“
”、“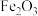 ”或“
”或“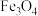 ”);
”);(3)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装
您最近一年使用:0次
解题方法
4 . 元素在元素周期表中的位置,反映了元素的原子结构和元素的性质,如下图所示是短周期元素在周期表中的位置。
请回答以下问题:
(1)碳元素在元素周期表中的位置为___________ ,第三周期ⅥA族的元素是___________ (写元素名称)。
(2)根据元素周期律,请判断下列关系:
①酸性强弱:H3PO4___________ (填“>”或“<”)HNO3;
②稳定性强弱:H2O___________ (填“>”或“<”)H2S;
③离子半径大小关系:O2-___________ (填“>”或“<”)Mg2+。
(3)元素甲的原子是第三周期中半径最大的,该元素的核外电子排布示意图为___________ ,甲的单质与水反应的离子方程式___________ 。
(4)标准状况下,22.4 LCl2的物质的量为___________ mol,质量为___________ g,含有的原子总数为___________ (用NA表示阿伏加德罗常数的数值)。
| 周期 | ⅠA | 0 | ||||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | He | ||
| 2 | Li | Be | B | C | N | O | F | Ne | ||
| 3 | Na | Mg | …… | Al | Si | P | S | Cl | Ar | |
(1)碳元素在元素周期表中的位置为
(2)根据元素周期律,请判断下列关系:
①酸性强弱:H3PO4
②稳定性强弱:H2O
③离子半径大小关系:O2-
(3)元素甲的原子是第三周期中半径最大的,该元素的核外电子排布示意图为
(4)标准状况下,22.4 LCl2的物质的量为
您最近一年使用:0次
5 . 采用电还原处理工业尾气,可将尾气中的 转化为重要的化工原料
转化为重要的化工原料 。某种处理工艺的主要过程:用
。某种处理工艺的主要过程:用 溶液吸收含
溶液吸收含 的工业尾气,
的工业尾气, 转化为
转化为 ;将
;将 溶液移入电解槽中电解,得到
溶液移入电解槽中电解,得到 。
。
(1) 的电离方程式为
的电离方程式为_____ 。
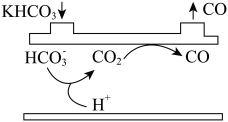
(2)电解槽的局部示意图如图。 转化为
转化为 过程,
过程, 发生
发生_____ 反应(填“氧化”或“还原”)。
②电解槽内生成 的离子方程式为
的离子方程式为_____ 。
(3)电还原处理工业尾气实现 转化为
转化为 的意义:
的意义:_____ (填一点即可)。
 转化为重要的化工原料
转化为重要的化工原料 。某种处理工艺的主要过程:用
。某种处理工艺的主要过程:用 溶液吸收含
溶液吸收含 的工业尾气,
的工业尾气, 转化为
转化为 ;将
;将 溶液移入电解槽中电解,得到
溶液移入电解槽中电解,得到 。
。(1)
 的电离方程式为
的电离方程式为(2)电解槽的局部示意图如图。
 转化为
转化为 过程,
过程, 发生
发生②电解槽内生成
 的离子方程式为
的离子方程式为(3)电还原处理工业尾气实现
 转化为
转化为 的意义:
的意义:
您最近一年使用:0次
6 . 化学家研究有机化合物的组成、结构、性质及合成,并将研究成果应用于实践,使我们的生活变得越来越美好。选择合适的物质,将其标号填在横线上。
A. B.
B. C.
C. D.
D. E.葡萄糖 F.淀粉 G.蛋白质 H.油脂
E.葡萄糖 F.淀粉 G.蛋白质 H.油脂
(1)分子空间构型为正四面体的是_____ 。
(2)遇碘水变蓝的是_____ 。
(3)可作为食品酸味调味剂的是_____ 。
(4)水解最终产物为氨基酸的是_____ 。
(5)医疗上常用作消毒剂的是_____ 。
(6)人体血液里的血糖,通常指血液中的_____ 。
(7)用于合成聚乙烯塑料的是_____ 。
(8)工业上可用于生产肥皂的原料是_____ 。
A.
 B.
B. C.
C. D.
D. E.葡萄糖 F.淀粉 G.蛋白质 H.油脂
E.葡萄糖 F.淀粉 G.蛋白质 H.油脂(1)分子空间构型为正四面体的是
(2)遇碘水变蓝的是
(3)可作为食品酸味调味剂的是
(4)水解最终产物为氨基酸的是
(5)医疗上常用作消毒剂的是
(6)人体血液里的血糖,通常指血液中的
(7)用于合成聚乙烯塑料的是
(8)工业上可用于生产肥皂的原料是
您最近一年使用:0次
解题方法
7 . 元素周期表是学习和研究化学科学的重要工具。下表是元素周期表的一部分(a、b表示两种元素),按要求作答。
(1)a位于周期表中第_____ 周期_____ 族。
(2)b的元素符号是_____ ,其最高化合价是_____ 。
(3)有机化合物中一定含有的元素是_____ 。
(4)钙原子最外层电子数为_____ 。
(5)O与S中,原子半径较小的是_____ 。
(6)氮的原子结构示意图为_____ 。
(7)非金属性最强的元素是_____ ;氢氧化物呈两性的元素是_____ 。
(8) 与
与 中,酸性较强的是
中,酸性较强的是_____ 。
(9)钠、钾分别与水反应,反应更剧烈的是_____ 。
(10)已知溴 与氯同主族,且位于第4周期。根据溴元素在元素周期表中的位置推测,下列结论正确的是
与氯同主族,且位于第4周期。根据溴元素在元素周期表中的位置推测,下列结论正确的是_____ (填标号)。
A.热稳定性:
B.氧化性: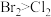
C. 能与
能与 溶液发生反应
溶液发生反应
族 周期 | 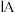 | 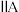 | 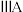 | 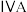 | 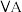 | 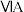 | 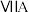 |
| 2 | a | C | N | O | F | ||
| 3 |  |  | b | S |  | ||
| 4 | K |  |
(2)b的元素符号是
(3)有机化合物中一定含有的元素是
(4)钙原子最外层电子数为
(5)O与S中,原子半径较小的是
(6)氮的原子结构示意图为
(7)非金属性最强的元素是
(8)
 与
与 中,酸性较强的是
中,酸性较强的是(9)钠、钾分别与水反应,反应更剧烈的是
(10)已知溴
 与氯同主族,且位于第4周期。根据溴元素在元素周期表中的位置推测,下列结论正确的是
与氯同主族,且位于第4周期。根据溴元素在元素周期表中的位置推测,下列结论正确的是A.热稳定性:

B.氧化性:
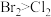
C.
 能与
能与 溶液发生反应
溶液发生反应
您最近一年使用:0次
8 . 在2L的恒容密闭容器中充入1mol CO和2mol 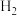 ,一定条件下发生反应:
,一定条件下发生反应: ,测得和
,测得和 的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
的物质的量变化如图1所示,反应过程中的能量变化如图2所示。___________  。平衡时
。平衡时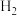 的转化率为
的转化率为___________ 。
(2)下列措施能增大反应速率的是___________(填字母)。
(3)下列描述中能说明上述反应达到平衡状态的是___________。
(4)该反应是___________ 反应(填“吸热”或“放热”),已知断开1mol CO(g)和2mol  中的化学键需要吸收的能量为1924kJ,则断开1mol
中的化学键需要吸收的能量为1924kJ,则断开1mol  中的化学键所需要吸收
中的化学键所需要吸收___________ kJ的能量。
(5)汽车尾气(含有烃类、CO、 、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式
、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式___________ 。
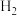 ,一定条件下发生反应:
,一定条件下发生反应: ,测得和
,测得和 的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
的物质的量变化如图1所示,反应过程中的能量变化如图2所示。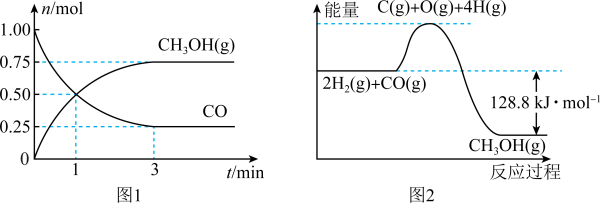
 。平衡时
。平衡时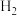 的转化率为
的转化率为(2)下列措施能增大反应速率的是___________(填字母)。
| A.升高温度 | B.降低压强 | C.减小 的浓度 的浓度 | D.加入合适的催化剂 |
(3)下列描述中能说明上述反应达到平衡状态的是___________。
A.CO、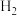 和 和 三种物质的浓度相等 三种物质的浓度相等 |
| B.混合气体的密度不随时间的变化而变化 |
| C.混合气体的总物质的量不随时间的变化而变化 |
D.单位时间内消耗2mol 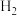 的同时生成1mol 的同时生成1mol  |
(4)该反应是
 中的化学键需要吸收的能量为1924kJ,则断开1mol
中的化学键需要吸收的能量为1924kJ,则断开1mol  中的化学键所需要吸收
中的化学键所需要吸收(5)汽车尾气(含有烃类、CO、
 、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式
、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式
您最近一年使用:0次
2024-07-12更新
|
98次组卷
|
2卷引用:2024年天津市普通高中学业水平合格性考试河东区化学模拟试卷
9 . 化学与人类生活、生产密切相关。请根据题意填空:
(1)84消毒液是生活中常用的消毒剂,其有效成分是___________ (填“NaCl”或“NaClO”);
(2)工业制硝酸中的一个重要反应为: 。一定条件下,将3 mol H2和2 mol N2充入体积为1L的密闭容器中,5min后得到NH3的物质的量为1mol,则用NH3的浓度变化表示该反应的平均速率为
。一定条件下,将3 mol H2和2 mol N2充入体积为1L的密闭容器中,5min后得到NH3的物质的量为1mol,则用NH3的浓度变化表示该反应的平均速率为___________  ;
;
(3)工艺师刻蚀石英制作艺术品所用试剂是___________ (填“盐酸”或“氢氟酸”)。
(1)84消毒液是生活中常用的消毒剂,其有效成分是
(2)工业制硝酸中的一个重要反应为:
 。一定条件下,将3 mol H2和2 mol N2充入体积为1L的密闭容器中,5min后得到NH3的物质的量为1mol,则用NH3的浓度变化表示该反应的平均速率为
。一定条件下,将3 mol H2和2 mol N2充入体积为1L的密闭容器中,5min后得到NH3的物质的量为1mol,则用NH3的浓度变化表示该反应的平均速率为 ;
;(3)工艺师刻蚀石英制作艺术品所用试剂是
您最近一年使用:0次
10 . 化学是一门实用性很强的科学。请根据题意填空:
(1)钠有多种化合物,其中可作为治疗胃酸的药物的成分是___________ (填“Na2CO3”或“NaHCO3”);
(2)铁有多种氧化物,其中铁锈的主要成分是___________ (填“Fe2O3”或“Fe3O4”);
(3)滴加氢氧化钠溶液,先产生白色沉淀,继续滴加氢氧化钠溶液,白色沉淀逐渐溶解的是___________ (填“ ”或“
”或“ ”)。
”)。
(1)钠有多种化合物,其中可作为治疗胃酸的药物的成分是
(2)铁有多种氧化物,其中铁锈的主要成分是
(3)滴加氢氧化钠溶液,先产生白色沉淀,继续滴加氢氧化钠溶液,白色沉淀逐渐溶解的是
 ”或“
”或“ ”)。
”)。
您最近一年使用:0次



