1 . 如表是元素周期表的一部分,表中的每个编号代表一种短周期主族元素,请回答下列问题:
(1)元素②的原子结构示意图是______ 。
(2)比较元素原子半径大小:③______ ④(填“>”或“<”)。
(3)元素③位于元素周期表中第______ 周期VA族。
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式______ 。
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为______ 。
| 族 周期 | IA | 0 | ||||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ② | ③ | ④ | |||||||
| 3 | ⑤ | ⑥ | ||||||||
(2)比较元素原子半径大小:③
(3)元素③位于元素周期表中第
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为
您最近一年使用:0次
2 . 实验室需要配制100mL1.00mol/L的NaNO3溶液,扎西老师进行了如下操作:
(1)计算需要NaNO3固体的质量:______ 克。
(2)根据计算结果,用______ (填仪器名称)称量NaNO3固体。
(3)在烧杯中加入适量蒸馏水,将固体溶解;冷却至室温,将烧杯中的溶液转移至容量瓶时,玻璃棒的作用是______ ;用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液一并注入到容量瓶中。
(4)将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1~2cm时,改用______ (填仪器名称)滴加蒸馏水至液面与刻度线相切;盖好瓶塞,反复上下颠倒,摇匀。
(5)定容时,仰视液面,则所配溶液物质的量浓度______ (填“偏大”或“偏小”)。
(1)计算需要NaNO3固体的质量:
(2)根据计算结果,用
(3)在烧杯中加入适量蒸馏水,将固体溶解;冷却至室温,将烧杯中的溶液转移至容量瓶时,玻璃棒的作用是
(4)将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1~2cm时,改用
(5)定容时,仰视液面,则所配溶液物质的量浓度
您最近一年使用:0次
3 . 某化学兴趣小组欲利用下列试剂:铁粉、锌粉、 溶液、KSCN溶液、新制氯水,探究
溶液、KSCN溶液、新制氯水,探究 的还原性,请回答下列问题:
的还原性,请回答下列问题:
(1)用所给试剂写出体现 具有还原性的离子反应方程式:
具有还原性的离子反应方程式:_______ ,由此得出,在配制 溶液时,
溶液时, 容易被氧化,欲检验
容易被氧化,欲检验 溶液是否变质,应加入的试剂是
溶液是否变质,应加入的试剂是_______ ;
(2)该小组同学用 溶液和NaOH溶液混合制备
溶液和NaOH溶液混合制备 ,观察到沉淀最终变成红褐色,原因是
,观察到沉淀最终变成红褐色,原因是_______ (用化学方程式解释);
(3)酸性条件下,某反应中反应物与生成物有 、
、 、
、 、
、 、
、 和一种未知离子X。
和一种未知离子X。
已知:反应中1mol 得5mol电子。
得5mol电子。
① 中Mn元素的化合价为
中Mn元素的化合价为_______ ,X离子是_______ 。
②该反应的离子方程式是_______ 。
 溶液、KSCN溶液、新制氯水,探究
溶液、KSCN溶液、新制氯水,探究 的还原性,请回答下列问题:
的还原性,请回答下列问题:(1)用所给试剂写出体现
 具有还原性的离子反应方程式:
具有还原性的离子反应方程式: 溶液时,
溶液时, 容易被氧化,欲检验
容易被氧化,欲检验 溶液是否变质,应加入的试剂是
溶液是否变质,应加入的试剂是(2)该小组同学用
 溶液和NaOH溶液混合制备
溶液和NaOH溶液混合制备 ,观察到沉淀最终变成红褐色,原因是
,观察到沉淀最终变成红褐色,原因是(3)酸性条件下,某反应中反应物与生成物有
 、
、 、
、 、
、 、
、 和一种未知离子X。
和一种未知离子X。已知:反应中1mol
 得5mol电子。
得5mol电子。①
 中Mn元素的化合价为
中Mn元素的化合价为②该反应的离子方程式是
您最近一年使用:0次
4 . 现有以下物质:①Cu、② 、③
、③ 胶体、④酒精、⑤
胶体、④酒精、⑤ 、⑥稀硫酸、⑦
、⑥稀硫酸、⑦ 固体、⑧NaOH溶液。
固体、⑧NaOH溶液。
(1)以上物质中属于混合物的是_______ (填数字序号,下同),属于电解质的是_______ ;
(2)向③中逐滴滴加⑥至过量,可观察到的现象是_______ ,此过程中发生反应的离子方程式为_______ ;
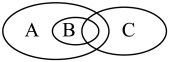
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_______ (填字母序号);
(4)有同学认为 只表示强酸和强碱反应生成可溶性盐的中和反应,请用题中所给物质举个反例反驳上述观点
只表示强酸和强碱反应生成可溶性盐的中和反应,请用题中所给物质举个反例反驳上述观点_______ (用化学方程式表示);
(5)在标准状况下,a L 气体中含有b个氧原子,则阿伏加德罗常数为
气体中含有b个氧原子,则阿伏加德罗常数为_______  。
。
 、③
、③ 胶体、④酒精、⑤
胶体、④酒精、⑤ 、⑥稀硫酸、⑦
、⑥稀硫酸、⑦ 固体、⑧NaOH溶液。
固体、⑧NaOH溶液。(1)以上物质中属于混合物的是
(2)向③中逐滴滴加⑥至过量,可观察到的现象是
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(4)有同学认为
 只表示强酸和强碱反应生成可溶性盐的中和反应,请用题中所给物质举个反例反驳上述观点
只表示强酸和强碱反应生成可溶性盐的中和反应,请用题中所给物质举个反例反驳上述观点(5)在标准状况下,a L
 气体中含有b个氧原子,则阿伏加德罗常数为
气体中含有b个氧原子,则阿伏加德罗常数为 。
。
您最近一年使用:0次
5 . 从下列五种有机物中选择合适的答案,将其选项符号填在空格内。
A.乙醇 B.乙酸 C.油脂 D.葡萄糖 E.纤维素
(1)属于食醋的主要成分是_______ 。
(2)血糖较低时,可及时补充的是_______ 。
(3)75%(体积分数)的水溶液具有消毒作用的是_______ 。
(4)花生油、胡麻油、牛油的主要成分是_______ 。
(5)植物的根、茎、叶、果皮主要含有的有机成分是_______ 。
A.乙醇 B.乙酸 C.油脂 D.葡萄糖 E.纤维素
(1)属于食醋的主要成分是
(2)血糖较低时,可及时补充的是
(3)75%(体积分数)的水溶液具有消毒作用的是
(4)花生油、胡麻油、牛油的主要成分是
(5)植物的根、茎、叶、果皮主要含有的有机成分是
您最近一年使用:0次
6 . 下表是元素周期表的一部分,回答下列问题。
(1)原子结构示意图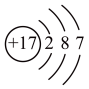 所表示的原子是
所表示的原子是___________ 。
(2)H2O分子的电子式为___________ (填序号)。
a.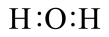 b.
b.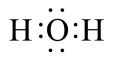 c.
c. 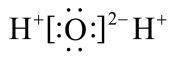
(3)根据元素在周期表中的位置推测Na、Al和Cl原子半径由大到小的顺序为___________ 。
(4)重水是核能开发中的重要原料。核素 H与
H与 H之间互称
H之间互称___________ 。
(5)已知:
据此推断,F、Cl两元素非金属性较强的是___________ (填元素符号)。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | H | ||||||
| 二 | O | F | |||||
| 三 | Na | Al | Cl |
 所表示的原子是
所表示的原子是(2)H2O分子的电子式为
a.
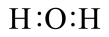 b.
b.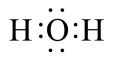 c.
c. 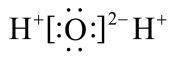
(3)根据元素在周期表中的位置推测Na、Al和Cl原子半径由大到小的顺序为
(4)重水是核能开发中的重要原料。核素
 H与
H与 H之间互称
H之间互称(5)已知:
| H2+F2=2HF | 在暗处能剧烈化合并发生爆炸,生成的氟化氢很稳定 |
H2+Cl2 2HCl 2HCl | 光照或点燃发生反应,生成的氯化氢较稳定 |
您最近一年使用:0次
解题方法
7 . 2021年10月20日,央视新闻报道:
a.2022年冬奥会火种抵达北京,火炬传递方案确定;
b.我国自主研制的世界最大推力整体式固体火箭发动机试车成功;
c.我国将加快推进汽车动力电池回收利用立法。
(1)关于奥运火炬燃料、固体火箭发动机燃料和汽车动力电池,下列说法正确的是___________ (填字母)。
A.作为奥运火炬燃料的主要成分,丙烷和丁烷互为同系物
B.固体火箭发动机燃料燃烧时,发生剧烈氧化还原反应
C.汽车动力电池只能将化学能转化为电能
(2)结合上述新闻报道,从多个角度谈谈你的认识___________ 。
a.2022年冬奥会火种抵达北京,火炬传递方案确定;
b.我国自主研制的世界最大推力整体式固体火箭发动机试车成功;
c.我国将加快推进汽车动力电池回收利用立法。
(1)关于奥运火炬燃料、固体火箭发动机燃料和汽车动力电池,下列说法正确的是
A.作为奥运火炬燃料的主要成分,丙烷和丁烷互为同系物
B.固体火箭发动机燃料燃烧时,发生剧烈氧化还原反应
C.汽车动力电池只能将化学能转化为电能
(2)结合上述新闻报道,从多个角度谈谈你的认识
您最近一年使用:0次
解题方法
8 . 工业上用FeCl3溶液作印刷电路铜板的腐蚀液。化学小组设计如下流程对腐蚀废液(阳离子主要有Fe2+、Cu2+、Fe3+和H+)进行处理,实现FeCl3溶液再生并回收Cu。_______ (填“氧化”或“还原”)为Fe3+。
(2)步骤Ⅱ中发生反应的离子方程式为_______ 。
(3)溶液C中含有大量Fe2+。取少量溶液C于试管中,滴加_______ 溶液,有白色沉淀生成,白色沉淀迅速变为灰绿色,最终变为红褐色。
(4)下列说法合理的是_______ (填字母)。
a.溶液A、溶液B和固体C中都含有铜元素
b.溶液C和溶液D可回收利用,体现“绿色化学”理念
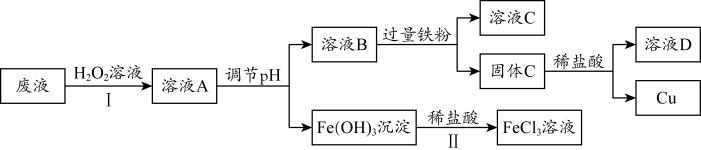
(2)步骤Ⅱ中发生反应的离子方程式为
(3)溶液C中含有大量Fe2+。取少量溶液C于试管中,滴加
(4)下列说法合理的是
a.溶液A、溶液B和固体C中都含有铜元素
b.溶液C和溶液D可回收利用,体现“绿色化学”理念
您最近一年使用:0次
名校
解题方法
9 . 一氯化碘(ICl)是一种卤素互化物,与卤素单质性质相似,可用于制农药等。
(1)Cl在元素周期表中位于第三周期、第_______ 族。
(2)Cl的最高价氧化物对应的水化物为HClO4,其中Cl元素的化合价为_______ 价。
(3)Cl的非金属性强于I的,用原子结构解释原因:Cl和I位于同一主族,最外层电子数相同,_______ ,得电子能力Cl强于I。
(4)下列推断中,正确的是_______ (填字母)。
a.ICl有氧化性
b.热稳定性:HI>HCl
c.I的最高价氧化物对应的水化物为HIO4
(1)Cl在元素周期表中位于第三周期、第
(2)Cl的最高价氧化物对应的水化物为HClO4,其中Cl元素的化合价为
(3)Cl的非金属性强于I的,用原子结构解释原因:Cl和I位于同一主族,最外层电子数相同,
(4)下列推断中,正确的是
a.ICl有氧化性
b.热稳定性:HI>HCl
c.I的最高价氧化物对应的水化物为HIO4
您最近一年使用:0次
2023-01-17更新
|
273次组卷
|
2卷引用:北京市2022-2023学年高二上学期第二次合格考化学试题
名校
解题方法
10 . 阅读短文,回答问题。
2021年10月16日,我国神舟十三号载人飞船成功将三名航天员送入太空。
我国自主研发、拥有知识产权的高科技新材料为航天事业的发展做出了巨大贡献。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)飞船使用的铝合金材料仅由铝元素组成。(_______)
(2)用于飞船推进舱承力截锥的碳纤维复合材料,具备强度高、承载力大的特点。(_______)
(3)航天员舱内生活用服装体感舒适,采用了高科技康纶纤维材料。(_______)
(4)我国研发的高科技新材料为航天事业的发展做出了巨大贡献。(_______)
2021年10月16日,我国神舟十三号载人飞船成功将三名航天员送入太空。

我国自主研发、拥有知识产权的高科技新材料为航天事业的发展做出了巨大贡献。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)飞船使用的铝合金材料仅由铝元素组成。(_______)
(2)用于飞船推进舱承力截锥的碳纤维复合材料,具备强度高、承载力大的特点。(_______)
(3)航天员舱内生活用服装体感舒适,采用了高科技康纶纤维材料。(_______)
(4)我国研发的高科技新材料为航天事业的发展做出了巨大贡献。(_______)
您最近一年使用:0次
2023-01-17更新
|
174次组卷
|
2卷引用:北京市2022-2023学年高二上学期第二次合格考化学试题



