现有以下物质:①Cu、② 、③
、③ 胶体、④酒精、⑤
胶体、④酒精、⑤ 、⑥稀硫酸、⑦
、⑥稀硫酸、⑦ 固体、⑧NaOH溶液。
固体、⑧NaOH溶液。
(1)以上物质中属于混合物的是_______ (填数字序号,下同),属于电解质的是_______ ;
(2)向③中逐滴滴加⑥至过量,可观察到的现象是_______ ,此过程中发生反应的离子方程式为_______ ;
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_______ (填字母序号);
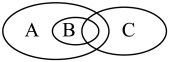
(4)有同学认为 只表示强酸和强碱反应生成可溶性盐的中和反应,请用题中所给物质举个反例反驳上述观点
只表示强酸和强碱反应生成可溶性盐的中和反应,请用题中所给物质举个反例反驳上述观点_______ (用化学方程式表示);
(5)在标准状况下,a L 气体中含有b个氧原子,则阿伏加德罗常数为
气体中含有b个氧原子,则阿伏加德罗常数为_______  。
。
 、③
、③ 胶体、④酒精、⑤
胶体、④酒精、⑤ 、⑥稀硫酸、⑦
、⑥稀硫酸、⑦ 固体、⑧NaOH溶液。
固体、⑧NaOH溶液。(1)以上物质中属于混合物的是
(2)向③中逐滴滴加⑥至过量,可观察到的现象是
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(4)有同学认为
 只表示强酸和强碱反应生成可溶性盐的中和反应,请用题中所给物质举个反例反驳上述观点
只表示强酸和强碱反应生成可溶性盐的中和反应,请用题中所给物质举个反例反驳上述观点(5)在标准状况下,a L
 气体中含有b个氧原子,则阿伏加德罗常数为
气体中含有b个氧原子,则阿伏加德罗常数为 。
。
2022高一上·江西抚州·学业考试 查看更多[2]
更新时间:2023-08-05 11:55:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系。
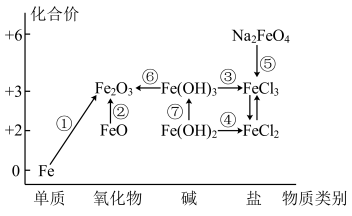
请回答以下问题:
(1) 中Fe的化合价为
中Fe的化合价为_______ 。
(2) 是否为碱性氧化物
是否为碱性氧化物_______ (填是或否),理由:_______ 。
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:_______ 。
(4)已知 在强碱溶液中稳定存在,PH越小稳定性越差;则制备
在强碱溶液中稳定存在,PH越小稳定性越差;则制备 时需要在
时需要在_______ (填“酸性”“碱性”或“中性”)环境中进行: 也可以作为净水剂,能与水反应生成具有吸附性的
也可以作为净水剂,能与水反应生成具有吸附性的 胶体,写出其中离子方程式:
胶体,写出其中离子方程式:_______ 。其中检验溶液中 的试剂是
的试剂是_______ 。
(5)FeO、 是合成氨工业生产中所用的
是合成氨工业生产中所用的 催化剂的主要成分。某FeO、
催化剂的主要成分。某FeO、 混合物中,铁原子、氧原子的物质的量之比为4∶5,其中FeO、
混合物中,铁原子、氧原子的物质的量之比为4∶5,其中FeO、 的物质的量之比为
的物质的量之比为_______ 。

请回答以下问题:
(1)
 中Fe的化合价为
中Fe的化合价为(2)
 是否为碱性氧化物
是否为碱性氧化物(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(4)已知
 在强碱溶液中稳定存在,PH越小稳定性越差;则制备
在强碱溶液中稳定存在,PH越小稳定性越差;则制备 时需要在
时需要在 也可以作为净水剂,能与水反应生成具有吸附性的
也可以作为净水剂,能与水反应生成具有吸附性的 胶体,写出其中离子方程式:
胶体,写出其中离子方程式: 的试剂是
的试剂是(5)FeO、
 是合成氨工业生产中所用的
是合成氨工业生产中所用的 催化剂的主要成分。某FeO、
催化剂的主要成分。某FeO、 混合物中,铁原子、氧原子的物质的量之比为4∶5,其中FeO、
混合物中,铁原子、氧原子的物质的量之比为4∶5,其中FeO、 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请按要求回答下列问题:
(1)写出硫酸氢钠溶于水的电离方程式:___________ 。
(2)写出实验室制取氯气的离子反应方程式:___________ 。
(3)我国古代四大发明之一的黑火药是由硫黄、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。
①该反应的氧化剂是___________ 。
②在标准状况下,若生成22.4L气体,则转移的电子数目为___________ NA。
(4)某元素G的一种含氧酸化学式为H3GO3,属于二元酸,则H3GO3与过量氢氧化钠溶液反应生成的产物Na2HGO3为___________ (填“酸式盐”或“正盐”)。
(1)写出硫酸氢钠溶于水的电离方程式:
(2)写出实验室制取氯气的离子反应方程式:
(3)我国古代四大发明之一的黑火药是由硫黄、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。
①该反应的氧化剂是
②在标准状况下,若生成22.4L气体,则转移的电子数目为
(4)某元素G的一种含氧酸化学式为H3GO3,属于二元酸,则H3GO3与过量氢氧化钠溶液反应生成的产物Na2HGO3为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列物质:①Na2CO3·10H2O晶体,②石墨,③无水酒精,④小苏打,⑤硫酸氢钾固体,⑥熔融的硝酸钾,⑦氨气,⑧稀硝酸,⑨醋酸。
(1)按物质的分类方法,填写表格的空白处(填序号):
(2)写出下列物质在水溶液中的电离方程式:
小苏打_____________
硫酸氢钾___________
醋酸____________
(3)写出属于酸式盐的两种物质在水溶液中反应的离子方程式:___ 。
(1)按物质的分类方法,填写表格的空白处(填序号):
分类标准 | 能导电的物质 | 电解质 | 非电解质 | 强电解质 |
| 属于该类的物质 |
(2)写出下列物质在水溶液中的电离方程式:
小苏打
硫酸氢钾
醋酸
(3)写出属于酸式盐的两种物质在水溶液中反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】24g O2分子所含氧原子数目(用NA表示)_______ ;
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】50 mL 12 mol·L-1盐酸与足量MnO2共热, 转移的电子数为0.3NA___
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1) 个
个 分子含有原子
分子含有原子_______  ,含H
,含H_______  。
。
(2) 和
和 的混合溶液,已知其中
的混合溶液,已知其中 的浓度为
的浓度为 ,
,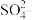 浓度为
浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为_______ 。
(3)某小组同学探究碳酸钠和碳酸氢钠的性质,设计实验如下,请你根据实验现象,按要求作答。
(1)
 个
个 分子含有原子
分子含有原子 ,含H
,含H 。
。(2)
 和
和 的混合溶液,已知其中
的混合溶液,已知其中 的浓度为
的浓度为 ,
,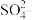 浓度为
浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为(3)某小组同学探究碳酸钠和碳酸氢钠的性质,设计实验如下,请你根据实验现象,按要求作答。
| 实验步骤 | 实验现象 | 结论或解释(用离子方程式表示) |
| ①分别向盛有Na2CO3溶液和NaHCO3的试管中滴加少量澄清石灰水 | 均产生浑浊 | 碳酸钠溶液: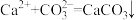 碳酸氢钠溶液: |
| ②向盛有Na2CO3溶液的试管中滴加稀盐酸 | 开始无气泡产生一段时间后产生气泡 | 开始时:CO +H+ = HCO +H+ = HCO 一段时间后: |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有下列物质:①酒精、②NaHSO4溶液、③液氯、④NH3、⑤Ba(OH)2固体、⑥铁、⑦小苏打、⑧淀粉溶液、⑨NaHCO3溶液、⑩澄清石灰水。
(1)属于电解质的是________ (填序号,下同),属于非电解质的是________ 。
(2)②⑧两种分散系的本质区别是________________ 。
(3)向⑨中滴加少量⑩的离子方程式为________________ 。
(4)写出实验室制备气态③的化学方程式________________ 。
(1)属于电解质的是
(2)②⑧两种分散系的本质区别是
(3)向⑨中滴加少量⑩的离子方程式为
(4)写出实验室制备气态③的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求书写方程式
(1)过氧化钠与水反应:___________ 。
(2)将 改写为对应的化学方程式
改写为对应的化学方程式___________ 。
(3)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的 ,配平该反应的离子方程式:
,配平该反应的离子方程式:___________ 。

(1)过氧化钠与水反应:
(2)将
 改写为对应的化学方程式
改写为对应的化学方程式(3)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的
 ,配平该反应的离子方程式:
,配平该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列下题
(1)下列叙述中正确的有___________ (填序号)。
①NaCl溶液在电流的作用下电离成钠离子和氯离子
②强电解质溶液的导电性比弱电解质溶液的导电性强
③CO2的水溶液导电能力很弱,所以CO2是弱电解质
④BaSO4溶于水的部分能够完全电离,故它是强电解质
(2)NaHSO4在水溶液中的电离方程式为___________ ,若向其中加入NaOH溶液,反应的离子方程式为___________ 。KHCO3在水溶液中的电离方程式为___________ ,若向其中加入少量Ba(OH)2溶液,反应的离子方程式为___________ 。
(3)amolH2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为___________ mol﹣1
(4)在标准状况下,NO和NO2的混合气体共33.6L,质量为53g,该混合气体中NO与NO2的体积之比为___________ 。
(5)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是___________ 。
(1)下列叙述中正确的有
①NaCl溶液在电流的作用下电离成钠离子和氯离子
②强电解质溶液的导电性比弱电解质溶液的导电性强
③CO2的水溶液导电能力很弱,所以CO2是弱电解质
④BaSO4溶于水的部分能够完全电离,故它是强电解质
(2)NaHSO4在水溶液中的电离方程式为
(3)amolH2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为
(4)在标准状况下,NO和NO2的混合气体共33.6L,质量为53g,该混合气体中NO与NO2的体积之比为
(5)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是
您最近一年使用:0次



