回答下列问题:
(1) 个
个 分子含有原子
分子含有原子_______  ,含H
,含H_______  。
。
(2) 和
和 的混合溶液,已知其中
的混合溶液,已知其中 的浓度为
的浓度为 ,
,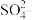 浓度为
浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为_______ 。
(3)某小组同学探究碳酸钠和碳酸氢钠的性质,设计实验如下,请你根据实验现象,按要求作答。
(1)
 个
个 分子含有原子
分子含有原子 ,含H
,含H 。
。(2)
 和
和 的混合溶液,已知其中
的混合溶液,已知其中 的浓度为
的浓度为 ,
,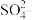 浓度为
浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为(3)某小组同学探究碳酸钠和碳酸氢钠的性质,设计实验如下,请你根据实验现象,按要求作答。
| 实验步骤 | 实验现象 | 结论或解释(用离子方程式表示) |
| ①分别向盛有Na2CO3溶液和NaHCO3的试管中滴加少量澄清石灰水 | 均产生浑浊 | 碳酸钠溶液: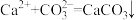 碳酸氢钠溶液: |
| ②向盛有Na2CO3溶液的试管中滴加稀盐酸 | 开始无气泡产生一段时间后产生气泡 | 开始时:CO +H+ = HCO +H+ = HCO 一段时间后: |
更新时间:2023-01-02 10:41:50
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4C1、FeC13、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是______ (写化学式)。
(2)写出并配平该反应的化学方程式:______ ;
(3)当转移的电子总数为a个时,氮气物质的量变化了bmol,阿伏加德罗数常数为(用含a、b的代数式表示)______ 。
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为______ 。
(1)根据题意,可判断出X是
(2)写出并配平该反应的化学方程式:
(3)当转移的电子总数为a个时,氮气物质的量变化了bmol,阿伏加德罗数常数为(用含a、b的代数式表示)
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】 中含有b个
中含有b个 ,则阿伏加德罗常数为
,则阿伏加德罗常数为___________ 。(用含有a,b的代数式表示)
 中含有b个
中含有b个 ,则阿伏加德罗常数为
,则阿伏加德罗常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是_______ 。
A.(2023·海南卷)2.4g镁条在空气中充分燃烧,转移的电子数目为
B.(2023·辽宁卷)我国古代四大发明之一黑火药的爆炸反应为: ,每生成
,每生成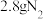 转移电子数目为
转移电子数目为
C.(2023·重庆卷)已知反应: ,若消耗
,若消耗 (标准状况)
(标准状况) ,转移的电子数为
,转移的电子数为
D.(2022·全国卷)电解熔融 ,阴极增重
,阴极增重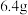 ,外电路中通过电子的数目为
,外电路中通过电子的数目为
E.(2022·浙江卷)足量的浓盐酸与8.7gMnO2反应,转移电子的数目为0.4NA
F.(2022·河北卷)3.9gNa2O2与足量水反应,转移电子个数为0.1NA
G.(2021·全国卷) 的
的 与
与 完全反应时转移的电子数为
完全反应时转移的电子数为
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.(2023·海南卷)2.4g镁条在空气中充分燃烧,转移的电子数目为

B.(2023·辽宁卷)我国古代四大发明之一黑火药的爆炸反应为:
 ,每生成
,每生成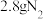 转移电子数目为
转移电子数目为
C.(2023·重庆卷)已知反应:
 ,若消耗
,若消耗 (标准状况)
(标准状况) ,转移的电子数为
,转移的电子数为
D.(2022·全国卷)电解熔融
 ,阴极增重
,阴极增重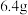 ,外电路中通过电子的数目为
,外电路中通过电子的数目为
E.(2022·浙江卷)足量的浓盐酸与8.7gMnO2反应,转移电子的数目为0.4NA
F.(2022·河北卷)3.9gNa2O2与足量水反应,转移电子个数为0.1NA
G.(2021·全国卷)
 的
的 与
与 完全反应时转移的电子数为
完全反应时转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】无土栽培是利用营养液栽培作物的一种方法,某科研小组取用0.2L营养液进行实验,该营养液含有KCl、K2SO4、NH4Cl三种溶质,测得该营养液中部分离子浓度大小如下表所示,回答下列问题
(1)该营养液中K2SO4的物质的量浓度为_______ mol·L-1,含溶质KCl的质量为_______ 。
(2)该营养液中NH4Cl的物质的量为_______ 。
(3)该营养液加水稀释的过程中测得溶液中NH 的物质的量浓度(c)随溶液体积(V)变化的曲线如图所示,则V1为
的物质的量浓度(c)随溶液体积(V)变化的曲线如图所示,则V1为_______ L,V2为_______ L。

| 离子符号 | K+ | SO | Cl- |
| 物质的量浓度(mol·L-1) | 9.0 | 4.0 | 9.0 |
(2)该营养液中NH4Cl的物质的量为
(3)该营养液加水稀释的过程中测得溶液中NH
 的物质的量浓度(c)随溶液体积(V)变化的曲线如图所示,则V1为
的物质的量浓度(c)随溶液体积(V)变化的曲线如图所示,则V1为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】标准状况下,400体积 溶于1体积水得到氨水溶液(
溶于1体积水得到氨水溶液(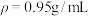 ),氨水浓度为
),氨水浓度为_______ 。
 溶于1体积水得到氨水溶液(
溶于1体积水得到氨水溶液(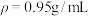 ),氨水浓度为
),氨水浓度为
您最近一年使用:0次
【推荐3】金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的相关知识回答下列问题:
(1)经检测某酸性废水中所含离子及其浓度如表所示:
则c(Al3+)=___________ mol/L。
(2)已知Fe(NO3)3的高纯度结晶体是一种紫色潮解性固体,适用于制备磁性氧化铁纳米粉末。写出磁性氧化铁与足量稀硝酸反应的离子方程式:___________ 。
(3)用托盘天平(1g以下用游码)称量绿矾(FeSO4·7H2O)晶体配制450mL0.1mol/L溶液,以下实验操作会导致所配溶液浓度偏低的是___________ 。
a.用托盘天平称量绿矾晶体时,将砝码放在左盘,药品放在右盘
b.洗涤烧杯和玻璃棒后,将洗涤液倒入废液缸中
c.摇匀后发现液面低于刻线,未补加水
d.定容时,俯视刻度线
(4)8.34 g绿矾(FeSO4·7H2O)晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示:

温度为159 ℃时固体N的化学式为___________ ,取适量380 ℃时所得的样品P,隔绝空气加热至650 ℃,得到一种红棕色固体物质Q,同时有两种无色气体生成,请写出该反应的化学方程式___________ 。
(5)钠的化合物广泛应用于工业生产。
①NaH能与水剧烈反应,反应方程式为NaH+H2O=NaOH+H2↑,NaH与液氨也有类似的反应,请写出NaH与液氨反应的化学方程式___________ 。
②现有由两种含钠化合物组成的混合物,溶于水后,逐滴加入某浓度盐酸,所得CO2的粒子数目与所耗HCl的粒子数目关系如图,两种含钠化合物的化学式及物质的量之比为___________ 。

(1)经检测某酸性废水中所含离子及其浓度如表所示:
| 离子 | Fe3+ | Al3+ | SO | NO | H+ |
| 浓度(mol/L) | 2×10-2 | 1×10-1 | 2×10-2 | 1×10-1 |
(2)已知Fe(NO3)3的高纯度结晶体是一种紫色潮解性固体,适用于制备磁性氧化铁纳米粉末。写出磁性氧化铁与足量稀硝酸反应的离子方程式:
(3)用托盘天平(1g以下用游码)称量绿矾(FeSO4·7H2O)晶体配制450mL0.1mol/L溶液,以下实验操作会导致所配溶液浓度偏低的是
a.用托盘天平称量绿矾晶体时,将砝码放在左盘,药品放在右盘
b.洗涤烧杯和玻璃棒后,将洗涤液倒入废液缸中
c.摇匀后发现液面低于刻线,未补加水
d.定容时,俯视刻度线
(4)8.34 g绿矾(FeSO4·7H2O)晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示:

温度为159 ℃时固体N的化学式为
(5)钠的化合物广泛应用于工业生产。
①NaH能与水剧烈反应,反应方程式为NaH+H2O=NaOH+H2↑,NaH与液氨也有类似的反应,请写出NaH与液氨反应的化学方程式
②现有由两种含钠化合物组成的混合物,溶于水后,逐滴加入某浓度盐酸,所得CO2的粒子数目与所耗HCl的粒子数目关系如图,两种含钠化合物的化学式及物质的量之比为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】用化学方法除去下列物质中混有的少量杂质,其中括号内为杂质,写出除杂需加入的试剂(用化学式表示)以及发生反应的离子方程式。
(1)固体Na2CO3(NaHCO3)除杂发生反应的化学方程式___ ;
(2)固体Fe(OH)3(Al(OH)3)除杂发生反应的离子方程式____ ;
(3)溶液FeCl2(CuCl2)除杂发生反应的离子方程式____ ;
(4)气体CO2(HCl)除杂发生反应的离子方程式___ 。
(1)固体Na2CO3(NaHCO3)除杂发生反应的化学方程式
(2)固体Fe(OH)3(Al(OH)3)除杂发生反应的离子方程式
(3)溶液FeCl2(CuCl2)除杂发生反应的离子方程式
(4)气体CO2(HCl)除杂发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有以下几种物质:①液氧②硝酸钾溶液③ ④干冰⑤
④干冰⑤ ⑥熔融的
⑥熔融的 ⑦纯碱⑧
⑦纯碱⑧ ⑨
⑨ ⑩澄清石灰水
⑩澄清石灰水
(1)属于电解质的是___________ ,属于非电解质的是___________ ,能导电的是___________ 。
(2)将⑧慢慢滴入⑦的溶液的现象为:___________ 。
(3)少量⑥的与⑩混合的离子反应:___________ 。
(4)⑨在熔融状态下的电离方程式___________ 。
(5)如何鉴别②的阳离子(写出具体操作、现象、结论):___________ 。
 ④干冰⑤
④干冰⑤ ⑥熔融的
⑥熔融的 ⑦纯碱⑧
⑦纯碱⑧ ⑨
⑨ ⑩澄清石灰水
⑩澄清石灰水(1)属于电解质的是
(2)将⑧慢慢滴入⑦的溶液的现象为:
(3)少量⑥的与⑩混合的离子反应:
(4)⑨在熔融状态下的电离方程式
(5)如何鉴别②的阳离子(写出具体操作、现象、结论):
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】二氧化硅和碳酸钙是牙膏中常用的摩擦剂。
(1)物质分类。判断二氧化硅和碳酸钙所属的物质类别(填“酸”“碱”“盐” “酸性氧化物”或“碱性氧化物”)并填入下表。
(2)性质预测。根据用途可推测二氧化硅___________ (填“易溶”或“难溶”)于水。根据二氧化硅所属的物质类别,预测其与CaO在高温下反应的化学方程式:___________ 。
(3)物质制备。以石灰石为原料制备摩擦剂碳酸钙的实验方案如下。
方案1:
方案2:
①写出方案2中石灰石与稀盐酸反应的离子方程式:___________ 。
②为了减少碳排放,上述两个方案中,均需回收利用的物质是___________ (填化学式);与方案1相比,方案2的优点是___________ 。
(1)物质分类。判断二氧化硅和碳酸钙所属的物质类别(填“酸”“碱”“盐” “酸性氧化物”或“碱性氧化物”)并填入下表。
| 摩擦剂 | 二氧化硅 | 碳酸钙 |
| 物质类别 |
(2)性质预测。根据用途可推测二氧化硅
(3)物质制备。以石灰石为原料制备摩擦剂碳酸钙的实验方案如下。
方案1:

方案2:

①写出方案2中石灰石与稀盐酸反应的离子方程式:
②为了减少碳排放,上述两个方案中,均需回收利用的物质是
您最近一年使用:0次



