请按要求回答下列问题:
(1)写出硫酸氢钠溶于水的电离方程式:___________ 。
(2)写出实验室制取氯气的离子反应方程式:___________ 。
(3)我国古代四大发明之一的黑火药是由硫黄、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。
①该反应的氧化剂是___________ 。
②在标准状况下,若生成22.4L气体,则转移的电子数目为___________ NA。
(4)某元素G的一种含氧酸化学式为H3GO3,属于二元酸,则H3GO3与过量氢氧化钠溶液反应生成的产物Na2HGO3为___________ (填“酸式盐”或“正盐”)。
(1)写出硫酸氢钠溶于水的电离方程式:
(2)写出实验室制取氯气的离子反应方程式:
(3)我国古代四大发明之一的黑火药是由硫黄、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。
①该反应的氧化剂是
②在标准状况下,若生成22.4L气体,则转移的电子数目为
(4)某元素G的一种含氧酸化学式为H3GO3,属于二元酸,则H3GO3与过量氢氧化钠溶液反应生成的产物Na2HGO3为
更新时间:2024-01-30 18:07:38
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求用序号填空 :
(1)现有几种物质:①H2O ②空气 ③Mg ④CaO ⑤H2SO4 ⑥Ca(OH)2 ⑦CuSO4 ⑧碘酒 ⑨葡萄糖 ⑩NaHCO3。其中属于混合物的是___________ (填序号,下同);属于单质的是___________ ;属于酸的是___________ ;属于盐的是___________ ;属于有机物的是___________ 。
(2)现有几种物质:①NaHCO3晶体 ②液态HCl ③铁 ④蔗糖 ⑤酒精 ⑥熔融的K2SO4 ⑦干冰 ⑧石墨;其中能导电的是___________ ;(填序号,下同)属于非电解质的是___________ ;属于电解质的是___________ 。
(1)现有几种物质:①H2O ②空气 ③Mg ④CaO ⑤H2SO4 ⑥Ca(OH)2 ⑦CuSO4 ⑧碘酒 ⑨葡萄糖 ⑩NaHCO3。其中属于混合物的是
(2)现有几种物质:①NaHCO3晶体 ②液态HCl ③铁 ④蔗糖 ⑤酒精 ⑥熔融的K2SO4 ⑦干冰 ⑧石墨;其中能导电的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】国际化学年中国宣传口号是“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
I.同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂,勿食用”,其主要成分是生石灰。
(1)生石灰属于_______ (填“酸性氧化物”或“碱性氧化物”)。
(2)生石灰可作干燥剂的理由是_______ (用化学方程式表示)。
(3)生石灰与稀盐酸反应的离子方程式_______ 。
II.Na2CO3和NaHCO3是日常生活中经常遇到的物质。
(4)下列实验方案中,不能测定出Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是_______。
(5)甲组同学为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1g样品加热至质量不再发生变化,其质量变为w2g,则该Na2CO3样品的纯度(质量分数)是_______ 。
(6)混合样品中碳酸钠的质量分数,也可通过加热分解得到的CO2质量进行计算,乙组同学设计的实验装置示意图如下,则下列说法正确的是_______。

I.同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂,勿食用”,其主要成分是生石灰。
(1)生石灰属于
(2)生石灰可作干燥剂的理由是
(3)生石灰与稀盐酸反应的离子方程式
II.Na2CO3和NaHCO3是日常生活中经常遇到的物质。
(4)下列实验方案中,不能测定出Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是_______。
| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
| C.取ag混合物与足量NaOH溶液充分反应,得到bg溶液 |
| D.取ag混合物与足量稀硫酸充分反应,逸出气体经浓硫酸干燥后,用碱石灰吸收质量增加bg |
(6)混合样品中碳酸钠的质量分数,也可通过加热分解得到的CO2质量进行计算,乙组同学设计的实验装置示意图如下,则下列说法正确的是_______。

| A.X气体可以是空气,反应前和反应后均需通一段时间空气 |
| B.装置B、C之间缺少CO2的干燥装置 |
| C.没有a装置会导致所测碳酸钠的质量分数偏高 |
| D.a装置内应装碱石灰,目的是为了尾气处理 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某同学在碳酸饮料和薯片配料表中,发现如下物质:①水、②蔗糖、③浓缩橙汁、④味精(谷氨酸钠)、⑤柠檬酸晶体、⑥小苏打、⑦NaCl晶体、⑧生石灰、⑨二氧化硅固体、⑩Fe粉。请回答下列问题:
(1)上述物质中,既不属于电解质,也不属于非电解质的是_______ ;(填序号)
(2)生石灰CaO属于_______ ;(填字母:A.酸 B.碱 C.盐 D.纯净物 E.化合物 F.金属氧化物 G.非金属氧化物 H.酸性氧化物 I.碱性氧化物)其包装袋上,明确写着不可食用。请问生石灰在食品中的作用主要是:_______ (请用离子方程式表示);该反应属于_______ 反应(四大基本反应类型)。
(3)上述物质易导电的是_______ (填序号);写出NaHCO3在水中的电离方程式_______ ;
(4)实验发现,熔融状态下的NaCl可以导电,但是熔融状态下的AlCl3却不能导电,而AlCl3水溶液却可以导电,请猜测其原因:_______ 。
(1)上述物质中,既不属于电解质,也不属于非电解质的是
(2)生石灰CaO属于
(3)上述物质易导电的是
(4)实验发现,熔融状态下的NaCl可以导电,但是熔融状态下的AlCl3却不能导电,而AlCl3水溶液却可以导电,请猜测其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列10种物质:①铁 ②蔗糖固体 ③盐酸 ④熔融CaO ⑤NaHCO3溶液 ⑥CO2 ⑦熔融NaOH ⑧氢氧化铁胶体 ⑨无水酒精 ⑩FeCl3固体
(1)上述物质属于电解质的有_______ (填序号,下同),属于非电解质的有_______ 。
(2)NaHSO4在水溶液中的电离方程式:_______ 。
(3)少量CO2通入澄清石灰水反应的离子方程式:_______ 。
(4)NaHCO3与NaHSO4溶液反应的离子方程式:_______ 。
(5)实验室制备氢氧化铁胶体的化学方程式:_______ 。
(1)上述物质属于电解质的有
(2)NaHSO4在水溶液中的电离方程式:
(3)少量CO2通入澄清石灰水反应的离子方程式:
(4)NaHCO3与NaHSO4溶液反应的离子方程式:
(5)实验室制备氢氧化铁胶体的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列十种物质: ①蔗糖②熔融 NaCl③石墨④铜丝⑤NaOH固体⑥金刚石⑦NaHSO4固体⑧K2O 固体⑨液态H2SO4⑩饱和 FeCl3溶液
(1)上述物质中可导电的是__________ (填序号,下同); 属于电解质的是__________ 。
(2)上述物质中互为同素异形体的是______________________ 。
(3)NaHSO4是一种酸式盐,在水溶液中的电离方程式为______________________ ;NaHSO4与 Ba(OH)2溶液混合时溶液呈中性,该反应的离子方程式为______________________ 。
(1)上述物质中可导电的是
(2)上述物质中互为同素异形体的是
(3)NaHSO4是一种酸式盐,在水溶液中的电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在图(Ⅰ)所示的装置中,烧杯中盛放的是Ba(OH)2溶液,当从滴定管中逐渐加入某种溶液A时,溶液的导电性的变化趋势如图(Ⅱ)所示。
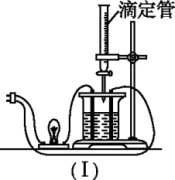
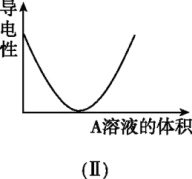
(1)滴加液体至图(Ⅱ)中曲线最低点时,灯泡可能熄灭,溶液A中含有的溶质可能是(填序号)___________ 。
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
(2)NaHSO4属于___________ (填“酸”“碱”或“盐”),写出NaHSO4在水溶液中的电离方程式:___________ 。
(3)用一种试剂除去下列各物质中的杂质(括号内的物质),写出所用的试剂。
Ⅰ.CaCl2(HCl):试剂___________ , Ⅱ.O2(CO2):试剂___________ 。


(1)滴加液体至图(Ⅱ)中曲线最低点时,灯泡可能熄灭,溶液A中含有的溶质可能是(填序号)
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
(2)NaHSO4属于
(3)用一种试剂除去下列各物质中的杂质(括号内的物质),写出所用的试剂。
Ⅰ.CaCl2(HCl):试剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系________ (填“属于”或“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为_____ (填“酸”或“碱”)性,表示该试样酸碱性的c(H+)或c(OH-)=______ mol·L-1。
Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(3)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C______ 具有(填“氧化性”或“还原性”)。
(4)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中每生成1molClO2分子,转移电子的数目为_____ 。
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_____ 。
A.O2 B.FeCl2 C.KCl D.KMnO4
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(3)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C
(4)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中每生成1molClO2分子,转移电子的数目为
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KCl D.KMnO4
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原是一类重要的反应。
(1)某同学写出以下三个化学方程式(未配平)
①N2O4+H2O→HNO3+HNO2 ②NO+HNO3→N2O3+H2O ③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是(填代号)____________ ;
(2)以下反应中H2O2仅体现还原性的是(填代号)____________ ,H2O2既体现氧化性又体现还原性的是(填代号)____________ ,从反应中判断H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是_______________ ;
A.H2O2+2Fe2++2H+=2Fe3++2H2O
B.2H2O2=2H2O+O2↑
C.Ag2O+H2O2=2Ag+O2↑+H2O
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
E.H2O2+MnSO4=MnO2+H2SO4
(3)用“双线桥法”标明以下反应中电子转移的方向和数目________ ,若反应中有3.01×1023个电子转移,则被氧化的还原剂的物质的量为___________ 。
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)某同学写出以下三个化学方程式(未配平)
①N2O4+H2O→HNO3+HNO2 ②NO+HNO3→N2O3+H2O ③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是(填代号)
(2)以下反应中H2O2仅体现还原性的是(填代号)
A.H2O2+2Fe2++2H+=2Fe3++2H2O
B.2H2O2=2H2O+O2↑
C.Ag2O+H2O2=2Ag+O2↑+H2O
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
E.H2O2+MnSO4=MnO2+H2SO4
(3)用“双线桥法”标明以下反应中电子转移的方向和数目
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
您最近一年使用:0次
【推荐3】氧化剂和还原剂在生产生活中使用广泛。
(1)氯气可与溴化亚铁溶液反应:2FeBr2+3Cl2=2Br2+2FeCl3。
①其中氧化剂为_____________ (填化学式,下同),还原产物为_________ 。
②若消耗标准状况下2.24 LCl2,则转移电子的物质的量是_________ 。
(2)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路板,其化学原理如下:2FeCl3+Cu=CuCl2+2FeCl2。用双线桥法表示电子的转移情况:________ 。
(3)氯气也是常见的氧化剂。根据下列反应回答问题:
A.KClO3+6HCl=KCl+3Cl2↑+3H2O
B.5Cl2+I2+6H2O=2HIO3+10HCl
①上述反应说明KClO3、Cl2、HIO3的氧化性由强到弱的顺序为_________________ 。
②将过量的氯气通入滴有淀粉的KI溶液中,则可能出现的实验现象为_________ 。
(1)氯气可与溴化亚铁溶液反应:2FeBr2+3Cl2=2Br2+2FeCl3。
①其中氧化剂为
②若消耗标准状况下2.24 LCl2,则转移电子的物质的量是
(2)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路板,其化学原理如下:2FeCl3+Cu=CuCl2+2FeCl2。用双线桥法表示电子的转移情况:
(3)氯气也是常见的氧化剂。根据下列反应回答问题:
A.KClO3+6HCl=KCl+3Cl2↑+3H2O
B.5Cl2+I2+6H2O=2HIO3+10HCl
①上述反应说明KClO3、Cl2、HIO3的氧化性由强到弱的顺序为
②将过量的氯气通入滴有淀粉的KI溶液中,则可能出现的实验现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】实验室制取氯气的反应原理为: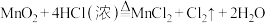 ,据此回答下列问题:
,据此回答下列问题:
(1)氧化剂与还原剂的个数之比_______ 。
(2)实验室制取氯气时,下列装置能达到相应实验目的的是_______ 。
(3)有一种“地康法”制取氯气的反应原理如下图所示:
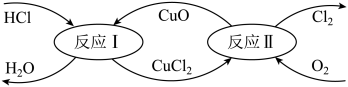
①写出反应Ⅰ的化学方程式_______ 。
②反应Ⅱ属于_______ 反应(填基本反应类型)。
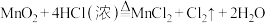 ,据此回答下列问题:
,据此回答下列问题:(1)氧化剂与还原剂的个数之比
(2)实验室制取氯气时,下列装置能达到相应实验目的的是
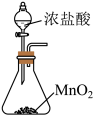 | 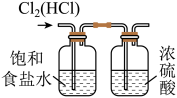 |  | 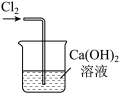 |
A.制备 | B.除去 中的HCl 中的HCl | C.收集 | D.尾气处理 |
(3)有一种“地康法”制取氯气的反应原理如下图所示:

①写出反应Ⅰ的化学方程式
②反应Ⅱ属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)实验室制取氯气反应的离子方程式为_________________________
(2)工业上制取漂白粉反应的化学方程式为_________________________
(3)配平:____ KClO3+____ H2C2O4+____ H2SO4→_____ K2SO4+____ ClO2↑+_____ CO2↑+_____ H2O
(4)二氧化碳气体通过一定量的过氧化钠固体,固体增重2.8g时,放出热量为Q KJ
则此反应的热化学方程式为_________________________
(5)标况下3.136 L Cl2通入0.1 L FeBr2溶液中,测得溶液Br-中消耗了三分之二,则此时总反应的离子方程式为_________________________
(2)工业上制取漂白粉反应的化学方程式为
(3)配平:
(4)二氧化碳气体通过一定量的过氧化钠固体,固体增重2.8g时,放出热量为Q KJ
则此反应的热化学方程式为
(5)标况下3.136 L Cl2通入0.1 L FeBr2溶液中,测得溶液Br-中消耗了三分之二,则此时总反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】海水中的卤素资源。地球是一颗蓝色星球,浩瀚的海洋覆盖了70%以上的地球表面,是蕴藏着极为丰富化学资源的“聚宝盆”,其中氯化物含量很高,氯和同族的氟、溴、碘、砹总称为卤素。
(1)氯气是一种重要的化工原料,可用以下几种方法制取氯气。
a.实验室可用二氧化锰与浓盐酸反应制氯气,写出其反应的离子方程式:___________ 。
b.工业上电解饱和食盐水制氯气,写出其反应的离子方程式:___________ 。
c.氯酸钾与浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比为___________ 。
(2)将氯气分别通入含下列离子的溶液中,离子浓度减小的是___________ 。
(3)氯气的水溶液即氯水,某学习小组拟用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是___________ 。

(1)氯气是一种重要的化工原料,可用以下几种方法制取氯气。
a.实验室可用二氧化锰与浓盐酸反应制氯气,写出其反应的离子方程式:
b.工业上电解饱和食盐水制氯气,写出其反应的离子方程式:
c.氯酸钾与浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比为
(2)将氯气分别通入含下列离子的溶液中,离子浓度减小的是
A. | B. | C. | D. |

| A.图1表示氯水pH随时间的变化 |
| B.图2表示溶液中氯离子浓度随时间的变化 |
| C.图3表示氯水的电导率随时间的变化 |
| D.图4表示液面上方氧气体积分数随时间的变化 |
您最近一年使用:0次



