如表是元素周期表的一部分,表中的每个编号代表一种短周期主族元素,请回答下列问题:
(1)元素②的原子结构示意图是______ 。
(2)比较元素原子半径大小:③______ ④(填“>”或“<”)。
(3)元素③位于元素周期表中第______ 周期VA族。
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式______ 。
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为______ 。
| 族 周期 | IA | 0 | ||||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ② | ③ | ④ | |||||||
| 3 | ⑤ | ⑥ | ||||||||
(2)比较元素原子半径大小:③
(3)元素③位于元素周期表中第
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为
2022高二·西藏·学业考试 查看更多[2]
更新时间:2023/09/23 19:24:12
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】请完成下列问题:
(1)画出氯原子结构示意图___________ 。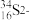 微粒中的质子数是
微粒中的质子数是___________ ,中子数是___________ 。
(2)49g 硫酸的物质的量为___________ mol,其完全电离产生 H+的个数为___________ 。组成硫酸的各原子中, 原子半径最大的是___________ 。
(3)写出实验室制氨气的化学方程式:___________
(1)画出氯原子结构示意图
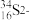 微粒中的质子数是
微粒中的质子数是(2)49g 硫酸的物质的量为
(3)写出实验室制氨气的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】现有六种微粒:
①镁原子;②硫离子;③氦原子;④核电荷数为+17,中子数为+18,核外有三个电子层,各层分别含有电子数为2,8,8;⑤核电荷数为+12,核外有两个电子层,各层含有电子数分别为2,8;⑥核电荷数为+17,质量数为37,核外有三个电子层,各层含有电子数分别为2,8,7。
(1)属于同种元素的是___________ ;
(2)核外电子排布相同的是___________ ;
(3)带电的微粒是___________ 。
①镁原子;②硫离子;③氦原子;④核电荷数为+17,中子数为+18,核外有三个电子层,各层分别含有电子数为2,8,8;⑤核电荷数为+12,核外有两个电子层,各层含有电子数分别为2,8;⑥核电荷数为+17,质量数为37,核外有三个电子层,各层含有电子数分别为2,8,7。
(1)属于同种元素的是
(2)核外电子排布相同的是
(3)带电的微粒是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】如表为元素周期表中的一部分,请回答下列问题:
(1)写出⑤元素的名称_______ 。
(2)写出③元素的离子结构示意图_______ 。
(3)④单质与水发生反应的离子方程式_______ 。
(4)写出⑥元素在周期表中的位置_______ 。
(5)比较单质氧化性的强弱⑤_______ ⑦(填”>”、”<”或”=”)。
| 项目 | I A | II A | III A | IV A | V A | VI A | VII A |
| 二 | ① | ② | ③ | ||||
| 三 | ④ | ⑤ | |||||
| 四 | ⑥ | ⑦ |
(1)写出⑤元素的名称
(2)写出③元素的离子结构示意图
(3)④单质与水发生反应的离子方程式
(4)写出⑥元素在周期表中的位置
(5)比较单质氧化性的强弱⑤
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,回答下列问题:
(1)写出③、⑤两种元素形成的化合物有两种,电子式分别是:__ ,___ 。
(2)写出①元素形成最简单有机物是__ ,它和氯气反应的一个方程式__ 。
(3)这些元素的最高价氧化物的对应水化物中__ 酸性最强;__ 碱性最强;能形成两性氢氧化物的元素是__ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(1)写出③、⑤两种元素形成的化合物有两种,电子式分别是:
(2)写出①元素形成最简单有机物是
(3)这些元素的最高价氧化物的对应水化物中
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】表中列出了A~R这9种元素在周期表中的位置:
请回答下列问题。
(1)表中部分元素的元素符号分别是:E____ ,H___ 。
(2)R的原子结构示意图为___ 。
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是___ 。
(4)A、B、C三种元素按原子半径由大到小的顺序排列为___ 。
(5)F元素与氢元素组成10个电子的分子的化学式为___ ,在常温下该分子可与B发生反应,所得溶液的pH____ 7(填“>”、“<”、“=”)。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
请回答下列问题。
(1)表中部分元素的元素符号分别是:E
(2)R的原子结构示意图为
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(4)A、B、C三种元素按原子半径由大到小的顺序排列为
(5)F元素与氢元素组成10个电子的分子的化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】德米特里·伊万诺维奇·门捷列夫是著名的俄国化学家,他对化学发展作出了卓越的贡献。请根据实际情况回答下列问题:
1.门捷列夫的突出贡献是
2.某元素的原子L层电子数比K层电子数多3个,与该元素同一主族的短周期元素是___________ 。
3.C、O、Na的原子半径从大到小的顺序为___________ 。
1.门捷列夫的突出贡献是
| A.提出原子学说 | B.发现元素周期律 | C.提出分子学说 | D.发现氧气 |
3.C、O、Na的原子半径从大到小的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】硫化钠广泛应用于染料工业。请完成下列各题:
(1)写出 的电子式
的电子式____________ ,比较 和
和 的熔点高低:
的熔点高低:
____  。
。
(2)O、S属于同主族元素,其单质的氧化性不同,用反应的化学方程式表示______________ ,O、S、 半径从大到小的顺序是
半径从大到小的顺序是_______________ 。
(1)写出
 的电子式
的电子式 和
和 的熔点高低:
的熔点高低:
 。
。(2)O、S属于同主族元素,其单质的氧化性不同,用反应的化学方程式表示
 半径从大到小的顺序是
半径从大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】下表是元素周期表的一部分,根据所给的10种元素,完成以下各小题。
(1)金属性最强的元素是____________  填元素符号
填元素符号 。
。
(2)最不活泼元素的原子结构示意图为___________ 。
(3)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是__________  填元素名称
填元素名称 。
。
(4)Na、Mg两种元素中,原子半径较大的是__________ 。
(5)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为___________ 。
(6)Na极易与水反应,该反应的化学方程式为____________ 。
(7)HF与HCl热稳定性较强的是_________ 。
(8)由碳与氢元素形成的最简单有机物的化学式为________ ,该物质中碳元素与氢元素的质量比为____________ ,其分子空间构型为____________ 。
(9)重氢( )和超重氢(
)和超重氢(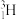 )两种核素都可用作制造氢弹的原料,它们所含中子数之比为
)两种核素都可用作制造氢弹的原料,它们所含中子数之比为___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | H | |||||||
2 | C | N | F | Ne | ||||
3 | Na | Mg | Al | S | Cl |
(1)金属性最强的元素是
 填元素符号
填元素符号 。
。 (2)最不活泼元素的原子结构示意图为
(3)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是
 填元素名称
填元素名称 。
。 (4)Na、Mg两种元素中,原子半径较大的是
(5)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为
(6)Na极易与水反应,该反应的化学方程式为
(7)HF与HCl热稳定性较强的是
(8)由碳与氢元素形成的最简单有机物的化学式为
(9)重氢(
 )和超重氢(
)和超重氢(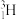 )两种核素都可用作制造氢弹的原料,它们所含中子数之比为
)两种核素都可用作制造氢弹的原料,它们所含中子数之比为
您最近一年使用:0次




