下表是元素周期表的一部分,回答下列问题:
(1)写出③、⑤两种元素形成的化合物有两种,电子式分别是:__ ,___ 。
(2)写出①元素形成最简单有机物是__ ,它和氯气反应的一个方程式__ 。
(3)这些元素的最高价氧化物的对应水化物中__ 酸性最强;__ 碱性最强;能形成两性氢氧化物的元素是__ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(1)写出③、⑤两种元素形成的化合物有两种,电子式分别是:
(2)写出①元素形成最简单有机物是
(3)这些元素的最高价氧化物的对应水化物中
更新时间:2020-06-29 13:47:49
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】如图是元素周期表的一部分,表中的①~⑩中元素,填空回答:
用元素符号 或化学式 回答下列问题:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为______________ 。
(2)氧化性最强的单质是_____________ 。
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是_____________ ,碱性最强的是_____________ ,呈两性的氢氧化物是_____________ 。
(4)写出①②③⑦对应的氢化物的稳定性由强到弱的是_____________ ,
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
用
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为
(2)氧化性最强的单质是
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是
(4)写出①②③⑦对应的氢化物的稳定性由强到弱的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】元素周期表(律)在学习、 研究和生产实践中有很重要的作用。图表为元素周期表的一部分,回答下列问题
(1)⑦的元素名称为______________ 。
(2)元素①~⑧ 中金属性最强的是____________ ( 填元素符号)。
(3)比较②和⑤两种元素原子半径的大小:②______ ⑤(填“ >”或“< ”)。
(4)⑨ 的原子序数是_________ 。
(5)元素④~⑧中,最高价氧化物属于两性氧化物的是________ (填元素符号)。
族 周期 | ⅠA | 0 | |||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ② | ③ | |||||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | …… | ⑨ |
(1)⑦的元素名称为
(2)元素①~⑧ 中金属性最强的是
(3)比较②和⑤两种元素原子半径的大小:②
(4)⑨ 的原子序数是
(5)元素④~⑧中,最高价氧化物属于两性氧化物的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】金属Na、Mg、Al有广泛的应用。
(1)Al在元素周期表中的位置是______ 。
(2)金属镁可以用来生产金属铀(元素符号是U): ,该反应中,作为还原剂的物质是
,该反应中,作为还原剂的物质是______ (填化学式,下同),被还原的物质是______ 。
(3)为比较Na、Mg、Al的金属性,进行了如下实验(金属固体的表面积都相同):
由实验1和实验2得出的结论是:金属性,______ >______ >______ (填元素符号),用原子结构理论解释:同周期元素从左到右,______ 。
(4)写出Na和Al最高价氧化物的水化物相互反应的离子反应方程式______ 。
(1)Al在元素周期表中的位置是
(2)金属镁可以用来生产金属铀(元素符号是U):
 ,该反应中,作为还原剂的物质是
,该反应中,作为还原剂的物质是(3)为比较Na、Mg、Al的金属性,进行了如下实验(金属固体的表面积都相同):
| 实验1 | 实验2 |
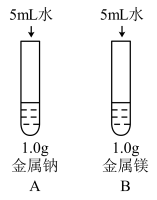 |  |
| 钠与水反应剧烈,镁与水反应缓慢 | 镁与盐酸反应剧烈,铝与盐酸反应缓慢 |
由实验1和实验2得出的结论是:金属性,
(4)写出Na和Al最高价氧化物的水化物相互反应的离子反应方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】如图是元素周期表的框架,请在表中①~⑩元素中回答问题

请用化学语言回答下列问题:
(1)在表中④、⑤、⑥三种元素的简单离子半径由大到小的顺序为______。
(2)其中⑤与⑦两元素的最高价氧化物的水化物反应的离子方程式为______。
(3)⑧与⑩两种元素非金属较强的是______,请用一个离子方程式证明该结论______。
(4)①与③的两种单质可以在金属铂做电极时构成一种对环境友好的燃料电池,电解质为⑨的最高价氧化物的水化物,请书写出正极反应式______,电池工作时阴离子定向移动到______极(填正或负)。
(5)元素①与⑧的两种单质在一定条件下可反应生成一种化合物甲,已知下表中的数据是破坏1mol物质中的化学键所吸收的能量(kJ),则生成1mol甲时释放的能量为______kJ。

请用化学语言回答下列问题:
(1)在表中④、⑤、⑥三种元素的简单离子半径由大到小的顺序为______。
(2)其中⑤与⑦两元素的最高价氧化物的水化物反应的离子方程式为______。
(3)⑧与⑩两种元素非金属较强的是______,请用一个离子方程式证明该结论______。
(4)①与③的两种单质可以在金属铂做电极时构成一种对环境友好的燃料电池,电解质为⑨的最高价氧化物的水化物,请书写出正极反应式______,电池工作时阴离子定向移动到______极(填正或负)。
(5)元素①与⑧的两种单质在一定条件下可反应生成一种化合物甲,已知下表中的数据是破坏1mol物质中的化学键所吸收的能量(kJ),则生成1mol甲时释放的能量为______kJ。
| 化学键 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】有7种短周期元素,其原子半径及主要化合价如下:
完成下列填空:
(1)A在元素周期表中的位置是_______ 。
(2)上述7种元素形成的简单离子中,离子半径最大是_______ (用离子符号表示)
(3)甲是由G、H两种元素组成的18e-分子,用电子式表示其形成过程_______ 。
(4)用一个化学方程式表示E元素的非金属性比D强_______ 。
| 元素代号 | A | B | D | E | F | G | H |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
| 主要化合价 | +1 | +3 | +6,-2 | +7,-1 | +5,-3 | -2 | +1 |
完成下列填空:
(1)A在元素周期表中的位置是
(2)上述7种元素形成的简单离子中,离子半径最大是
(3)甲是由G、H两种元素组成的18e-分子,用电子式表示其形成过程
(4)用一个化学方程式表示E元素的非金属性比D强
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】下列关于元素周期表及周期律的叙述,其中错误的是
| A.一般在过渡元素中寻找一些化学反应新型催化剂 |
| B.氯化氢HCl是比溴化氢HBr稳定的气体 |
| C.研制农药通常考虑含有元素周期表右上角元素(氟、氯、硫、磷等)的有机物 |
| D.按F2→I2的顺序单质氧化性逐渐减弱,故前面的卤素单质可将后面的卤素从它们的盐溶液里置换出来 |
| E.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
| F.砹(At)为ⅦA元素,推测单质砹为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸 |
| G.ⅠA族元素全部是金属元素,第ⅦA族位于元素周期表第7纵列 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】元素周期律
(1)内容:元素的性质随着原子序数的递增而呈__________ 变化。
(2)实质:元素性质的周期性变化是元素原子的________________________ 的必然结果。
(3)同周期从左到右的结构与性质的递变性
(1)内容:元素的性质随着原子序数的递增而呈
(2)实质:元素性质的周期性变化是元素原子的
(3)同周期从左到右的结构与性质的递变性
| 原子结构 | 核电荷数 | |
| 电子层数 | ||
| 原子半径 | ||
| 性质 | 化合价 | |
| 元素的金属性和非金属性 | ||
| 离子的氧化性、还原性 | ||
| 气态氢化物的稳定性、还原性 | ||
| 最高价氧化物对应的水化物的酸碱性 |
您最近一年使用:0次




