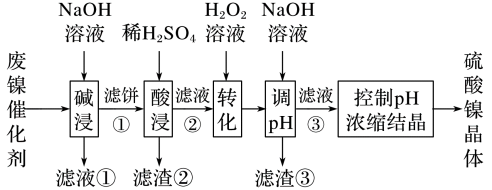
金属Na、Mg、Al有广泛的应用。
(1)Al在元素周期表中的位置是______ 。
(2)金属镁可以用来生产金属铀(元素符号是U): ,该反应中,作为还原剂的物质是
,该反应中,作为还原剂的物质是______ (填化学式,下同),被还原的物质是______ 。
(3)为比较Na、Mg、Al的金属性,进行了如下实验(金属固体的表面积都相同):
由实验1和实验2得出的结论是:金属性,______ >______ >______ (填元素符号),用原子结构理论解释:同周期元素从左到右,______ 。
(4)写出Na和Al最高价氧化物的水化物相互反应的离子反应方程式______ 。
(1)Al在元素周期表中的位置是
(2)金属镁可以用来生产金属铀(元素符号是U):
 ,该反应中,作为还原剂的物质是
,该反应中,作为还原剂的物质是(3)为比较Na、Mg、Al的金属性,进行了如下实验(金属固体的表面积都相同):
| 实验1 | 实验2 |
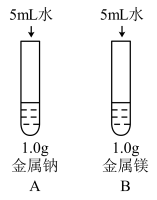 |  |
| 钠与水反应剧烈,镁与水反应缓慢 | 镁与盐酸反应剧烈,铝与盐酸反应缓慢 |
由实验1和实验2得出的结论是:金属性,
(4)写出Na和Al最高价氧化物的水化物相互反应的离子反应方程式
更新时间:2022-12-14 21:26:09
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】氧化还原反应在生产、生活中具有广泛的用途、贯穿古今。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用右下图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:________________,其中水为________剂。
(2)过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:
①下列反应中,H2O2既体现氧化性又体现还原性的反应是( )
②保存过氧化氢的试剂瓶上最适合贴上的一个标签是( )(填序号)

(3)焊接铜器时,可先用NH4Cl 除去其表面的氧化铜再进行焊接,该反应可表示为:
4CuO + 2NH4Cl △ 3Cu + CuCl2 + N2↑+ 4H2O
①用双线桥标明电子转移的方向和数目。
②该反应中,被氧化的元素是 ,氧化剂是 。
③还原剂与氧化产物的物质的量之比为 。
④反应中若产生0.2 mol的氮气,则有 mol的电子转移。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用右下图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:________________,其中水为________剂。
(2)过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:
①下列反应中,H2O2既体现氧化性又体现还原性的反应是( )
| A.Na2O2+2HCl═2NaCl+H2O2 | B.Ag2O+H2O2═2Ag+O2↑+H2O |
| C.2H2O2═2H2O +O2↑ | |
| D.3H2O2+Cr2(SO4)3 +10KOH═2K2CrO4+3K2SO4+8H2O | |

(3)焊接铜器时,可先用NH4Cl 除去其表面的氧化铜再进行焊接,该反应可表示为:
4CuO + 2NH4Cl △ 3Cu + CuCl2 + N2↑+ 4H2O
①用双线桥标明电子转移的方向和数目。
②该反应中,被氧化的元素是 ,氧化剂是 。
③还原剂与氧化产物的物质的量之比为 。
④反应中若产生0.2 mol的氮气,则有 mol的电子转移。
您最近一年使用:0次
【推荐2】(1)根据反应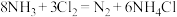 ,回答下列问题:
,回答下列问题:
①用双线桥法标出该反应中电子转移的方向和数目:______ 。
②该反应中______ 元素被还原,______ 元素被氧化。
③在该反应中,若有 电子发生转移,在标准状况下,可生成
电子发生转移,在标准状况下,可生成 的体积为
的体积为_____ L。
(2)配平化学方程式且回答下列问题:
①______ 
______ 
___ 
_____ 
___ Cl2 ___ H2O
②若生成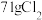 ,则被氧化的HCl是
,则被氧化的HCl是_________ mol,
(3)已知反应:2H2S+H2SO3=2H2O +3S,若氧化产物比还原产物多 ,则同时会生成水的质量为
,则同时会生成水的质量为 ______ g。
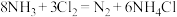 ,回答下列问题:
,回答下列问题:①用双线桥法标出该反应中电子转移的方向和数目:
②该反应中
③在该反应中,若有
 电子发生转移,在标准状况下,可生成
电子发生转移,在标准状况下,可生成 的体积为
的体积为(2)配平化学方程式且回答下列问题:
①




②若生成
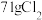 ,则被氧化的HCl是
,则被氧化的HCl是(3)已知反应:2H2S+H2SO3=2H2O +3S,若氧化产物比还原产物多
 ,则同时会生成水的质量为
,则同时会生成水的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)已知下列十种物质①CH3COOH②Cu③NO④干冰⑤硫酸⑥Ba(OH)2⑦Fe(OH)3胶体⑧液氨⑨稀硝酸⑩NaHSO4。根据上述提供的物质,回答下列问题
①属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
②在熔融状态下不导电而在水溶液下导电的电解质是___________ 。
③实验室制备⑦的操作是___________
(2)在2Fe3++2I﹣=I2+2Fe2+反应中,___________ 是氧化剂,___________ 发生氧化反应。
①属于电解质的是
②在熔融状态下不导电而在水溶液下导电的电解质是
③实验室制备⑦的操作是
(2)在2Fe3++2I﹣=I2+2Fe2+反应中,
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】请根据下图中的信息回答问题。
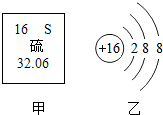
(1)硫属于________ (填“金属”或“非金属”)元素;硫元素的原子序数为_________ 。
(2)图乙所表示粒子的化学符号是____________ 。
(3)硫在空气中燃烧的化学方程式为____________________ 。

(1)硫属于
(2)图乙所表示粒子的化学符号是
(3)硫在空气中燃烧的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在1—18号元素中,选择合适的选项回答下列问题
1.写出①和②的非金属性较强的是( )
2.写出④的最高价氧化物化学式( )
3.写出③和⑤的最高价氧化物对应水化物反应的离子方程式( )
4.③和④两种元素的最高价氧化物对应水化物中碱性较强的是
5.写出③的单质在②单质中燃烧的现象()
6.①元素在周期表中的位置是( )
7.②和⑤两种元素中原子半径较大的是( )
8.下列化学用语表达不正确 的是( )
9.⑤和⑥形成的气态氢化物最稳定的是( )
10.④的氧化物类型为 ( )
| ① | ② | ||||||||||||||
| ③ | ④ | ⑤ | ⑥ |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
| A.RO | B.R2O | C.R2O3 | D.RO2 |
| A.2NaOH+H2SO4=Na2SO4+2H2O | B.H+ +OH- =H2O |
| C.NaOH+H2SO4=Na2SO4+H2O | D.2OH- +H2SO4=SO42- +2H2O |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
| A.白色固体 | B.淡黄色固体 | C.浅紫色火焰 | D.苍白色火焰 |
| A.第二周期第四主族 | B.第二周期第IV主族 |
| C.第二周期第IVA族 | D.第二周期第VA族 |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
A.氟离子的结构示意图: | B.水分子的电子式: |
| C.二氧化碳的结构式:O=C=O | D.硫酸钠的电离方程式:Na2SO4=2Na++SO42- |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
| A.酸性氧化物,非金属氧化物 | B.两性氧化物,金属氧化物 |
| C.碱性氧化物,金属氧化物 | D.酸性氧化物,金属氧化物 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下表是周期表中的一部分,根据A-I在周期表中的位置,第(1)~(4)小题用元素符号或化学式 回答,(5)~(8)小题按题目要求回答。
(1)表中元素,化学性质最不活泼的是_______ ,只有负价而无正价的是_______ ,氧化性最强的单质是_______ ,还原性最强的单质是_______ 。
(2)最高价氧化物的水化物碱性最强的是_______ ,酸性最强的是_______ ,呈两性的是_______ 。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的_______ 。
(4)在B、C、E、F、G、H中,原子半径最大的是_______ 。
(5)A和D组成化合物的电子式_______ 。
(6)用电子式表示B和H组成化合物的形成过程_______ 。
(7)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式_______
族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在B、C、E、F、G、H中,原子半径最大的是
(5)A和D组成化合物的电子式
(6)用电子式表示B和H组成化合物的形成过程
(7)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】化学工业为疫情防控提供了强有力的物质支撑。氯及其化合物既是重要化工原料,又是广泛使用的高效灭菌消毒剂。回答下列问题:
(1)用氯气制备漂白液的离子方程式是______ 。
(2)TCCA是一种高效含氯消毒漂白剂,贮运稳定,在水中释放有效氯时间长,应用于游泳池等公共场合,其分子结构如图所示:

已知:X、Y、Z、W属于原子序数递增的短周期元素,Z核外最外层电子数是电子层数的3倍。
①TCCA的分子式是______ 。
②X、Y、Z对应简单氢化物中热稳定性最强的是______ (用氢化物的化学式表示)。
(3)ClO2和NaClO2均为重要的杀菌消毒剂,将ClO2通入到NaOH和H2O2混合溶液中,可制备NaClO2。
资料:NaClO2晶体易溶于水,难溶于乙醇。NaClO2饱和溶液在温度低于38 ℃时析出NaClO2·3H2O晶体,高于38 ℃时析出NaClO2晶体,高于60 ℃时NaClO2分解成NaClO3和NaCl。
① 写出由ClO2制备NaClO2的离子方程式______ 。
② 从上述NaClO2溶液获得干燥的NaClO2晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体析出后,______ ,______ ,低于60℃干燥,得到NaClO2晶体 (补全实验步骤)。
(1)用氯气制备漂白液的离子方程式是
(2)TCCA是一种高效含氯消毒漂白剂,贮运稳定,在水中释放有效氯时间长,应用于游泳池等公共场合,其分子结构如图所示:

已知:X、Y、Z、W属于原子序数递增的短周期元素,Z核外最外层电子数是电子层数的3倍。
①TCCA的分子式是
②X、Y、Z对应简单氢化物中热稳定性最强的是
(3)ClO2和NaClO2均为重要的杀菌消毒剂,将ClO2通入到NaOH和H2O2混合溶液中,可制备NaClO2。
资料:NaClO2晶体易溶于水,难溶于乙醇。NaClO2饱和溶液在温度低于38 ℃时析出NaClO2·3H2O晶体,高于38 ℃时析出NaClO2晶体,高于60 ℃时NaClO2分解成NaClO3和NaCl。
① 写出由ClO2制备NaClO2的离子方程式
② 从上述NaClO2溶液获得干燥的NaClO2晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体析出后,
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)写出下列物质的电子式:
NaCl____________ ;HCl_____________
(2)第三周期元素中的最高价氧化物对应的水化物中,酸性最强的是________ ,碱性最强的是_____________ ,呈两性的氢氧化物是_______________ 。半径最大的原子是__________ ,氢化物最稳定的元素是___________ 。
(3)硫元素位于元素周期表中______ 周期_______ 族,气态氢化物的化学式是____________ ,最高价氧化物对应水化物的化学式_________________
NaCl
(2)第三周期元素中的最高价氧化物对应的水化物中,酸性最强的是
(3)硫元素位于元素周期表中
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)元素最高正化合价为+6,其负化合价为____ ,某元素R与氢形成的气态氢化物的化学式为RH3,其最高价氧化物的化学式为___________ 。
(2)下列各题中有关物质的比较,请用“>”、“<”、“=”填空
酸性: H3PO4____ HNO3 ,H2SO4______ HClO4
热稳定性:CH4_____ NH3 ,HCl____ HI
(3)1~18号元素中,最外层电子数是次外层电子数二倍的元素是______ ,原子结构示意图_______________ ,能与氧形成的氧化物的化学式________ 、_______ 。
(2)下列各题中有关物质的比较,请用“>”、“<”、“=”填空
酸性: H3PO4
热稳定性:CH4
(3)1~18号元素中,最外层电子数是次外层电子数二倍的元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据如图实验装置,请回答:___________ 。
(2)检查装置A气密性的方法是夹紧止水夹,___________ ,则气密性良好。
(3)用H2O2制取氧气,选择的发生装置为___________ (填字母),反应的化学方程式为___________ 。
(4)用装置F和另一仪器(除导管外)收集并测量O2体积,另一仪器名称为___________ ,在F中气体应从导管___________ (填“b”或“c”)端通入。
(5)实验室里,常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷。
①选择的发生装置为___________ (填字母)。用装置E收集甲烷,利用了甲烷___________ 的物理性质;用装置C而不用装置D收集甲烷,原因是___________ 。
②设计实验证明CH4中含有氢元素:检验其纯度后,___________ 。

(2)检查装置A气密性的方法是夹紧止水夹,
(3)用H2O2制取氧气,选择的发生装置为
(4)用装置F和另一仪器(除导管外)收集并测量O2体积,另一仪器名称为
(5)实验室里,常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷。
①选择的发生装置为
②设计实验证明CH4中含有氢元素:检验其纯度后,
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】三草酸合铁酸钾晶体 可用于摄影和蓝色印刷。某小组将无水三草酸合铁酸钾
可用于摄影和蓝色印刷。某小组将无水三草酸合铁酸钾 在一定条件下加热分解,对所得气体产物和固体产物进行探究。
在一定条件下加热分解,对所得气体产物和固体产物进行探究。
(1)三草酸合铁酸钾晶体 属于
属于___________ (填“混合物、酸、碱或盐”);已知该物质中铁的化合价为 ,则该物质中C的化合价为
,则该物质中C的化合价为___________ 。
Ⅰ.气体产物成分探究
(2)将气体产物依次通过(A)澄清石灰水(过量)、(B)浓硫酸、(C)灼热氧化铜、(D)澄清石灰水,观察到A、D中澄清石灰水均变浑浊,C中有红色固体生成,则气体产物的成分是___________ 。(填化学式)
Ⅱ.固体产物成分探究
(3)该小组同学查阅资料后推知,固体产物中铁元素以 和Fe存在,完成实验设计。
和Fe存在,完成实验设计。
实验前,先预测 的性质。用新制纯净的
的性质。用新制纯净的 粉末,完成以下实验设计表格:(已知铁元素的化合价有0、
粉末,完成以下实验设计表格:(已知铁元素的化合价有0、 、
、 ,稀溶液中
,稀溶液中 、
、 的颜色分别为浅绿色、黄色)
的颜色分别为浅绿色、黄色)
限选 试剂:炭粉、酸性 溶液、稀盐酸、
溶液、稀盐酸、 溶液、澄清石灰水。
溶液、澄清石灰水。
 可用于摄影和蓝色印刷。某小组将无水三草酸合铁酸钾
可用于摄影和蓝色印刷。某小组将无水三草酸合铁酸钾 在一定条件下加热分解,对所得气体产物和固体产物进行探究。
在一定条件下加热分解,对所得气体产物和固体产物进行探究。(1)三草酸合铁酸钾晶体
 属于
属于 ,则该物质中C的化合价为
,则该物质中C的化合价为Ⅰ.气体产物成分探究
(2)将气体产物依次通过(A)澄清石灰水(过量)、(B)浓硫酸、(C)灼热氧化铜、(D)澄清石灰水,观察到A、D中澄清石灰水均变浑浊,C中有红色固体生成,则气体产物的成分是
Ⅱ.固体产物成分探究
(3)该小组同学查阅资料后推知,固体产物中铁元素以
 和Fe存在,完成实验设计。
和Fe存在,完成实验设计。实验前,先预测
 的性质。用新制纯净的
的性质。用新制纯净的 粉末,完成以下实验设计表格:(已知铁元素的化合价有0、
粉末,完成以下实验设计表格:(已知铁元素的化合价有0、 、
、 ,稀溶液中
,稀溶液中 、
、 的颜色分别为浅绿色、黄色)
的颜色分别为浅绿色、黄色) 溶液、稀盐酸、
溶液、稀盐酸、 溶液、澄清石灰水。
溶液、澄清石灰水。预测的 性质 性质 | 预测的依据 | 预期现象 |
| 能与 | 从组成看, 属于碱性氧化物 属于碱性氧化物 | 固体溶解,溶液为浅绿色 |
| 能与 | ||
| 能与炭粉反应 |
您最近一年使用:0次