1 . 无机物A~C在一定条件下的转化关系如图所示,A为淡黄色的固体化合物,B是地壳中含量最多的金属元素的单质,请回答下列问题:
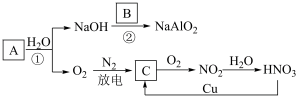
(1)写出A的化学式______ ,C的化学式______ 。
(2)写出稀HNO3与Cu反应生成C的离子方程式________ ;在该反应中,HNO3表现出酸性和强______ (填“氧化性”或“还原性”)。
(3)写出反应②的化学方程式________ 。

(1)写出A的化学式
(2)写出稀HNO3与Cu反应生成C的离子方程式
(3)写出反应②的化学方程式
您最近一年使用:0次
2 . 乙烯的产量可以用来衡量一个国家的石油化工发展水平,A和B是生活中两种常见的有机物,C是一种具有香味的物质,且碳原子数是A的两倍。现以乙烯为主要原料合成C,其合成路线如图所示,请回答下列问题:
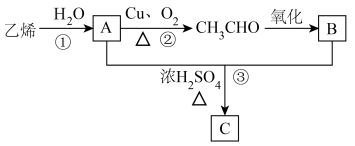
(1)乙烯的结构简式:______ 。
(2)A分子中含有的官能团名称为______ 。
(3)②的反应类型为______ ,③的反应类型为______ 。
(4)写出反应①的化学方程式_______ 。

(1)乙烯的结构简式:
(2)A分子中含有的官能团名称为
(3)②的反应类型为
(4)写出反应①的化学方程式
您最近一年使用:0次
3 . Ⅰ.已知A和B两支试管的溶液中共含有 、
、 、
、 、
、 、
、 、
、 六种离子,向试管B的溶液中滴入酚酞,溶液呈粉红色。请回答下列问题:
六种离子,向试管B的溶液中滴入酚酞,溶液呈粉红色。请回答下列问题:
(1)试管B中含有的离子为_______ ;
(2)若向试管A的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是_______ (填化学式);
(3)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,该物质可以用作_______ (列举一种用途即可),混合过程中发生反应的离子方程式为:_______ 、_______ 。
Ⅱ.甲同学用如下装置模拟“侯氏制碱法”制纯碱。
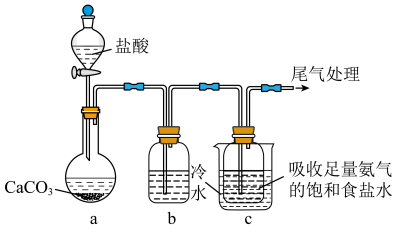
(4)c中饱和食盐水事先吸收足量 的原因是
的原因是_______ ;
(5)装置c中发生反应的离子反应方程式为_______ 。
 、
、 、
、 、
、 、
、 、
、 六种离子,向试管B的溶液中滴入酚酞,溶液呈粉红色。请回答下列问题:
六种离子,向试管B的溶液中滴入酚酞,溶液呈粉红色。请回答下列问题:(1)试管B中含有的离子为
(2)若向试管A的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(3)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,该物质可以用作
Ⅱ.甲同学用如下装置模拟“侯氏制碱法”制纯碱。

(4)c中饱和食盐水事先吸收足量
 的原因是
的原因是(5)装置c中发生反应的离子反应方程式为
您最近一年使用:0次
4 . 含氯消毒剂在生产生活中有着广泛的用途,这些都与氯气息息相关。
Ⅰ.实验室制备和收集氯气的常用装置如图:
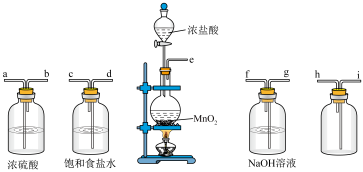
(1)在实验过程中饱和食盐水的作用是_______ 。
(2)实验装置接口的连接顺序为e→_______ →g→f;
(3)工业上常将 通入石灰乳中来制备漂白粉。使用漂白粉时,一般先将其溶于水形成溶液,在空气中放置一段时间后再使用,这样做的原因是(用化学方程式表示)
通入石灰乳中来制备漂白粉。使用漂白粉时,一般先将其溶于水形成溶液,在空气中放置一段时间后再使用,这样做的原因是(用化学方程式表示)_______ 。
Ⅱ.为探究NaCl对 在水中溶解度的影响,某兴趣小组同学进行实验,测定常温下
在水中溶解度的影响,某兴趣小组同学进行实验,测定常温下 在不同浓度NaCl溶液中的溶解度,结果如下表所示:
在不同浓度NaCl溶液中的溶解度,结果如下表所示:
已知: 在常温下水中的溶解度为
在常温下水中的溶解度为 。
。
(4)根据实验数据,当NaCl溶液浓度大于_______  时,NaCl溶液浓度增加对
时,NaCl溶液浓度增加对 在水中溶解度无明显影响;
在水中溶解度无明显影响;
(5)为进一步探究食盐水中哪些微粒能降低 在水中的溶解度,该小组同学取三支试管,分别加入一定浓度NaCl溶液、
在水中的溶解度,该小组同学取三支试管,分别加入一定浓度NaCl溶液、 溶液和KCl溶液,通入足量
溶液和KCl溶液,通入足量 后,测其溶解度,结果如下表所示:
后,测其溶解度,结果如下表所示:
请回答下列问题:
① ,b=
,b=_______  ,c=
,c=_______  ;
;
②设置实验2的目的是_______ ;
③对比实验1和实验3可以得到的结论是_______ ;
④实验结论:食盐水中能够降低 在水中溶解度的微粒有
在水中溶解度的微粒有_______ 。
Ⅰ.实验室制备和收集氯气的常用装置如图:

(1)在实验过程中饱和食盐水的作用是
(2)实验装置接口的连接顺序为e→
(3)工业上常将
 通入石灰乳中来制备漂白粉。使用漂白粉时,一般先将其溶于水形成溶液,在空气中放置一段时间后再使用,这样做的原因是(用化学方程式表示)
通入石灰乳中来制备漂白粉。使用漂白粉时,一般先将其溶于水形成溶液,在空气中放置一段时间后再使用,这样做的原因是(用化学方程式表示)Ⅱ.为探究NaCl对
 在水中溶解度的影响,某兴趣小组同学进行实验,测定常温下
在水中溶解度的影响,某兴趣小组同学进行实验,测定常温下 在不同浓度NaCl溶液中的溶解度,结果如下表所示:
在不同浓度NaCl溶液中的溶解度,结果如下表所示: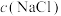 / / | 0.50 | 1.00 | 2.00 | 4.50 | 5.00 |
 溶解度( 溶解度( ) ) | 0.0658 | 0.0580 | 0.0490 | 0.0360 | 0.0360 |
 在常温下水中的溶解度为
在常温下水中的溶解度为 。
。(4)根据实验数据,当NaCl溶液浓度大于
 时,NaCl溶液浓度增加对
时,NaCl溶液浓度增加对 在水中溶解度无明显影响;
在水中溶解度无明显影响;(5)为进一步探究食盐水中哪些微粒能降低
 在水中的溶解度,该小组同学取三支试管,分别加入一定浓度NaCl溶液、
在水中的溶解度,该小组同学取三支试管,分别加入一定浓度NaCl溶液、 溶液和KCl溶液,通入足量
溶液和KCl溶液,通入足量 后,测其溶解度,结果如下表所示:
后,测其溶解度,结果如下表所示:| 实验编号 | 1 | 2 | 3 |
| 实验装置 |  |  |  |
 溶解度 溶解度 | 0.0580 | 0.0800 | 0.0665 |
①
 ,b=
,b= ,c=
,c= ;
;②设置实验2的目的是
③对比实验1和实验3可以得到的结论是
④实验结论:食盐水中能够降低
 在水中溶解度的微粒有
在水中溶解度的微粒有
您最近一年使用:0次
解题方法
5 . 以下是实验室制取氯气的装置,请回答下列问题:

(1)仪器A的名称是_______ 。
(2)请补全实验室制取氯气的化学方程式:
_______  ,该反应中的氧化剂为
,该反应中的氧化剂为_______ (填化学式)。
(3)图中饱和食盐水的作用是_______ ﹔浓硫酸的作用是_______ 。
(4)烧杯F中氢氧化钠溶液的作用是_______ ;其中发生反应的化学方程式为_______ 。

(1)仪器A的名称是
(2)请补全实验室制取氯气的化学方程式:

 ,该反应中的氧化剂为
,该反应中的氧化剂为(3)图中饱和食盐水的作用是
(4)烧杯F中氢氧化钠溶液的作用是
您最近一年使用:0次
6 . 下表列出了5种元素在周期表中的位置。
回答下列问题:
(1)①的元素符号是_______ ,⑤的元素符号是_______
(2)以上元素中,金属性最强的是_______ (填元素符号)。
(3)④元素的最高价氧化物对应的水化物呈_______ 性(填“酸”或“碱”或“两”)。
(4)③④⑤对应元素中原子半径最小的是_______ (填元素符号)。
(5)元素③与元素②形成的化合物,可用于呼吸面具或潜水艇中作为氧气的来源,它的化学式是_______ 。
(6)少量元素③的单质通常保存在_______ 中(填“煤油”或“水”)。
(7)元素①的氢化物与元素②的氢化物更稳定的是_______ (填化学式)。
族 周期 | I A | 0 | ||||||
| 1 | H | Ⅱ A | Ⅲ A | Ⅳ A | V A | Ⅵ A | Ⅶ A | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ |
(1)①的元素符号是
(2)以上元素中,金属性最强的是
(3)④元素的最高价氧化物对应的水化物呈
(4)③④⑤对应元素中原子半径最小的是
(5)元素③与元素②形成的化合物,可用于呼吸面具或潜水艇中作为氧气的来源,它的化学式是
(6)少量元素③的单质通常保存在
(7)元素①的氢化物与元素②的氢化物更稳定的是
您最近一年使用:0次
解题方法
7 . 下图所示烧瓶中充满了NH3,打开止水夹,挤压胶头滴管,使水进入烧瓶。烧瓶中出现红色喷泉。回答下列问题。
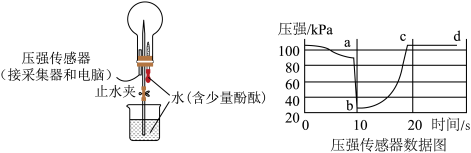
(1)NH3是___________ 气味的气体。
(2)由压力传感器的数据图可知,b点压强最小,烧瓶中压强变小的原因是___________ 。线段cd显示压强不再变化,说明___________ 。
(3)下列方程式中,能解释喷泉呈红色的原因是___________ (填序号)。
a.NH3+H2O NH3·H2O
NH3·H2O NH
NH +OH-
+OH-
b.NH +H2O
+H2O NH3·H2O+H+
NH3·H2O+H+
c.H2O H++OH-
H++OH-
(4)实验室常用加热NH4Cl和Ca(OH)2混合固体的方法制备NH3,该反应的化学方程式为___________ 。

(1)NH3是
(2)由压力传感器的数据图可知,b点压强最小,烧瓶中压强变小的原因是
(3)下列方程式中,能解释喷泉呈红色的原因是
a.NH3+H2O
 NH3·H2O
NH3·H2O NH
NH +OH-
+OH-b.NH
 +H2O
+H2O NH3·H2O+H+
NH3·H2O+H+c.H2O
 H++OH-
H++OH-(4)实验室常用加热NH4Cl和Ca(OH)2混合固体的方法制备NH3,该反应的化学方程式为
您最近一年使用:0次
解题方法
8 . 元素①~⑤在元素周期表中的位置如下表所示:
回答下列问题:
(1)原子半径最大的是___________ (填元素符号);简单离子半径最小的是___________ (填离子符号)。
(2)①、④简单气态氢化物的稳定性较强的是___________ (填化学式)。
(3)②、③最高价氧化物对应水化物之间反应的离子方程式为___________ 。
(4)④、⑤最高价氧化物对应水化物的酸性较强的是___________ (填化学式)。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ||||
(1)原子半径最大的是
(2)①、④简单气态氢化物的稳定性较强的是
(3)②、③最高价氧化物对应水化物之间反应的离子方程式为
(4)④、⑤最高价氧化物对应水化物的酸性较强的是
您最近一年使用:0次
解题方法
9 . 电子工业中常用覆铜板为材料,利用FeCl3溶液做“腐蚀液”制作印刷电路板。从废腐蚀液(含FeCl3,FeCl2和CuCl2)中回收Cu并实现FeCl3溶液循环再利用,其工艺流程如下:

回答下列问题:
(1)工业上制作印刷电路板时发生的化学反应方程式为_______ 。
(2)操作方法①为_______ ,固体A的成分为_______ (填化学式)。
(3)实验室检验溶液A中是否含有FeCl3的试剂为_______ 溶液(填化学式)。
(4)溶液A中加入NaOH溶液时产生的实验现象为_______ 。
(5)若回收过程中取废腐蚀液V L,回收到a g Cu,则废腐蚀液中Cu2+的物质的量浓度为_______ mol/L(用含a和V的表达式表示)。

回答下列问题:
(1)工业上制作印刷电路板时发生的化学反应方程式为
(2)操作方法①为
(3)实验室检验溶液A中是否含有FeCl3的试剂为
(4)溶液A中加入NaOH溶液时产生的实验现象为
(5)若回收过程中取废腐蚀液V L,回收到a g Cu,则废腐蚀液中Cu2+的物质的量浓度为
您最近一年使用:0次
10 . 二氧化硫在食品加工中有着重要作用,但过量使用可能导致食品中残留量超标,会对人体健康造成不利影响。实验室可用下图装置制取并探究二氧化硫的性质。回答下列问题:

(1)①中试管内发生反应的化学方程式为_______ ,该反应中体现了浓H2SO4的酸性和_______ 性。在标准状况下生成224 mLSO2时,消耗的H2SO4的物质的量为_______ mol。
(2)实验过程中铜丝可以上下抽动,其作用为_______ 。
(3)②中试管内的溴水褪色,SO2表现出_______ 性,③中试管内的石蕊溶液出现的实验现象为_______ 。
(4)浸有NaOH溶液的棉团的作用为_______ 。

(1)①中试管内发生反应的化学方程式为
(2)实验过程中铜丝可以上下抽动,其作用为
(3)②中试管内的溴水褪色,SO2表现出
(4)浸有NaOH溶液的棉团的作用为
您最近一年使用:0次



