名校
解题方法
1 . 已知甲、乙、丙为常见单质,且丙是无色气体;A—G均为常见的化合物;B为淡黄色固体,B的式量比A的式量大16,E是形成酸雨的主要物质,在一定条件下,各物质相互转化关系如下图所示(产物中水已忽略):

(1)写出下列物质的化学式:G_______ ,F_______ ;
(2)写出下列变化的化学方程式
B+H2O → 丙 + C :_______ ;
(3)E是一种有毒气体,工业上常用生石灰对E气体进行处理。写出其化学反应方程式_______ 。

(1)写出下列物质的化学式:G
(2)写出下列变化的化学方程式
B+H2O → 丙 + C :
(3)E是一种有毒气体,工业上常用生石灰对E气体进行处理。写出其化学反应方程式
您最近一年使用:0次
2 . 硫酸是一种重要的化学试剂。某实验小组的同学利用浓硫酸进行如下实验。请按要求回答下列问题。
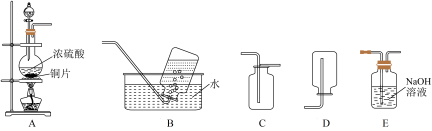
(1)装置A中发生反应的化学方程式为_______ 。上述装置中适于收集二氧化硫气体的是(填字母)_______ 。
(2)将一收集满二氧化硫气体的小试管倒置于滴有紫色石蕊溶液的水中,可观察到的现象是_______ 。
(3)上述实验所产生的二氧化硫尾气可选用E装置来吸收,该反应的化学方程式为_______ 。

(1)装置A中发生反应的化学方程式为
(2)将一收集满二氧化硫气体的小试管倒置于滴有紫色石蕊溶液的水中,可观察到的现象是
(3)上述实验所产生的二氧化硫尾气可选用E装置来吸收,该反应的化学方程式为
您最近一年使用:0次
3 . 下表列出了①~⑨九种元素在周期表中的位置。
请按要求回答下列问题:
(1)元素⑧的原子结构示意图:___________ ,元素⑥与⑨组成的化合物的电子式:___________ 。
(2)元素⑥~⑨中原子半径最小的是___________ (填元素符号)。
(3)元素①~⑨中化学性质最不活泼的是___________ (填元素符号)。
(4)元素③和④的气态氢化物中,稳定性较强的是___________ (填化学式)。
(5)元素⑥和⑦的最高价氧化物对应的水化物分别为X和Y,其中碱性较强的是___________ (填化学式),X和Y反应的离子方程式:___________ 。
(6)元素①与②所形成的最简单有机物的空间结构是___________ 。元素①与②所形成的最简单烯烃为Z,写出Z与水在催化剂、加热、加压条件下反应的化学方程式:___________ ,该反应生成物的官能团是___________ (填名称),反应类型为___________ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)元素⑧的原子结构示意图:
(2)元素⑥~⑨中原子半径最小的是
(3)元素①~⑨中化学性质最不活泼的是
(4)元素③和④的气态氢化物中,稳定性较强的是
(5)元素⑥和⑦的最高价氧化物对应的水化物分别为X和Y,其中碱性较强的是
(6)元素①与②所形成的最简单有机物的空间结构是
您最近一年使用:0次
4 . 常温下,A是双原子分子形成的气态单质。A在标准状况下的密度为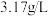 ,B、C、D都是含A中元素的化合物,它们之间的转化关系如图所示(图中有些反应的产物和反应条件没有标出)。
,B、C、D都是含A中元素的化合物,它们之间的转化关系如图所示(图中有些反应的产物和反应条件没有标出)。
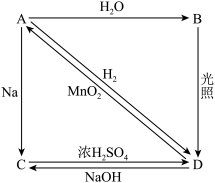
请回答下列问题:
(1)写出下列B的化学式:_______ ;
(2)氢气在A中点燃的现象为_______ ,A通入紫色石蕊溶液中的现象为_______ ;
(3)检验C中的阴离子需要加入的试剂是_______ (填化学式);
(4)常温下,A与 溶液反应的离子方程式为
溶液反应的离子方程式为_______ ;
(5)写出D→A的化学反应方程式为_______ ,此反应中,氧化剂与还原剂的物质的量之比为_______ 。
 ,B、C、D都是含A中元素的化合物,它们之间的转化关系如图所示(图中有些反应的产物和反应条件没有标出)。
,B、C、D都是含A中元素的化合物,它们之间的转化关系如图所示(图中有些反应的产物和反应条件没有标出)。
请回答下列问题:
(1)写出下列B的化学式:
(2)氢气在A中点燃的现象为
(3)检验C中的阴离子需要加入的试剂是
(4)常温下,A与
 溶液反应的离子方程式为
溶液反应的离子方程式为(5)写出D→A的化学反应方程式为
您最近一年使用:0次
解题方法
5 . 某同学用下图装置制备乙酸乙酯,a试管中是乙醇、浓硫酸、乙酸的混合液,b试管盛饱和 溶液。请回答下列问题:
溶液。请回答下列问题:
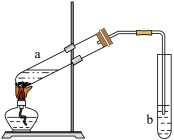
(1)指出装置中的错误是_______ ;
(2)b试管中饱和 溶液的作用:①降低乙酸乙酯的溶解度,使其分层析出,②
溶液的作用:①降低乙酸乙酯的溶解度,使其分层析出,②_____ ;
(3)此反应的现象是看到液面上有_______ ,并可以闻到香味;
(4)从b试管中分离出乙酸乙酯的实验操作是_______ (填操作名称);
(5)写出a试管中发生反应的化学方程式为,在该实验中,若用 乙醇和
乙醇和 乙酸在浓硫酸作用下加热,充分反应,能否生成
乙酸在浓硫酸作用下加热,充分反应,能否生成 乙酸乙酯
乙酸乙酯_______ (填“能”或“不能”)
 溶液。请回答下列问题:
溶液。请回答下列问题:
(1)指出装置中的错误是
(2)b试管中饱和
 溶液的作用:①降低乙酸乙酯的溶解度,使其分层析出,②
溶液的作用:①降低乙酸乙酯的溶解度,使其分层析出,②(3)此反应的现象是看到液面上有
(4)从b试管中分离出乙酸乙酯的实验操作是
(5)写出a试管中发生反应的化学方程式为,在该实验中,若用
 乙醇和
乙醇和 乙酸在浓硫酸作用下加热,充分反应,能否生成
乙酸在浓硫酸作用下加热,充分反应,能否生成 乙酸乙酯
乙酸乙酯
您最近一年使用:0次
6 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出①~⑨九种元素在周期表中的位置。请回答下列问题:
(1)⑨的原子结构示意图是_______ ;
(2)编号元素中,非金属性最强的是_______ (填元素名称);
(3)①②③三种元素的最高价氧化物对应的水化物中,碱性最强的是_______ (填化学式);
(4)写出⑦形成氢化物的电子式:_______ ,⑦、⑧两种元素分别形成的氢化物,稳定性较强的是_______ (填化学式);
(5)②③⑦三种元素原子半径由小到大的顺序是_______ (填元素符号);
(6)编号元素中,最高价氧化物对应的水化物呈两性的氢氧化物与氢氧化钠溶液反应的化学方程式为_______ ;
(7)④形成的常见气态氢化物与⑤形成的双原子分子单质,它们在催化剂和加热的条件下发生化学反应的化学方程式为_______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ④ | ⑤ | ⑥ | ⑨ | ||||
| 三 | ① | ② | ③ | ⑦ | ⑧ |
(2)编号元素中,非金属性最强的是
(3)①②③三种元素的最高价氧化物对应的水化物中,碱性最强的是
(4)写出⑦形成氢化物的电子式:
(5)②③⑦三种元素原子半径由小到大的顺序是
(6)编号元素中,最高价氧化物对应的水化物呈两性的氢氧化物与氢氧化钠溶液反应的化学方程式为
(7)④形成的常见气态氢化物与⑤形成的双原子分子单质,它们在催化剂和加热的条件下发生化学反应的化学方程式为
您最近一年使用:0次
7 . 下图是部分短周期元素的单质及其化合物的转化关系。已知A、B、C、D、E都是单质,常温常压下,A是固体,其余是气体,且C呈黄绿色。化合物H和I两种气体相遇时产生白烟,化合物G的焰色反应为黄色。反应①和②均在水溶液中进行。
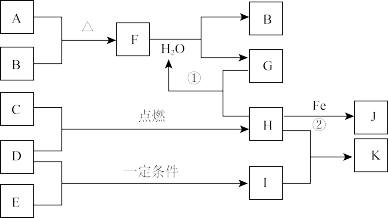
请回答下列问题:
(1)写出下列物质的化学式:A_______ 、K_______ ;
(2)F可水反应的化学方程式为_______ ,该反应中水的作用是_______ ;
a.氧化剂 b.还原剂
c.既是氧化剂又是还原剂 d.既不是氧化剂又不是还原剂
(3)向盛有J溶液的试管中滴加G溶液,可以观察到的现象为_______ ;
(4)C通入盛有G溶液的试管中可以得到漂白液,该反应的离子方程式为_______ ,
(5)D和E的反应在化工生产中可以用于氮的固定,对应的化学方程式为_______ 。

请回答下列问题:
(1)写出下列物质的化学式:A
(2)F可水反应的化学方程式为
a.氧化剂 b.还原剂
c.既是氧化剂又是还原剂 d.既不是氧化剂又不是还原剂
(3)向盛有J溶液的试管中滴加G溶液,可以观察到的现象为
(4)C通入盛有G溶液的试管中可以得到漂白液,该反应的离子方程式为
(5)D和E的反应在化工生产中可以用于氮的固定,对应的化学方程式为
您最近一年使用:0次
解题方法
8 . 下图是实验室制取 并验证
并验证 某些性质的装置图。已知
某些性质的装置图。已知 固体与硫酸可发生反应:
固体与硫酸可发生反应: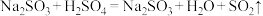 。试回答:
。试回答:
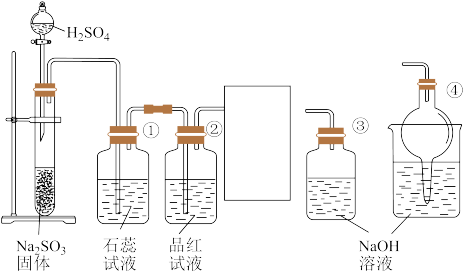
(1)盛放 溶液的仪器名称是
溶液的仪器名称是_______ ;
(2)①中石蕊试液产生的现象为_______ ,原因是_______ (用化学方程式表示);
(3)②中品红试液产生的现象为_______ ,证明 具有
具有_______ 性;
(4)为防止环境污染,上图方框内可用于吸收多余 的装置是
的装置是_______ (填③或④),其中发生反应的离子方程式为_______ ;
(5)实验室中 气体的收集方法应选择
气体的收集方法应选择_______ 。
a.向上排空气法 b.向下排空㺬法
c.排水法 d.排饱和 溶液法
溶液法
 并验证
并验证 某些性质的装置图。已知
某些性质的装置图。已知 固体与硫酸可发生反应:
固体与硫酸可发生反应: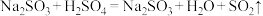 。试回答:
。试回答:
(1)盛放
 溶液的仪器名称是
溶液的仪器名称是(2)①中石蕊试液产生的现象为
(3)②中品红试液产生的现象为
 具有
具有(4)为防止环境污染,上图方框内可用于吸收多余
 的装置是
的装置是(5)实验室中
 气体的收集方法应选择
气体的收集方法应选择a.向上排空气法 b.向下排空㺬法
c.排水法 d.排饱和
 溶液法
溶液法
您最近一年使用:0次
名校
解题方法
9 . 实验小组利用传感器探究Na2CO3和NaHCO3的性质。
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱
【实验过程】
【分析与解释】
(1)实验I中,溶解时吸收热量的物质是_______ 。
(2)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为_______ ,OH-未参与该反应的实验证据是_______ 。
(3)实验II中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,造成这种差异是由于滴加NaHCO3溶液的烧杯中有_______ (填写离子符号)参与反应。
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱
【实验过程】
| 编号 | 实验操作 | 实验数据 |
| 实验I | 测量下述实验过程的温度变化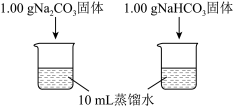 | 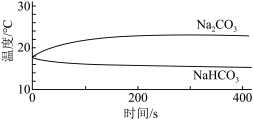 |
| 实验II | 测量下述实验过程的pH变化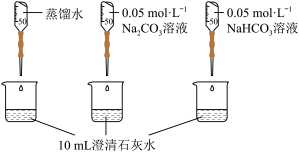 |  |
(1)实验I中,溶解时吸收热量的物质是
(2)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为
(3)实验II中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,造成这种差异是由于滴加NaHCO3溶液的烧杯中有
您最近一年使用:0次
2022-11-30更新
|
428次组卷
|
13卷引用:北京市2020年普通高中学业水平合格性模拟考试化学试题
北京市2020年普通高中学业水平合格性模拟考试化学试题2020年北京市第一次普通高中学业水平合格性考试化学试题高一必修第一册(苏教2019)专题3 第二单元 金属钠及钠的化合物4北京市回民学校2020-2021学年高一上学期期中考试化学试题北京市第三十一中学2020—2021学年度高一下学期期中考试化学试题北京第七中学2020-2021学年高一下学期期中考试化学试题天津市红桥区2020-2021学年高一下学期期末考试化学试题(已下线)北京市第四中学2022-2023学年高一上学期期中考试化学试题北京市第四十三中学2022-2023学年高一上学期期中考试化学试题北京市第八中学2022-2023学年高一下学期期末考试化学试题(已下线)专题八 钠及其化合物北京市第十一中学2023-2024学年高一上学期期中考试化学试题北京市月坛中学2023-2024学年高一上学期期中考试化学试题
解题方法
10 . NaHCO3干法脱硫具有无腐蚀、无废水等特点,常用于除去工业烟气中少量的SO2。为探究不同温度下烟气的脱硫效果,设计如图装置(省略夹持装置)进行模拟实验。回答下列问题。

(1)实验开始前,先检查装置的____ 。II中添加的SiO2使NaHCO3分散,从而____ (填“增大”或“减小”)反应物接触面,提高脱硫效果。
(2)通入由SO2、N2组成的模拟烟气,待气流稳定后,点燃II处酒精灯,缓慢升温。当II中脱硫温度低于270℃时,反应为2NaHCO3+SO2=Na2SO3+2CO2+H2O;高于270℃时,NaHCO3完全分解为Na2CO3。由于Na2CO3的碱性比NaHCO3的____ (填“强”或“弱”),因而其脱硫效果更好,Na2CO3脱硫反应的方程式为____ 。
(3)装置IV的作用是吸收体系中的残余SO2,可选用的试剂有____ 。
(4)保持II中反应温度为300℃不变,待气流完全稳定时,从SO2检测器读数并进行换算,得出I和III中SO2的浓度依次为C1、C2,用C1、C2表示的脱硫率计算式为____ 。
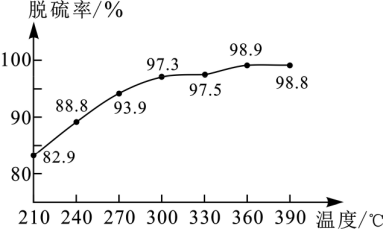
(5)持续测定并处理数据,得出不同温度下的脱硫率(如图)。根据图中实验数据判断,该方法最适宜的脱硫温度范围是____ ,选择该温度范围的理由有____ 。

(1)实验开始前,先检查装置的
(2)通入由SO2、N2组成的模拟烟气,待气流稳定后,点燃II处酒精灯,缓慢升温。当II中脱硫温度低于270℃时,反应为2NaHCO3+SO2=Na2SO3+2CO2+H2O;高于270℃时,NaHCO3完全分解为Na2CO3。由于Na2CO3的碱性比NaHCO3的
(3)装置IV的作用是吸收体系中的残余SO2,可选用的试剂有
| A.NaOH溶液 | B.酸性KMnO4溶液 | C.浓硫酸 | D.盐酸 |
(5)持续测定并处理数据,得出不同温度下的脱硫率(如图)。根据图中实验数据判断,该方法最适宜的脱硫温度范围是

您最近一年使用:0次
2022-08-15更新
|
98次组卷
|
2卷引用:广西壮族自治区普通高中2020—2021学年高三上学期12月学业水平考试化学试题



