为解决二氧化碳的过量排放带来的气候变暖、海洋酸化的负面效应,二氧化碳的捕集及转化成为高价值的低碳烯烃已成为热门的科研项目。回答下列问题:
I.高温条件下二氧化碳可以氢化制备乙烯。
(1)已知下列反应的热化学方程式:
i. ;
;
ii.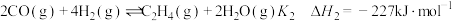 ;
;
反应iii: 的
的
_______  ,平衡常数
,平衡常数
_______ (用 、
、 表示)。
表示)。
(2)研究表明,合成气体在 、起始
、起始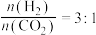 时,
时, 平衡转化率随温度的变化如图1所示,乙烯选择性随温度的变化如图2所示[乙烯选择性
平衡转化率随温度的变化如图1所示,乙烯选择性随温度的变化如图2所示[乙烯选择性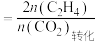 ]:
]: 平衡转化率随温度升高出现先下降后升高可能的原因是
平衡转化率随温度升高出现先下降后升高可能的原因是_______ 。
②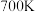 时,反应i的
时,反应i的
_______ (列出计算式即可)。
(3)关于上述反应,下列说法正确的是_______(填选项字母)。
II.二氧化碳电催化还原制乙烯。
(4)科学家研究利用电催化还原 制乙烯,其工作原理如图所示,涂有
制乙烯,其工作原理如图所示,涂有 催化剂的铜电极作阴极,阴极的电极反应式为
催化剂的铜电极作阴极,阴极的电极反应式为_______ ;当阴极生成 气体时,理论上阳极生成气体的物质的量为
气体时,理论上阳极生成气体的物质的量为_______ 。
I.高温条件下二氧化碳可以氢化制备乙烯。
(1)已知下列反应的热化学方程式:
i.
 ;
;ii.
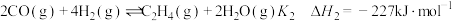 ;
;反应iii:
 的
的
 ,平衡常数
,平衡常数
 、
、 表示)。
表示)。(2)研究表明,合成气体在
 、起始
、起始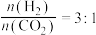 时,
时, 平衡转化率随温度的变化如图1所示,乙烯选择性随温度的变化如图2所示[乙烯选择性
平衡转化率随温度的变化如图1所示,乙烯选择性随温度的变化如图2所示[乙烯选择性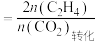 ]:
]: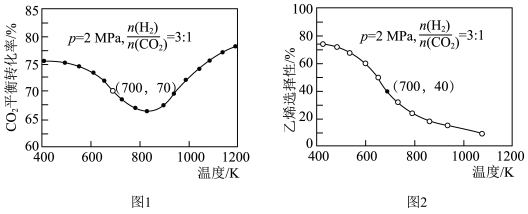
 平衡转化率随温度升高出现先下降后升高可能的原因是
平衡转化率随温度升高出现先下降后升高可能的原因是②
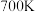 时,反应i的
时,反应i的
(3)关于上述反应,下列说法正确的是_______(填选项字母)。
A.提高投料比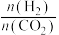 , , 的平衡转化率减小 的平衡转化率减小 |
| B.使用高效催化剂可提高平衡时乙烯的体积分数 |
| C.若在恒容、绝热容器中进行,温度不变则反应达到平衡 |
D.体系内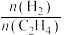 比值不变反应达到平衡状态 比值不变反应达到平衡状态 |
II.二氧化碳电催化还原制乙烯。
(4)科学家研究利用电催化还原
 制乙烯,其工作原理如图所示,涂有
制乙烯,其工作原理如图所示,涂有 催化剂的铜电极作阴极,阴极的电极反应式为
催化剂的铜电极作阴极,阴极的电极反应式为 气体时,理论上阳极生成气体的物质的量为
气体时,理论上阳极生成气体的物质的量为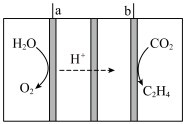
更新时间:2024-05-27 16:10:45
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】以下是关于“外界因素对化学平衡移动影响的实验研究”的课题,回答问题:
(1)影响化学平衡因素的界定:化学平衡发生移动的本质原因是________ ,所以影响化学平衡的因素可以从分析影响的因素入手.
a. v(正)≠v(逆) .v(正)和v(逆)都增大
.v(正)和v(逆)都增大 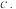 v(正)和v(逆)都减小
v(正)和v(逆)都减小
(2)研究的思路与方法
①研究对象的选择,现有以下可逆反应:
 .
.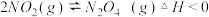
 .
.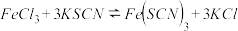
其中, 适合于研究
适合于研究_______ 对平衡的影响, 适合于研究
适合于研究_______ 对平衡的影响.
 .浓度
.浓度  .温度
.温度  .压强
.压强  .催化剂
.催化剂
②研究方法:采用控制其他因素不变,改变其中一个因素的方法,并进行对比实验.
(3)单一因素对化学平衡移动影响的实验研究:
 .浓度:将
.浓度:将 与
与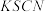 反应后所得的混合液分为
反应后所得的混合液分为 等份,分别加入浓
等份,分别加入浓 溶液、浓
溶液、浓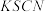 溶液和
溶液和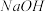 固体,观察现象.现象:加入浓
固体,观察现象.现象:加入浓 溶液后的混合溶液红色
溶液后的混合溶液红色________ ,加入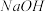 固体后,混合溶液红棕色
固体后,混合溶液红棕色________ .
 .温度:将密封并相互连通的盛有
.温度:将密封并相互连通的盛有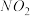 的两个玻璃球,一个放入热水中,另一个放入冷水中.
的两个玻璃球,一个放入热水中,另一个放入冷水中.
现象:放入热水中的球内红棕色________ ;放入冷水中的球内红棕色________ .
(4)综合(3)能得出的影响化学平衡移动的原因是________ .
(1)影响化学平衡因素的界定:化学平衡发生移动的本质原因是
a. v(正)≠v(逆)
 .v(正)和v(逆)都增大
.v(正)和v(逆)都增大 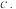 v(正)和v(逆)都减小
v(正)和v(逆)都减小(2)研究的思路与方法
①研究对象的选择,现有以下可逆反应:
 .
.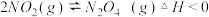
 .
.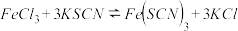
其中,
 适合于研究
适合于研究 适合于研究
适合于研究 .浓度
.浓度  .温度
.温度  .压强
.压强  .催化剂
.催化剂②研究方法:采用控制其他因素不变,改变其中一个因素的方法,并进行对比实验.
(3)单一因素对化学平衡移动影响的实验研究:
 .浓度:将
.浓度:将 与
与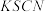 反应后所得的混合液分为
反应后所得的混合液分为 等份,分别加入浓
等份,分别加入浓 溶液、浓
溶液、浓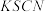 溶液和
溶液和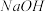 固体,观察现象.现象:加入浓
固体,观察现象.现象:加入浓 溶液后的混合溶液红色
溶液后的混合溶液红色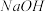 固体后,混合溶液红棕色
固体后,混合溶液红棕色 .温度:将密封并相互连通的盛有
.温度:将密封并相互连通的盛有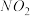 的两个玻璃球,一个放入热水中,另一个放入冷水中.
的两个玻璃球,一个放入热水中,另一个放入冷水中.现象:放入热水中的球内红棕色
(4)综合(3)能得出的影响化学平衡移动的原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】I.一定条件下,反应室(容积恒定为2L)中有反应:A(g)+2B(g) C(g)。
C(g)。
(1)能说明上述反应达到平衡状态的是________ (填字母,下同)。
A.反应中A与B的物质的量浓度之比为1∶2 B.混合气体总物质的量不再变化
C.混合气体的密度不随时间的变化而变化 D.2v正(A)=v逆(B)
(2)1molA(g)与2molB(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:

①p1________ p2(填“<”、“>”或“=”,下同),正反应的ΔH________ 0。
②下列措施中一定能使 增大的是
增大的是________ 。
A.升高温度B.恒温恒容再充入A
C.恒温恒容再充入BD.恒温恒容再充入1molC
(3)100℃时将1molA和2molB通入反应室,保持温度不变,10min末C(g)的浓度为0.05mol·L-1,则10min末B的转化率为_____ ,此时v正_____ v逆(填“<”、“>”或“=”)。
II.一定温度下,在容积为VL的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
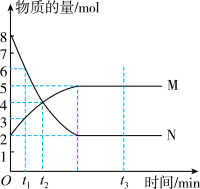
(1)此反应的化学方程式中 =
=____________ 。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为____________ 。
(3)下列叙述能说明上述反应达到平衡状态的是____________ (填字母)。
A.反应中M与N的物质的量之比为1∶1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗amolN,同时生成bmolM
E.混合气体的压强不随时间的变化而变化
F.混合气体的平均相对分子质量不随时间的变化而变化
 C(g)。
C(g)。(1)能说明上述反应达到平衡状态的是
A.反应中A与B的物质的量浓度之比为1∶2 B.混合气体总物质的量不再变化
C.混合气体的密度不随时间的变化而变化 D.2v正(A)=v逆(B)
(2)1molA(g)与2molB(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:

①p1
②下列措施中一定能使
 增大的是
增大的是A.升高温度B.恒温恒容再充入A
C.恒温恒容再充入BD.恒温恒容再充入1molC
(3)100℃时将1molA和2molB通入反应室,保持温度不变,10min末C(g)的浓度为0.05mol·L-1,则10min末B的转化率为
II.一定温度下,在容积为VL的密闭容器中进行反应:aN(g)
 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中
 =
=(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为
(3)下列叙述能说明上述反应达到平衡状态的是
A.反应中M与N的物质的量之比为1∶1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗amolN,同时生成bmolM
E.混合气体的压强不随时间的变化而变化
F.混合气体的平均相对分子质量不随时间的变化而变化
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】CO2、CS2、COS是由C、O、S三种元素形成的结构相似的化合物。
(1)下列能说明碳、硫两种元素非金属性相对强弱的是_____________ (填序号)
A.亚硫酸溶液加入Na2CO3溶液中,产生气泡
B.氧化性:浓H2SO4>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
D.SO2有较强还原性,而CO2无还原性
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害。
① 羰基硫的结构式为:________________ 。沸点:CO2_________ COS(填“大于”或“小于”),说明原因_____________________ 。
②下列有关羰基硫的推测肯定不正确的是_________________
A.COS分子中,所有原子都满足8电子的稳定结构
B.COS分子是含有极性键的非极性分子
C.COS分子中三个原子处于同一直线上
D.COS可能在O2中燃烧
③羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下图:

已知A是一种盐,则A的化学式为________ ;气体单质a为____________________ .
(3)在恒容密闭容器中,CO和H2S混合加热生成羰基硫的反应为CO(g)+H2S(g) COS(g)+H2(g),反应前CO和H2S的物质的量均为10mol,平衡后CO的物质的量为8mol,回答下列问题:
COS(g)+H2(g),反应前CO和H2S的物质的量均为10mol,平衡后CO的物质的量为8mol,回答下列问题:
①升高温度,H2S浓度增加,表明该反应是__________________ 反应(填“放热”或“吸热”)。
②平衡时,继续通入CO10mol和H2S10mol,一段时间后再次达到平衡,此时H2S的转化率_____ (填“增大”“减小”或“不变”)
(4)若反应在恒容密闭容器中进行,能说明该反应已达到平衡状态的是____________
A.容器内气体密度保持不变
B.CO、H2S、COS、H2的浓度均不再变化
C.c(H2)=c(H2S)
D.v(H2)正=v(H2S)逆
(1)下列能说明碳、硫两种元素非金属性相对强弱的是
A.亚硫酸溶液加入Na2CO3溶液中,产生气泡
B.氧化性:浓H2SO4>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
D.SO2有较强还原性,而CO2无还原性
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害。
① 羰基硫的结构式为:
②下列有关羰基硫的推测肯定不正确的是
A.COS分子中,所有原子都满足8电子的稳定结构
B.COS分子是含有极性键的非极性分子
C.COS分子中三个原子处于同一直线上
D.COS可能在O2中燃烧
③羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下图:

已知A是一种盐,则A的化学式为
(3)在恒容密闭容器中,CO和H2S混合加热生成羰基硫的反应为CO(g)+H2S(g)
 COS(g)+H2(g),反应前CO和H2S的物质的量均为10mol,平衡后CO的物质的量为8mol,回答下列问题:
COS(g)+H2(g),反应前CO和H2S的物质的量均为10mol,平衡后CO的物质的量为8mol,回答下列问题:①升高温度,H2S浓度增加,表明该反应是
②平衡时,继续通入CO10mol和H2S10mol,一段时间后再次达到平衡,此时H2S的转化率
(4)若反应在恒容密闭容器中进行,能说明该反应已达到平衡状态的是
A.容器内气体密度保持不变
B.CO、H2S、COS、H2的浓度均不再变化
C.c(H2)=c(H2S)
D.v(H2)正=v(H2S)逆
您最近一年使用:0次
【推荐1】已知A(g)+B(g)⇌C(g)+D(g)反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的平衡常数表达式K=______ ,△H ______ 0(填“<”“>”“=”);
(2)900℃时,向一个固定容器为2L的密闭容器中充入0.20mol的A和0.80mol的B,若反应初始到2s内A浓度变化0.05mol•L-1.则A的平均反应速率v(A)=______ .该反应达到平衡时A的转化率为 ______ ,如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率为 ______ (填”变大“、”变小“或”不变“)
(3)判断反应是否达到平衡的依据为______ (填字母代号).
a 压强不随时间改变 b 气体的密度不随时间改变
c c(A)不随时间改变 d 单位时间里生成C和D的物质的量相等
(4)1200℃时,若向另一相同容器中充入0.30molA、0.40mol B、0.40mol C和0.50molD,此时v正______ v逆(填”大于“、”小于“或”等于“).
| 温度/℃ | 700 | 800 | 900 | 1000 | 1200 |
| 平衡常数 | 0.5 | 0.6 | 1.0 | 1.6 | 2.0 |
(1)该反应的平衡常数表达式K=
(2)900℃时,向一个固定容器为2L的密闭容器中充入0.20mol的A和0.80mol的B,若反应初始到2s内A浓度变化0.05mol•L-1.则A的平均反应速率v(A)=
(3)判断反应是否达到平衡的依据为
a 压强不随时间改变 b 气体的密度不随时间改变
c c(A)不随时间改变 d 单位时间里生成C和D的物质的量相等
(4)1200℃时,若向另一相同容器中充入0.30molA、0.40mol B、0.40mol C和0.50molD,此时v正
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】已知:Fe(s)+CO2(g) FeO(s)+CO(g) K1 ①
FeO(s)+CO(g) K1 ①
Fe(s)+H2O(g) FeO(s)+H2(g) K2 ②
FeO(s)+H2(g) K2 ②
H2(g)+CO2(g) H2O(g)+CO(g) K3 ③
H2O(g)+CO(g) K3 ③
又知不同温度下,K1、K2值如下:
(1)若500℃时进行反应①,CO2起始浓度为2 mol·L−1,2 min后建立平衡,则CO2转化率为_________ ,用CO表示的化学反应速率为____________ 。
(2)900℃时进行反应③,其平衡常数K3为___________ (填具体数值),焓变ΔH_____ 0(填“>”“=”或“<”),若已知该反应仅在高温时正反应自发进行,则ΔS_____ 0(填“>”“=”或“<”)。
(3)下列图象符合反应②的是____________ (填序号)。(图中v是速率,φ为混合物中H2的体积百分含量。)

 FeO(s)+CO(g) K1 ①
FeO(s)+CO(g) K1 ①Fe(s)+H2O(g)
 FeO(s)+H2(g) K2 ②
FeO(s)+H2(g) K2 ②H2(g)+CO2(g)
 H2O(g)+CO(g) K3 ③
H2O(g)+CO(g) K3 ③又知不同温度下,K1、K2值如下:
| 温度/℃ | K1 | K2 |
| 500 | 1.00 | 3.15 |
| 700 | 1.47 | 2.26 |
| 900 | 2.40 | 1.60 |
(2)900℃时进行反应③,其平衡常数K3为
(3)下列图象符合反应②的是

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】随着科学技术的发展和环保要求的不断提高, 的捕集利用技术成为研究的重点.完成下列填空:
的捕集利用技术成为研究的重点.完成下列填空:
(1)目前国际空间站处理 的一个重要方法是将
的一个重要方法是将 还原,所涉及的反应方程式为:
还原,所涉及的反应方程式为: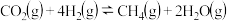
已知 的体积分数随温度的升高而增加.若温度从
的体积分数随温度的升高而增加.若温度从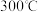 升至
升至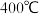 ,重新达到平衡,判断下列表格中各物理量的变化
,重新达到平衡,判断下列表格中各物理量的变化 选填“增大”、“减小”或“不变”
选填“增大”、“减小”或“不变”
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
a、b、c、d与m、n、x、y之间的关系式为________________________ .
(3)已知碳酸: ,
,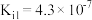 ,
,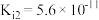 ;草酸:
;草酸: ,
,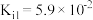 ,
,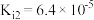 。
。
则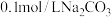 溶液的pH
溶液的pH ____________ 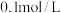
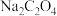 溶液的
溶液的 选填“大于”“小于”或“等于”
选填“大于”“小于”或“等于” 等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是 _______________  若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是 ___________  选填编号
选填编号
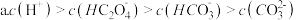
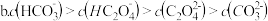
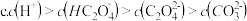
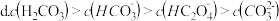
(4)人体血液中的碳酸和碳酸氢盐存在平衡: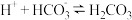 ,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象
,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象 ___________________________________________________ .
 的捕集利用技术成为研究的重点.完成下列填空:
的捕集利用技术成为研究的重点.完成下列填空:(1)目前国际空间站处理
 的一个重要方法是将
的一个重要方法是将 还原,所涉及的反应方程式为:
还原,所涉及的反应方程式为: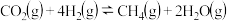
已知
 的体积分数随温度的升高而增加.若温度从
的体积分数随温度的升高而增加.若温度从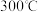 升至
升至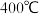 ,重新达到平衡,判断下列表格中各物理量的变化
,重新达到平衡,判断下列表格中各物理量的变化 选填“增大”、“减小”或“不变”
选填“增大”、“减小”或“不变”
 | 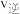 | 平衡常数K | 转化率 |
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
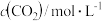 | 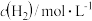 | 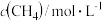 | 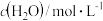 | |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为
(3)已知碳酸:
 ,
,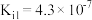 ,
,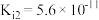 ;草酸:
;草酸: ,
,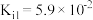 ,
,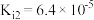 。
。则
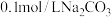 溶液的pH
溶液的pH 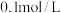
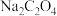 溶液的
溶液的 选填“大于”“小于”或“等于”
选填“大于”“小于”或“等于” 等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是  若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是  选填编号
选填编号
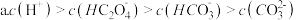
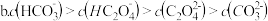
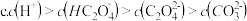
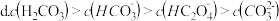
(4)人体血液中的碳酸和碳酸氢盐存在平衡:
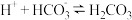 ,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象
,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】铁及其化合物在处理工业废水、废气过程中发挥着重要作用。
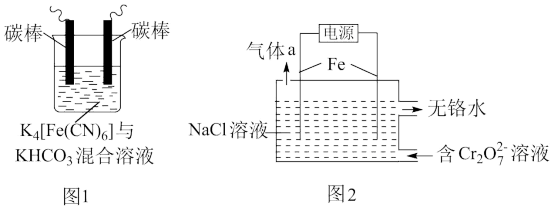
(1)用铁的化合物除硫化氢:2[Fe(CN)6]3-+ 2 +HS- =2[Fe(CN)6]4-+ 2
+HS- =2[Fe(CN)6]4-+ 2 +S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为
+S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为_______ ;电解过程中阴极区溶液的pH_______ (填“变大”、 “变小”或“不变")。
(2)以铁为电极电解除铬,如图2
已知: + H2O=2
+ H2O=2 +2H+
+2H+
氧化性: >
>
①电解过程中主要反应之一: +6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是
+6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是_______ 。
②电解过程中,不同pH时,通电时间与Cr元素的去除率关系如图3所示,pH=10相比pH=4,Cr元素的去除率偏低的原因可能是_______ 。
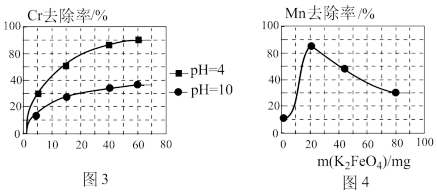
(3)高铁酸钾(K2FeO4)除锰
已知:K2FeO4具有强氧化性,极易溶于水
①在酸性条件下,能与废水中的Mn2+反应生成Fe(OH)3和MnO2沉淀来除锰,该反应的离子方程式_______ 。
②用K2FeO4处理1L 50 mg/L的含Mn2+废水,Mn元素的去除率与K2FeO4量的关系如图4所示,当K2FeO4超过20 mg时,Mn元素的去除率下降的原因可能是_______ 。

(1)用铁的化合物除硫化氢:2[Fe(CN)6]3-+ 2
 +HS- =2[Fe(CN)6]4-+ 2
+HS- =2[Fe(CN)6]4-+ 2 +S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为
+S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为(2)以铁为电极电解除铬,如图2
已知:
 + H2O=2
+ H2O=2 +2H+
+2H+氧化性:
 >
>
①电解过程中主要反应之一:
 +6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是
+6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是②电解过程中,不同pH时,通电时间与Cr元素的去除率关系如图3所示,pH=10相比pH=4,Cr元素的去除率偏低的原因可能是

(3)高铁酸钾(K2FeO4)除锰
已知:K2FeO4具有强氧化性,极易溶于水
①在酸性条件下,能与废水中的Mn2+反应生成Fe(OH)3和MnO2沉淀来除锰,该反应的离子方程式
②用K2FeO4处理1L 50 mg/L的含Mn2+废水,Mn元素的去除率与K2FeO4量的关系如图4所示,当K2FeO4超过20 mg时,Mn元素的去除率下降的原因可能是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】回答下列问题
(1)二氧化氯具有杀菌、漂白、除臭、消毒、保鲜的功能。电解法制取 的新工艺如图所示。
的新工艺如图所示。
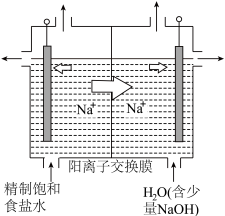
①用石墨作电极,在一定条件下电解饱和食盐水制取 (如图所示),阳极产生
(如图所示),阳极产生 的电极反应式为
的电极反应式为________ 。
②电解一段时间,当阴极产生的气体体积为 (标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为
(标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为________  。
。
(2)粗银精炼装置如图所示,电解液为稀硫酸。
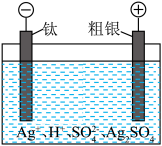
①阳极的电极反应式为________ 。
②下列说法正确的是________ (填字母)。
a.一段时间后,阳极质量减小
b.阴极区可获得银单质的原理:
c.体系中存在沉淀溶解平衡: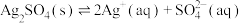
(3)一种用于心脏起搏器的微型电池具有容量大、寿命长和电压稳定等特点。该电池的电极材料是石墨和锂,电解质溶液为等物质的量的 、
、 溶解在
溶解在 中形成的溶液。这种电池的总反应为
中形成的溶液。这种电池的总反应为 。
。
①锂电极的电势比石墨电极的________ (填“低”或“高”)。
②放电时,石墨电极发生________ (填“氧化”或“还原”)反应。
③电池的正极反应为________ 。
(1)二氧化氯具有杀菌、漂白、除臭、消毒、保鲜的功能。电解法制取
 的新工艺如图所示。
的新工艺如图所示。
①用石墨作电极,在一定条件下电解饱和食盐水制取
 (如图所示),阳极产生
(如图所示),阳极产生 的电极反应式为
的电极反应式为②电解一段时间,当阴极产生的气体体积为
 (标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为
(标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为 。
。(2)粗银精炼装置如图所示,电解液为稀硫酸。

①阳极的电极反应式为
②下列说法正确的是
a.一段时间后,阳极质量减小
b.阴极区可获得银单质的原理:

c.体系中存在沉淀溶解平衡:
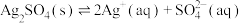
(3)一种用于心脏起搏器的微型电池具有容量大、寿命长和电压稳定等特点。该电池的电极材料是石墨和锂,电解质溶液为等物质的量的
 、
、 溶解在
溶解在 中形成的溶液。这种电池的总反应为
中形成的溶液。这种电池的总反应为 。
。①锂电极的电势比石墨电极的
②放电时,石墨电极发生
③电池的正极反应为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】如图,E为沾有Na2SO4溶液的滤纸,并加入几滴酚酞。A,B分别为Pt片,压在滤纸两端,R、S为电池的电极。M、N是用多微孔的Ni制成的电极材料,它在碱性溶液中可以视为惰性电极。G为电流计,K为开关。C、D和电解池中都充满浓KOH溶液。若在滤纸中央点上一滴紫色的KMnO4溶液,打开K,接通电源一段时间后,C、D中有气体产生。

(1)R为________ (填“正”或“负”)极。
(2)A极附近溶液的现象是____________ ,B极附近发生的电极反应式为_______________ 。
(3)滤纸上的紫色点向________ (填“A”或“B”)方移动。
(4)当C、D里的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,C中的电极为____ 极,电极反应式为_______________ 。
(5)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。右图是通过人工光合作用制备HCOOH的原理示意图,催化剂a附近酸性,催化剂b表面的反应是______________ 。

(1)R为
(2)A极附近溶液的现象是
(3)滤纸上的紫色点向
(4)当C、D里的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,C中的电极为
(5)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。右图是通过人工光合作用制备HCOOH的原理示意图,催化剂a附近酸性,催化剂b表面的反应是
您最近一年使用:0次




