如图是氮元素的各种价态与物质类别的对应关系:_____ 。从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的化合物有_______ 。
(2)实验室将浓氨水加入生石灰中可以快速制取NH3的化学方程式为_________ 。
(3)浓硝酸、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应使用___________ 。
(4)汽车尾气中含有CO和NOx等多种有害气体,若在汽车的排气管上安装一种催化转化装置,可使CO与NOx反应,生成两种无毒气体,则该反应的化学方程式为_____________ 。

(2)实验室将浓氨水加入生石灰中可以快速制取NH3的化学方程式为
(3)浓硝酸、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应使用
(4)汽车尾气中含有CO和NOx等多种有害气体,若在汽车的排气管上安装一种催化转化装置,可使CO与NOx反应,生成两种无毒气体,则该反应的化学方程式为
更新时间:2024-05-27 16:30:45
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】根据所学化学反应原理,解决以下问题:
(1)请用离子方程式表示泡沫灭火器的工作原理___ 。
(2)请用离子方程式解释漂白粉和洁厕灵不能混合使用的原因___ 。
(3)难溶物ZnS可作为沉淀剂除去废水中的Cu2+,写出该过程的离子方程式___ 。
(4)用CO(g)还原80gFe2O3(s)生成Fe(s)和CO2(g),放热12.4kJ,请写出该反应的热化学方程式___ 。
(5)已知2CO(g) CO2(g)+C(s),T=980K时,△H-T△S=0。在冶金工业中,以C为还原剂,温度高于980K时,C的氧化产物主要是
CO2(g)+C(s),T=980K时,△H-T△S=0。在冶金工业中,以C为还原剂,温度高于980K时,C的氧化产物主要是___ 。
(1)请用离子方程式表示泡沫灭火器的工作原理
(2)请用离子方程式解释漂白粉和洁厕灵不能混合使用的原因
(3)难溶物ZnS可作为沉淀剂除去废水中的Cu2+,写出该过程的离子方程式
(4)用CO(g)还原80gFe2O3(s)生成Fe(s)和CO2(g),放热12.4kJ,请写出该反应的热化学方程式
(5)已知2CO(g)
 CO2(g)+C(s),T=980K时,△H-T△S=0。在冶金工业中,以C为还原剂,温度高于980K时,C的氧化产物主要是
CO2(g)+C(s),T=980K时,△H-T△S=0。在冶金工业中,以C为还原剂,温度高于980K时,C的氧化产物主要是
您最近一年使用:0次
【推荐2】储氢纳米碳管研究成功体现了科技的进步,但用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,反应的化学方程式为:C+K2Cr2O7+H2SO4→CO2↑+K2SO4+Cr2(SO4)3+H2O(未配平)。回答下列问题。
(1)该反应中,还原剂是___________ (填化学式),被还原的元素是___________ (填元素符号)。
(2)该反应中,K2Cr2O7表现出___________ (选填“氧化性”或“还原性”),K2Cr2O7发生了___________ (选填“氧化反应”或“还原反应”)。
(3)H2SO4在该反应中表现出___________(填字母)。
(4)配平上述方程式:________ 。每生成2分子H2O,该反应转移_________ 个电子。
(1)该反应中,还原剂是
(2)该反应中,K2Cr2O7表现出
(3)H2SO4在该反应中表现出___________(填字母)。
| A.只有酸性 | B.只有氧化性 | C.酸性和氧化性 | D.酸性和还原性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氨基磺酸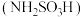 可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
(1)由尿素 与发烟硫酸(用
与发烟硫酸(用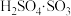 表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为
表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为_______ 。
(2)氨基磺酸在高温时的分解反应为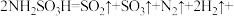
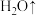 。
。
①检验该混合产物中含有 的试剂是
的试剂是_______ (填序号)。
A.品红溶液 B. 溶液 C.溴水 D.碳酸氢钠溶液
溶液 C.溴水 D.碳酸氢钠溶液
②高温时,该反应中转移2mol电子时,生成气体的总物质的量是_______ mol。
(3)硝酸与氨基磺酸能反应生成硫酸、水和一种氮氧化合物。
①0.5mol该氮氧化合物中氮元素的质量比氧元素的多6g,则该氮氧化合物的化学式为_______ 。
②下列有关浓硫酸和浓硝酸的说法正确的是_______ (填序号)。
A.浓硫酸可用于干燥 、
、 、HI
、HI
B.常温下,浓硫酸和浓硝酸均能将铝“钝化”,均体现其强氧化性
C.浓硫酸和浓硝酸分别长期露置在空气中,两者浓度变小的原理不同
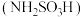 可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。(1)由尿素
 与发烟硫酸(用
与发烟硫酸(用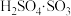 表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为
表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为(2)氨基磺酸在高温时的分解反应为
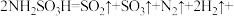
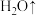 。
。①检验该混合产物中含有
 的试剂是
的试剂是A.品红溶液 B.
 溶液 C.溴水 D.碳酸氢钠溶液
溶液 C.溴水 D.碳酸氢钠溶液②高温时,该反应中转移2mol电子时,生成气体的总物质的量是
(3)硝酸与氨基磺酸能反应生成硫酸、水和一种氮氧化合物。
①0.5mol该氮氧化合物中氮元素的质量比氧元素的多6g,则该氮氧化合物的化学式为
②下列有关浓硫酸和浓硝酸的说法正确的是
A.浓硫酸可用于干燥
 、
、 、HI
、HIB.常温下,浓硫酸和浓硝酸均能将铝“钝化”,均体现其强氧化性
C.浓硫酸和浓硝酸分别长期露置在空气中,两者浓度变小的原理不同
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图是制取少量氨的实验装置:
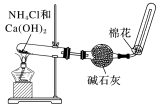
(1)在制取氨的实验装置中,使用棉花的作用是什么____ ?
(2)干燥管中的碱石灰是干燥氨的,能用无水CaCl2、P2O5代替碱石灰做干燥剂吗____ ?

(1)在制取氨的实验装置中,使用棉花的作用是什么
(2)干燥管中的碱石灰是干燥氨的,能用无水CaCl2、P2O5代替碱石灰做干燥剂吗
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填空。
(1)1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德•埃特尔在哈伯研究所证实了N2与H2在固体催化剂表面合成氨的反应过程。示意图如图(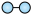 、
、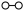 、
、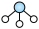 分别表示N2、H2、NH3):
分别表示N2、H2、NH3):
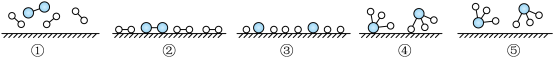
图②表示N2、H2被吸附在催化剂表面,图⑤表示生成的NH3离开催化剂表面,则图③表示___________ ,写出哈伯法合成氨的化学方程式___________ 。
(2)实验室利用复分解反应原理制取NH3的化学方程式是___________ 。
(3)合成法制硝酸是以NH3为原料,经催化氧化后再用水吸收来实现的。写出NH3催化氧化的化学方程式___________ ;若开始时投入17吨NH3,最后生产出的硝酸为42吨,则硝酸的产率是___________ 。
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应最好使用___________ (填“浓”或“稀”)硝酸,结合化学用语简述选择的理由___________ 。
(1)1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德•埃特尔在哈伯研究所证实了N2与H2在固体催化剂表面合成氨的反应过程。示意图如图(
 、
、 、
、 分别表示N2、H2、NH3):
分别表示N2、H2、NH3):
图②表示N2、H2被吸附在催化剂表面,图⑤表示生成的NH3离开催化剂表面,则图③表示
(2)实验室利用复分解反应原理制取NH3的化学方程式是
(3)合成法制硝酸是以NH3为原料,经催化氧化后再用水吸收来实现的。写出NH3催化氧化的化学方程式
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应最好使用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】依据下图中氮元素及其化合物的转化关系,回答问题:

(1)图1中, 的化学式为
的化学式为___________ ,从化合价上看, 具有
具有___________ (填“氧化性”或“还原性”)。
(2)回答下列关于 的问题:
的问题:
①实验室常用 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为___________ 。
②下列试剂不能用于干燥 的是
的是___________ (填字母)。
A.浓硫酸 B.碱石灰 C. 固体 D.
固体 D. E.
E.
(3)若要收集一瓶氨气,请将上述装置补充完整,在图2虚框内画出连接图_________ 。

(4)氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:___________ 。
(5)回答下列关于 的问题:
的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体 和
和 反应可转化为无害气体排放,写出相关反应的化学方程式:
反应可转化为无害气体排放,写出相关反应的化学方程式:___________ 。
② 和
和 按一定比例混合可以被
按一定比例混合可以被 溶液完全吸收,写出相关反应的化学方程式:
溶液完全吸收,写出相关反应的化学方程式:___________ 。
③工业生产中利用氨水吸收 和
和 ,原理如图所示。
,原理如图所示。

 被吸收过程的离子方程式为
被吸收过程的离子方程式为___________ 。

(1)图1中,
 的化学式为
的化学式为 具有
具有(2)回答下列关于
 的问题:
的问题:①实验室常用
 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为②下列试剂不能用于干燥
 的是
的是A.浓硫酸 B.碱石灰 C.
 固体 D.
固体 D. E.
E.
(3)若要收集一瓶氨气,请将上述装置补充完整,在图2虚框内画出连接图

(4)氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:
(5)回答下列关于
 的问题:
的问题:①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体
 和
和 反应可转化为无害气体排放,写出相关反应的化学方程式:
反应可转化为无害气体排放,写出相关反应的化学方程式:②
 和
和 按一定比例混合可以被
按一定比例混合可以被 溶液完全吸收,写出相关反应的化学方程式:
溶液完全吸收,写出相关反应的化学方程式:③工业生产中利用氨水吸收
 和
和 ,原理如图所示。
,原理如图所示。
 被吸收过程的离子方程式为
被吸收过程的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁是生活中常用的金属,利用铁的相关知识回答下列相关问题。
(1)生活中常使用铁锅炒菜,所利用的金属的物理性质是_______ 。
(2)在食品的包装袋中,经常放一小袋颗粒极细的铁粉,俗称“双吸粉”。铁粉能够吸收的物质是_______ (填写化学式)。
(3)铁的氧化物之一氧化铁的用途有_______ (写出一种),将少量的氧化铁固体加入到氢碘酸中,发生反应的离子方程式是_______ 。
(4)将一定量的 、
、 和
和 的混合物放入体积为
的混合物放入体积为 ,浓度为
,浓度为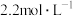 的
的 溶液中,充分反应后,生成气体
溶液中,充分反应后,生成气体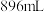 (标准状况),得到不溶固体
(标准状况),得到不溶固体 。过滤后,滤液中的金属离子只有
。过滤后,滤液中的金属离子只有 (假设滤液体积仍为
(假设滤液体积仍为 )。向滤液中加入
)。向滤液中加入 溶液至
溶液至 时开始出现沉淀。则未滴加
时开始出现沉淀。则未滴加 溶液前滤液中
溶液前滤液中 的物质的量浓度为
的物质的量浓度为_______ 。
(5)已知稀硝酸具有强氧化性,通常被还原成 ,向一定量的稀硝酸中加入足量的铁粉,发生氧化还原反应,写出对应的离子反应方程式
,向一定量的稀硝酸中加入足量的铁粉,发生氧化还原反应,写出对应的离子反应方程式_______ 。
(6)绿矾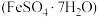 受热分解可以生成氧化铁、二氧化硫、三氧化硫、水。取少量绿矾固体加热一段时间后,某同学欲检验绿矾是否完全分解,取分解后的固体样品少许溶解在稀硫酸中,然后取样加入检验试剂,该同学需要用到的检验试剂是
受热分解可以生成氧化铁、二氧化硫、三氧化硫、水。取少量绿矾固体加热一段时间后,某同学欲检验绿矾是否完全分解,取分解后的固体样品少许溶解在稀硫酸中,然后取样加入检验试剂,该同学需要用到的检验试剂是_______ 。(写出检验试剂名称)
(1)生活中常使用铁锅炒菜,所利用的金属的物理性质是
(2)在食品的包装袋中,经常放一小袋颗粒极细的铁粉,俗称“双吸粉”。铁粉能够吸收的物质是
(3)铁的氧化物之一氧化铁的用途有
(4)将一定量的
 、
、 和
和 的混合物放入体积为
的混合物放入体积为 ,浓度为
,浓度为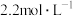 的
的 溶液中,充分反应后,生成气体
溶液中,充分反应后,生成气体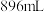 (标准状况),得到不溶固体
(标准状况),得到不溶固体 。过滤后,滤液中的金属离子只有
。过滤后,滤液中的金属离子只有 (假设滤液体积仍为
(假设滤液体积仍为 )。向滤液中加入
)。向滤液中加入 溶液至
溶液至 时开始出现沉淀。则未滴加
时开始出现沉淀。则未滴加 溶液前滤液中
溶液前滤液中 的物质的量浓度为
的物质的量浓度为(5)已知稀硝酸具有强氧化性,通常被还原成
 ,向一定量的稀硝酸中加入足量的铁粉,发生氧化还原反应,写出对应的离子反应方程式
,向一定量的稀硝酸中加入足量的铁粉,发生氧化还原反应,写出对应的离子反应方程式(6)绿矾
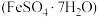 受热分解可以生成氧化铁、二氧化硫、三氧化硫、水。取少量绿矾固体加热一段时间后,某同学欲检验绿矾是否完全分解,取分解后的固体样品少许溶解在稀硫酸中,然后取样加入检验试剂,该同学需要用到的检验试剂是
受热分解可以生成氧化铁、二氧化硫、三氧化硫、水。取少量绿矾固体加热一段时间后,某同学欲检验绿矾是否完全分解,取分解后的固体样品少许溶解在稀硫酸中,然后取样加入检验试剂,该同学需要用到的检验试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氮及其化合物与生产生活及环境息息相关。请回答下列问题:
(1)N2在常温下性质很稳定,任意写出一种与此性质有关的用途:_____ 。
(2)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是_____ 。
A.酸雨 B.光化学烟雾 C. 白色污染 D.温室效应
②在含有a g HNO3的稀硝酸中,加入b g铁粉充分反应,铁全部溶解并生成NO,有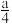 g HNO3被还原,则a∶b可能为
g HNO3被还原,则a∶b可能为_____ 。
A.2∶1 B.3∶1 C.4∶1 D.9∶2
(3)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式_____ ,氧化产物与还原产物的物质的量之比为_____ 。
(1)N2在常温下性质很稳定,任意写出一种与此性质有关的用途:
(2)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是
A.酸雨 B.光化学烟雾 C. 白色污染 D.温室效应
②在含有a g HNO3的稀硝酸中,加入b g铁粉充分反应,铁全部溶解并生成NO,有
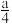 g HNO3被还原,则a∶b可能为
g HNO3被还原,则a∶b可能为A.2∶1 B.3∶1 C.4∶1 D.9∶2
(3)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式
您最近一年使用:0次

 。
。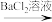 白色沉淀
白色沉淀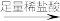 沉淀不溶解
沉淀不溶解 无沉淀
无沉淀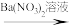 白色沉淀
白色沉淀

