1 . 酸和醇反应是合成酯的一种重要方法,例如:
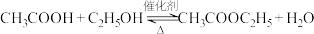
丙烯酸乙酯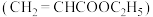 是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:
是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:

回答下列问题:
(1)乙烯和丙烯互称为__________ (填“同系物”或“同分异构体”)。
(2)乙醇分子中的官能团名称为___________ (填“羟基”或“羧基”)。
(3)有机物X的结构简式为__________ 。
(4)丙烯酸乙酯有两种官能团,它能发生的化学反应类型为______ (填标号)。
a.加成反应 b.水解反应 c.置换反应
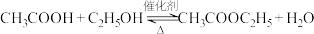
丙烯酸乙酯
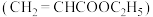 是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:
是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:
回答下列问题:
(1)乙烯和丙烯互称为
(2)乙醇分子中的官能团名称为
(3)有机物X的结构简式为
(4)丙烯酸乙酯有两种官能团,它能发生的化学反应类型为
a.加成反应 b.水解反应 c.置换反应
您最近一年使用:0次
2 . 基于自然界可再生资源获得石油化工产品,是绿色化学的研究热点。一定条件下,以纤维素和淀粉为原料,制备对二甲苯 (PX) 的合成路线如下:
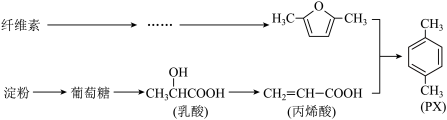
(1)下列关于纤维素、淀粉和葡萄糖的说法,正确的是
(2)乳酸的某些性质类似于乙醇和乙酸。下列关于乳酸的说法,正确的是
(3)化合物 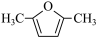 的某些性质类似于乙烯,在一定条件下与H2反应,生成化合物
的某些性质类似于乙烯,在一定条件下与H2反应,生成化合物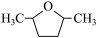 ,该反应类型为
,该反应类型为
(4)丙烯酸能通过原子利用率 100% 的加聚反应生成高分子化合物。下列化合物中,也能发生原子利用率100%的加聚反应的是
(5)化合物PX属于

(1)下列关于纤维素、淀粉和葡萄糖的说法,正确的是
| A.葡萄糖属于二糖 |
| B.葡萄糖可发生银镜反应 |
| C.稀酸催化下,纤维素和淀粉都能发生水解反应 |
| D.人体不能吸收纤维素,因此不宜食用含纤维素的食物 |
| A.分子式为C3H6O3 |
| B.能与NaOH反应 |
| C.能与CH3CH2OH发生酯化反应 |
| D.能与CH3COOH发生酯化反应 |
 的某些性质类似于乙烯,在一定条件下与H2反应,生成化合物
的某些性质类似于乙烯,在一定条件下与H2反应,生成化合物 ,该反应类型为
,该反应类型为| A.取代反应 | B.加成反应 | C.氧化反应 | D.水解反应 |
| A.乙烷 | B.乙烯 | C.乙醇 | D.氯乙烯 |
| A.烷烃 | B.芳香烃 | C.链状烃 | D.不饱和烃 |
您最近一年使用:0次
3 . 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工发展水平。请回答下列问题。
(1)乙烯的电子式为____ ,结构简式为____ 。
(2)鉴别甲烷和乙烯可用的试剂是____ (填字母)。
A 稀硫酸 B 溴的四氯化碳溶液
C 水 D 酸性高锰酸钾溶液
(3)已知2CH3CHO+O2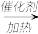 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如图所示。
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如图所示。
乙烯 A
A B
B 乙酸
乙酸
反应②的化学方程式为________ 。
工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为____ ,反应类型是____ 。
(1)乙烯的电子式为
(2)鉴别甲烷和乙烯可用的试剂是
A 稀硫酸 B 溴的四氯化碳溶液
C 水 D 酸性高锰酸钾溶液
(3)已知2CH3CHO+O2
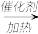 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如图所示。
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如图所示。乙烯
 A
A B
B 乙酸
乙酸反应②的化学方程式为
工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为
您最近一年使用:0次
2020-03-09更新
|
385次组卷
|
2卷引用:广东省2020年普通高中学业水平考试化学合格性考试模拟试题(六)
解题方法
4 . 对氯苯乙腈是制备医药、农药及染料的中间体,其合成路线如图所示:
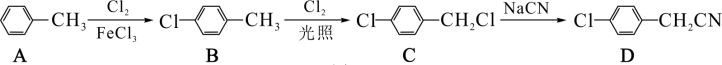
已知化合物A、B的沸点依次为110.6℃、162.0℃,两者均易溶于有机溶剂,难溶于水。回答下列问题。
(1)化合物A的名称是____ ,其核磁共振氢谱有____ 组(个)峰。
(2)化合物B的分子式为___ ;苯环上有两个取代基的B的同分异构体为___ (写结构简式)。
(3)化合物C的官能团是____ ,由C生成D的反应类型为____ 。
(4)分离A和B的方法为____ (填“萃取”或“蒸馏”),其原因是___ 。
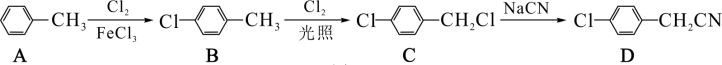
已知化合物A、B的沸点依次为110.6℃、162.0℃,两者均易溶于有机溶剂,难溶于水。回答下列问题。
(1)化合物A的名称是
(2)化合物B的分子式为
(3)化合物C的官能团是
(4)分离A和B的方法为
您最近一年使用:0次
5 . 我国科学家首次在实验室实现从CO2到淀粉的全合成。其部分合成路线如图所示:
CO2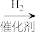 CH3OH
CH3OH HCHO
HCHO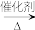 …→(C6H10O5)n
…→(C6H10O5)n
(1)CH3OH分子中与氧原子形成共价键的原子为_______ 。
(2)CH3CHO与HCHO互为同系物,具有相同的官能团是_______ (写名称)。
(3)CO2催化加H2制CH3OH,该反应一般由以下两步反应实现:
Ⅰ. CO2+H2⇌CO+H2O Ⅱ. ……
写出一定条件下反应Ⅱ的化学方程式:_______ 。
CO2
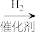 CH3OH
CH3OH HCHO
HCHO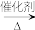 …→(C6H10O5)n
…→(C6H10O5)n(1)CH3OH分子中与氧原子形成共价键的原子为
(2)CH3CHO与HCHO互为同系物,具有相同的官能团是
(3)CO2催化加H2制CH3OH,该反应一般由以下两步反应实现:
Ⅰ. CO2+H2⇌CO+H2O Ⅱ. ……
写出一定条件下反应Ⅱ的化学方程式:
您最近一年使用:0次
6 . 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工发展水平。请回答下列问题:
(1)乙烯的结构简式为________ 。
(2)鉴别甲烷和乙烯的试剂是________ (填字母)。
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是________ (填字母)。
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
(4)若以乙烯为主要原料合成乙酸,其合成路线如图所示。

则反应③的反应类型为________ ,反应②的化学方程式为________________________________ 。
(1)乙烯的结构简式为
(2)鉴别甲烷和乙烯的试剂是
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
(4)若以乙烯为主要原料合成乙酸,其合成路线如图所示。

则反应③的反应类型为
您最近一年使用:0次
7 . 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工发展水平。请回答下列问题:
(1)乙烯的结构简式为___ 。
(2)鉴别甲烷和乙烯的试剂是___ (填字母)。
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是___ (填字母)。
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
(4)若以乙烯为主要原料合成乙酸,其合成路线如图所示。

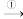
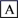
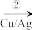
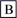

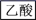
则反应①的反应类型为___ ,A、B中含有的官能团名称分别为___ 、___ ,反应②的化学方程式为___ 。
(1)乙烯的结构简式为
(2)鉴别甲烷和乙烯的试剂是
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
(4)若以乙烯为主要原料合成乙酸,其合成路线如图所示。

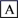
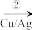
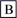

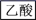
则反应①的反应类型为
您最近一年使用:0次
8 . 现以A为主要原料合成乙酸乙酯,其合成路线如图所示:
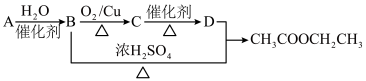
回答下列问题:
(1)写出C的结构简式:
(2)B、D分子中的官能团名称分别是
(3)写出A→B的反应类型:
(4)1 mol A与氯气发生完全加成反应,所得产物与氯气在光照的条件下发生完全取代反应,则两个过程中消耗的氯气的总的物质的量是
您最近一年使用:0次
2011高二·江苏南通·学业考试
解题方法
9 . (1)某肉制品包装上印有相关配料:精选瘦肉、食盐、胭脂红、苯甲酸钠。其中属于调味剂的是_________ ,属于着色剂的是__________ ,属于防腐剂的是_________ 。
(2)亚硝酸钠有毒,其外观和咸味与食盐很相似,因此要防止因误食亚硝酸钠而发生事故。亚硝酸钠和氯化钠的部分性质如下表:
①请根据表中信息设计一种鉴别NaNO2和NaCl的方法,写出简单的操作过程、现象和结论:_________________________________________________________________
②碘是人体中不可缺少的_________ (选填“常量”或“微量”)元素。
③食盐中加入碘元素能有效防止缺碘引起的疾病。以前在食盐中加入碘化钾(KI),放置一年后,碘流失约92%。现在食盐中加入碘酸钾(KIO3),在相同条件下碘仅损失约7%。食盐中加入碘化钾的碘损失率高的原因是______ ;(填字母)。
a.碘化钾被氧化,造成碘化钾的碘损失率高。
b.碘化钾升华,造成碘化钾的碘损失率高。
c.碘化钾与食物中的成分发生反应,造成碘化钾的碘损失率高。
④萃取碘水中的碘时,一般选用的试剂是(填字母)_____________ ;
A.酒精 B.四氯化碳 C.乙酸
⑤可用盐酸酸化的碘化钾和淀粉溶液检验食盐中的碘酸钾。反应化学方程式为: 5KI+KIO3+ 6HCl ="=" 6KCl + 3I2 + 3H2O,反应的现象是________________________
⑥已知碘酸钾受热易分解,你认为在用碘酸钾加碘盐进行烹饪时应注意什么问题?__________________ 。
⑶糖类、油脂、蛋白质都是人体必需的营养物质。
①油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和________ (写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
②氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(—NH2)和____________ (写结构简式)。人体中共有二十多种氨基酸,其中人体自身_____ (填“能”或“不能”)合成的氨基酸称为人体必需氨基酸。
③淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水。写出葡萄糖在体内被氧化的化学方程式:______________ 。
(2)亚硝酸钠有毒,其外观和咸味与食盐很相似,因此要防止因误食亚硝酸钠而发生事故。亚硝酸钠和氯化钠的部分性质如下表:
性质 | 亚硝酸钠 | 氯化钠 |
1.酸性条件下的稳定性 | 微热时分解为NO和NO2 | 微热时不分解 |
| 2.熔点 | 271℃ | 801℃ |
3.室温时的溶解度 | 约80g | 约35g |
①请根据表中信息设计一种鉴别NaNO2和NaCl的方法,写出简单的操作过程、现象和结论:
②碘是人体中不可缺少的
③食盐中加入碘元素能有效防止缺碘引起的疾病。以前在食盐中加入碘化钾(KI),放置一年后,碘流失约92%。现在食盐中加入碘酸钾(KIO3),在相同条件下碘仅损失约7%。食盐中加入碘化钾的碘损失率高的原因是
a.碘化钾被氧化,造成碘化钾的碘损失率高。
b.碘化钾升华,造成碘化钾的碘损失率高。
c.碘化钾与食物中的成分发生反应,造成碘化钾的碘损失率高。
④萃取碘水中的碘时,一般选用的试剂是(填字母)
A.酒精 B.四氯化碳 C.乙酸
⑤可用盐酸酸化的碘化钾和淀粉溶液检验食盐中的碘酸钾。反应化学方程式为: 5KI+KIO3+ 6HCl ="=" 6KCl + 3I2 + 3H2O,反应的现象是
⑥已知碘酸钾受热易分解,你认为在用碘酸钾加碘盐进行烹饪时应注意什么问题?
⑶糖类、油脂、蛋白质都是人体必需的营养物质。
①油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和
②氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(—NH2)和
③淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水。写出葡萄糖在体内被氧化的化学方程式:
您最近一年使用:0次
解题方法
10 . 阅读短文,回答问题。
2023年3月,科研成果“温和压力条件下实现乙二醇合成”入选2022年度中国科学十大进展,该成果有望促进煤化工的绿色发展,降低我国乙二醇产业对石油的依赖。
乙二醇是我国需求量非常大的一种化工原料,塑料瓶、纺织品、水箱防冻液等随处可见的生活用品都离不开它。传统工艺中,乙二醇主要以石油为原料合成得到,但我国石油高度依赖进口,开发利用我国相对丰富的煤炭资源,代替石油生产乙二醇,意义重大。
煤制乙二醇,催化是关键一环。原有合成方法中,催化剂稳定性差,且需要高压氢气,不仅存在安全隐患,产品纯度也不高。我国科研工作者将富勒烯与铜催化剂相结合,改进了一直以来煤制乙二醇的技术“卡点”,实现了在近常压和低于200℃的条件下制备乙二醇,大幅提高煤制乙二醇的安全性、效率和纯度。
请依据以上短文,判断下列说法是否正确。
(1)乙二醇属于无机化合物。___________
(2)由乙二醇作水箱防冻液,可推测乙二醇溶于水。___________
(3)煤制乙二醇可在温和条件下进行,无需使用催化剂。___________
(4)该科研成果有望降低我国乙二醇合成工业对石油的依赖。___________
2023年3月,科研成果“温和压力条件下实现乙二醇合成”入选2022年度中国科学十大进展,该成果有望促进煤化工的绿色发展,降低我国乙二醇产业对石油的依赖。
乙二醇是我国需求量非常大的一种化工原料,塑料瓶、纺织品、水箱防冻液等随处可见的生活用品都离不开它。传统工艺中,乙二醇主要以石油为原料合成得到,但我国石油高度依赖进口,开发利用我国相对丰富的煤炭资源,代替石油生产乙二醇,意义重大。
煤制乙二醇,催化是关键一环。原有合成方法中,催化剂稳定性差,且需要高压氢气,不仅存在安全隐患,产品纯度也不高。我国科研工作者将富勒烯与铜催化剂相结合,改进了一直以来煤制乙二醇的技术“卡点”,实现了在近常压和低于200℃的条件下制备乙二醇,大幅提高煤制乙二醇的安全性、效率和纯度。
请依据以上短文,判断下列说法是否正确。
(1)乙二醇属于无机化合物。
(2)由乙二醇作水箱防冻液,可推测乙二醇溶于水。
(3)煤制乙二醇可在温和条件下进行,无需使用催化剂。
(4)该科研成果有望降低我国乙二醇合成工业对石油的依赖。
您最近一年使用:0次



