解题方法
1 . 下表是元素周期表的一部分。
回答问题:
(1)门捷列夫科学地预言了“类铝”元素Ga, Ga在元素周期表中的位置是第_______ 周期、第_______ 族。
(2)第三周期主族元素中,金属性最强的元素原子结构示意图为_______ 。
(3)碳元素的一种放射性核素 C可用于文物年代的测定,
C可用于文物年代的测定, C 的原子核内中子数为
C 的原子核内中子数为_______ 。
(4)某研究小组探究氯与溴非金属性的强弱关系,过程如下:
[预测]非金属性: Cl>Br。
[设计与实验]如图所示,在点滴板的2个孔穴中分别滴入3滴新制氯水,然后向其中之一滴加3滴NaBr溶液。

[证据与分析]滴加NaBr溶液的孔穴中,溶液颜色变深,说明有Br2生成。
[结论]预测_______ (选项“正确”或“不正确”)。
[解释]从原子结构的角度解释为_______ 。
族 周期 | I A | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | C | ||||||
| 3 | Na | Mg | Al | Si | P | S | Cl |
| 4 | Ga | Br |
回答问题:
(1)门捷列夫科学地预言了“类铝”元素Ga, Ga在元素周期表中的位置是第
(2)第三周期主族元素中,金属性最强的元素原子结构示意图为
(3)碳元素的一种放射性核素
 C可用于文物年代的测定,
C可用于文物年代的测定, C 的原子核内中子数为
C 的原子核内中子数为(4)某研究小组探究氯与溴非金属性的强弱关系,过程如下:
[预测]非金属性: Cl>Br。
[设计与实验]如图所示,在点滴板的2个孔穴中分别滴入3滴新制氯水,然后向其中之一滴加3滴NaBr溶液。

[证据与分析]滴加NaBr溶液的孔穴中,溶液颜色变深,说明有Br2生成。
[结论]预测
[解释]从原子结构的角度解释为
您最近一年使用:0次
2 . 元素周期表的建立和元素周期律的发现,揭示了元素“位”“构”“性”之间的内在联系,可以根据“位”“构”的特点预测和解释元素的性质。下图是元素周期表的一部分,请回答下列问题:
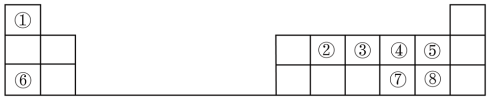
(1)元素⑦在周期表中的位置是
(2)元素③、④的原子半径大小关系正确的是
(3)元素④、⑦的非金属性强弱关系正确的是
(4)元素①、⑧形成化合物的电子式正确的是
(5)元素②有多种同位素,这些同位素具有相同的
(6)下列各组元素形成的化合物中只含有离子键的是

(1)元素⑦在周期表中的位置是
| A.第二周期、第ⅣA族 | B.第二周期、第ⅥA族 |
| C.第三周期、第ⅣA族 | D.第三周期、第ⅥA族 |
| A.③>④ | B.③<④ | C.③=④ | D.无法确定 |
| A.④>⑦ | B.④<⑦ | C.④=⑦ | D.无法确定 |
| A.HCl | B.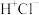 | C.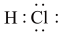 | D.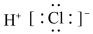 |
| A.质量数和电子数 | B.质子数和电子数 |
| C.质子数和中子数 | D.质量数和中子数 |
| A.①和④ | B.②和④ | C.①和⑤ | D.⑥和⑧ |
您最近一年使用:0次
名校
解题方法
3 . 钠及其重要化合物之间的转化关系如图所示:

回答下列问题;
(1)钠元素在周期表中的位置___ ,少量的钠应保存在___ 。
(2)Na2O2的颜色为___ ,其用途为___ 。
(3)反应①中的氧化剂是___ 。
(4)反应①中4.6g的金属钠与足量的水反应生成标况下___ L氢气,转移的电子的物质的量为___ mol。

回答下列问题;
(1)钠元素在周期表中的位置
(2)Na2O2的颜色为
(3)反应①中的氧化剂是
(4)反应①中4.6g的金属钠与足量的水反应生成标况下
您最近一年使用:0次
2012高二·江苏扬州·学业考试
4 . 物质A、B、C、D、E、F、G、H、I、J、K有下图转化关系,其中气体D、E为单质,请按要求回答下列问题。
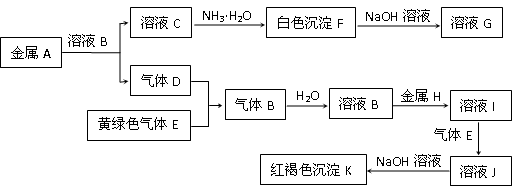
(1)金属A元素在周期表的位置是______ ,G的化学式是______ 。
(2)写出反应“C→F”的离子方程式______ ;
(3)写出反应“I→J”的离子方程式______ ;
(4)写出金属 H与水蒸气在高温下反应的化学方程式______ 。

(1)金属A元素在周期表的位置是
(2)写出反应“C→F”的离子方程式
(3)写出反应“I→J”的离子方程式
(4)写出金属 H与水蒸气在高温下反应的化学方程式
您最近一年使用:0次
2016-12-08更新
|
534次组卷
|
3卷引用:2011-2012学年江苏省扬州市普通高中学业水平测试化学(必修)模拟试卷(一)
(已下线)2011-2012学年江苏省扬州市普通高中学业水平测试化学(必修)模拟试卷(一)2016届江苏省沭阳县如东中学高三上学期阶段考试化学试卷2016届山西省曲沃中学校高三上学期阶段性考试化学试卷
2010高三·湖南·学业考试
5 . A、B、D和E四种元素均为短周期元素,原子序数逐渐增大.A元素原子的核外电子数、电子层数和最外层电子数均相等.B、D、E三种元素在周期表中相对位置如图①所示,只有E元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、B、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为N2H4,可作火箭燃料;甲、乙为非金属单质;X分子中含有10个电子.它们之间的转化关系如图②所示。
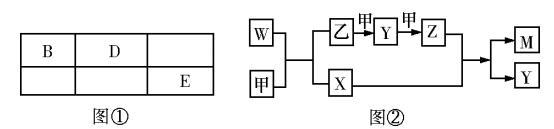
回答下列问题:
(1)Z的化学式为________________________ 。
(2)E 的单质与水反应的离子方程式为__________________________ 。
(3)W—空气燃料电池是一种碱性燃料电池,电解质溶液是20% ~30%的KOH溶液。W—空气燃料电池放电时,负极反应式为________________________________ 。
(4)将一定量的A2、B2 的混合气体放入2L密闭容器中,在500°C、2°C×107Pa下达到平衡。测得平衡气体的总物质的量为0.5mol,其中A2 为0.3mol,B2 为0.1mol。则该条件下A2 的平衡转化率为_______ ,该温度下反应2BA3(g ) 3A2(g)+B2(g)的平衡常数为
3A2(g)+B2(g)的平衡常数为_________ 。

回答下列问题:
(1)Z的化学式为
(2)E 的单质与水反应的离子方程式为
(3)W—空气燃料电池是一种碱性燃料电池,电解质溶液是20% ~30%的KOH溶液。W—空气燃料电池放电时,负极反应式为
(4)将一定量的A2、B2 的混合气体放入2L密闭容器中,在500°C、2°C×107Pa下达到平衡。测得平衡气体的总物质的量为0.5mol,其中A2 为0.3mol,B2 为0.1mol。则该条件下A2 的平衡转化率为
 3A2(g)+B2(g)的平衡常数为
3A2(g)+B2(g)的平衡常数为
您最近一年使用:0次



