元素周期表的建立和元素周期律的发现,揭示了元素“位”“构”“性”之间的内在联系,可以根据“位”“构”的特点预测和解释元素的性质。下图是元素周期表的一部分,请回答下列问题:
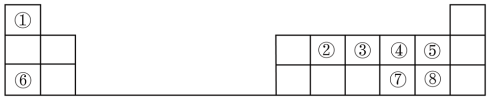
(1)元素⑦在周期表中的位置是
(2)元素③、④的原子半径大小关系正确的是
(3)元素④、⑦的非金属性强弱关系正确的是
(4)元素①、⑧形成化合物的电子式正确的是
(5)元素②有多种同位素,这些同位素具有相同的
(6)下列各组元素形成的化合物中只含有离子键的是

(1)元素⑦在周期表中的位置是
| A.第二周期、第ⅣA族 | B.第二周期、第ⅥA族 |
| C.第三周期、第ⅣA族 | D.第三周期、第ⅥA族 |
| A.③>④ | B.③<④ | C.③=④ | D.无法确定 |
| A.④>⑦ | B.④<⑦ | C.④=⑦ | D.无法确定 |
| A.HCl | B.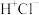 | C.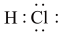 | D.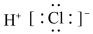 |
| A.质量数和电子数 | B.质子数和电子数 |
| C.质子数和中子数 | D.质量数和中子数 |
| A.①和④ | B.②和④ | C.①和⑤ | D.⑥和⑧ |
更新时间:2022-07-10 15:45:18
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分。根据表中的9种元素,用元素符号或化学式填空:
(1)在①~⑨元素中,金属性最强的金属元素是__________ 。(填元素符号)
(2)在①~⑨元素中,最高价氧化物的水化物呈两性的物质是__________ 。(写化学式)
(3)③、⑤、⑥对应的元素原子,半径最大的是__________ (填元素符号)。
(4)⑦和⑨可形成__________ (填“离子”或“共价”)化合物。
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(1)在①~⑨元素中,金属性最强的金属元素是
(2)在①~⑨元素中,最高价氧化物的水化物呈两性的物质是
(3)③、⑤、⑥对应的元素原子,半径最大的是
(4)⑦和⑨可形成
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)请用下列4种物质的序号填空:
①O2 ②NH4NO3 ③K2O2 ④NH3,既有离子键又有极性键的是_______ 。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为___ 。
(3)现有a~g 7种短周期元素,它们在元素周期表中的位置如图,请据此回答下列问题:
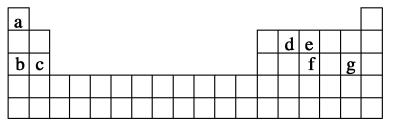
①元素的原子间反应最容易形成离子键的是_______ 。
A.c和f B.b和g C.d和g D.b和e
②d与g元素形成的分子中所有原子_______ (填“是”或“不是”)都满足最外层为8电子结构。
①O2 ②NH4NO3 ③K2O2 ④NH3,既有离子键又有极性键的是
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为
(3)现有a~g 7种短周期元素,它们在元素周期表中的位置如图,请据此回答下列问题:

①元素的原子间反应最容易形成离子键的是
A.c和f B.b和g C.d和g D.b和e
②d与g元素形成的分子中所有原子
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】下表是ⅥA族部分元素的相关性质。
请回答下列问题:
(1)硒的熔点范围可能是_______ 。
(2)碲的化合价可能有_______ 。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是_______ (填化学式)。
(4)氢硒酸有较强的_______ (填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生的化学方程式为_______ 。
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:_______
_______Al2Te3+_______=2Al(OH)3↓+_______H2Te↑
| 元素 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
请回答下列问题:
(1)硒的熔点范围可能是
(2)碲的化合价可能有
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是
(4)氢硒酸有较强的
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
_______Al2Te3+_______=2Al(OH)3↓+_______H2Te↑
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)鉴于 的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的_______ 族。
(2)甲元素 层上7个电子,甲元素与硫元素相比,非金属性较强的是
层上7个电子,甲元素与硫元素相比,非金属性较强的是_______ (填元素名称),写出可以验证该结论的一个化学方程式:_______ 。
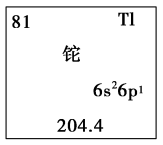
(3)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如图所示。下列叙述不正确的是_______(填字母)。
(1)鉴于
 的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的(2)甲元素
 层上7个电子,甲元素与硫元素相比,非金属性较强的是
层上7个电子,甲元素与硫元素相比,非金属性较强的是(3)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如图所示。下列叙述不正确的是_______(填字母)。

| A.铊元素在元素周期表中的位置是第六周期第ⅡA族 |
B.铊原子的中子数为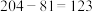 |
| C.铊原子有6个电子层,最外电子层上有3个电子 |
| D.铊元素的金属性比铝元素的强 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下表是元素周期表的一部分,根据所给的10种元素,完成以下各小题。
(1)金属性最强的元素是___________ (填元素符号)。最不活泼元素的原子结构示意图为___________ 。
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是___________ (填元素名称)。
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式___________ 。
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | N | F | Ne | ||||
| 3 | Na | Mg | Al | S | Cl |
(1)金属性最强的元素是
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】针对下面10种元素,完成以下各小题。
(1)地壳中含量最多的元素是_______ (填名称)。
(2)化学性质最不活泼的元素是_______ (填元素符号)。
(3)Al的原子结构示意图为_______ 。
(4)C与N相比,原子半径较小的是_______ 。
(5)最高价氧化物对应的水化物碱性最强的是_______ (填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是_______ 。
(7)S和Cl相比,元素非金属性较强的是_______ 。
(8)可用来制造光导纤维的物质是_______ ,晶体硅的主要用途是_______ (写出一种)。
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:_______ 。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(1)地壳中含量最多的元素是
(2)化学性质最不活泼的元素是
(3)Al的原子结构示意图为
(4)C与N相比,原子半径较小的是
(5)最高价氧化物对应的水化物碱性最强的是
(6)MgO和Al2O3中,属于两性氧化物的是
(7)S和Cl相比,元素非金属性较强的是
(8)可用来制造光导纤维的物质是
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】由以下一些微粒: 、
、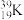 、
、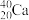 、
、 、
、 、
、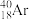 ,其中:
,其中:
(1)互为同位素的是________ 和________ ;
(2)质量数相等,但不能互称同位素的是_________ 和__________ ;
(3)中子数相等,但质子数不相等的是______ 和_______ 、______ 和_______ 。
 、
、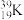 、
、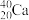 、
、 、
、 、
、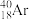 ,其中:
,其中:(1)互为同位素的是
(2)质量数相等,但不能互称同位素的是
(3)中子数相等,但质子数不相等的是
您最近一年使用:0次
【推荐2】(1)下列3种不同粒子 、
、 、
、 表示
表示_______ 种元素,_____ 种核素, 、
、 、
、 互称为
互称为______ 。
(2)有人称煤炭是“工业的粮食”,通过煤的综合利用可以获得重要化工原料,如焦炭,它是煤的_______ (填“蒸馏”或“干馏”)产物,可用于______ (填出一种用途);以煤为原料可以制得水煤气,其反应的化学方程式为_______ 。
 、
、 、
、 表示
表示 、
、 、
、 互称为
互称为(2)有人称煤炭是“工业的粮食”,通过煤的综合利用可以获得重要化工原料,如焦炭,它是煤的
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】下面所列的是一组你熟悉的物质:
A. HClO4 B. CO2 C. H2O D. CaO E. KOH F. MgBr2 G. H2
(1)上述物质中只存在离子键的有_____ (填“序号”,下同);只存在共价键的有__________ ;既存在离子键又存在共价键的有__________ 。
(2)上述物质中属于离子化合物的有_________ ;属于共价化合物的有___________ 。
(3)上述物质中属于非电解质的是_____ ;A和E的水溶液发生反应的离子方程式是_________ 。
A. HClO4 B. CO2 C. H2O D. CaO E. KOH F. MgBr2 G. H2
(1)上述物质中只存在离子键的有
(2)上述物质中属于离子化合物的有
(3)上述物质中属于非电解质的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下列①~⑤是中学化学常见的微粒。
① ②
② ③
③ ④
④ ⑤
⑤
用数字序号填空:
(1)立体构型为V形的是_______ 。
(2)中心原子的杂化轨道类型为 的是
的是_______ 。
(3)所有原子共线的是_______ 。
(4)存在配位键的是_______ 。
(5)含有非极性键的极性分子是_______ 。
①
 ②
② ③
③ ④
④ ⑤
⑤
用数字序号填空:
(1)立体构型为V形的是
(2)中心原子的杂化轨道类型为
 的是
的是(3)所有原子共线的是
(4)存在配位键的是
(5)含有非极性键的极性分子是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)在下列各组物质中:
A O2和O3 B 氘和氚 C CH4和CH3(CH2)2CH3
D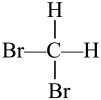 和
和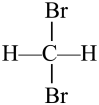 E CH3(CH2)2 CH3和
E CH3(CH2)2 CH3和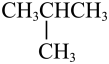
①互为同位素的是__________ ②互为同素异形体的是______ .
③互为同系物的是__________ ④互为同分异构的是_____ .(均填选项号)
(2)下列各种物质:①H2O②NH3③KOH④Na2O2⑤MgCl2⑥Ne ,不存在化学键的是_____ ;只存在离子键的是_____ ;属于共价化合物的是_______ ;含非极性键的离子化合物是__________________ 。
(3)CO2的电子式为________________ ;NH3的结构式为 _______________ ;
(4)Na2O2熔化时被破坏的是________ 。
A O2和O3 B 氘和氚 C CH4和CH3(CH2)2CH3
D
 和
和 E CH3(CH2)2 CH3和
E CH3(CH2)2 CH3和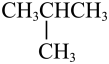
①互为同位素的是
③互为同系物的是
(2)下列各种物质:①H2O②NH3③KOH④Na2O2⑤MgCl2⑥Ne ,不存在化学键的是
(3)CO2的电子式为
(4)Na2O2熔化时被破坏的是
您最近一年使用:0次

 O、
O、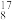 O、
O、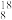 O三种核素,氢元素有
O三种核素,氢元素有 H、
H、 H、
H、 三种核素。
三种核素。

