回答下列问题:
(1)鉴于 的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的_______ 族。
(2)甲元素 层上7个电子,甲元素与硫元素相比,非金属性较强的是
层上7个电子,甲元素与硫元素相比,非金属性较强的是_______ (填元素名称),写出可以验证该结论的一个化学方程式:_______ 。
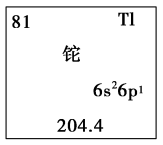
(3)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如图所示。下列叙述不正确的是_______(填字母)。
(1)鉴于
 的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的(2)甲元素
 层上7个电子,甲元素与硫元素相比,非金属性较强的是
层上7个电子,甲元素与硫元素相比,非金属性较强的是(3)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如图所示。下列叙述不正确的是_______(填字母)。

| A.铊元素在元素周期表中的位置是第六周期第ⅡA族 |
B.铊原子的中子数为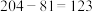 |
| C.铊原子有6个电子层,最外电子层上有3个电子 |
| D.铊元素的金属性比铝元素的强 |
更新时间:2022-03-16 11:53:06
|
相似题推荐
【推荐2】下图是元素周期表的一部分(号元素 ,用化学用语回答下列问题:
,用化学用语回答下列问题:

(1)D的基态电子排布式可简写为:___________ ;H代表的元素在周期表中的位置是___________ 。
(2)、G、J、K、M对应的简单离子的半径由大到小的顺序是___________ (用离子符号表示)
(3)在所列元素中,电负性最大的元素是___________ (填元素符号)。
(4)已知某原子的各级电离能如下:I1=577kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11578kJ/mol,则该原子在化合物中表现的化合价为___________
(5)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线规则。根据元素周期表对角线规则,金属铍Be与铝单质及其化合物性质十分相似。Be(OH)2和Mg(OH)2可用试剂NaOH溶液鉴别。涉及的化学方程式为:___________ 。
 ,用化学用语回答下列问题:
,用化学用语回答下列问题:
(1)D的基态电子排布式可简写为:
(2)、G、J、K、M对应的简单离子的半径由大到小的顺序是
(3)在所列元素中,电负性最大的元素是
(4)已知某原子的各级电离能如下:I1=577kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11578kJ/mol,则该原子在化合物中表现的化合价为
(5)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线规则。根据元素周期表对角线规则,金属铍Be与铝单质及其化合物性质十分相似。Be(OH)2和Mg(OH)2可用试剂NaOH溶液鉴别。涉及的化学方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下列说法是否正确(正确的打“√”,不正确的打“×”)若不正确请说明理由。
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。_________ ;
(2)FeCl3与Cu的反应为置换反应。_________ ;
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。_________ ;
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。_________
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。
(2)FeCl3与Cu的反应为置换反应。
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】元素周期表有____ 个横行,叫周期,每一周期中元素原子的_________ 相同,从左到右元素的金属性____ (填增强或减弱);元素周期表中有_____ 列,第ⅥA族处在第_____ 列,同一主族从上到下,元素的非金属性依次_______ (填增强或减弱)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知元素的电负性和原子半径等内容一样,也是元素的一种基本性质。下面给出14种元素的电负性:
试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,可推知元素的电负性具有的变化规律是_______ ;
(2)根据你的理解,元素的电负性指________ ;
(3)预测Br和I元素电负性的大小关系_____ 。
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,可推知元素的电负性具有的变化规律是
(2)根据你的理解,元素的电负性指
(3)预测Br和I元素电负性的大小关系
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】最新报道,我国科学家通过与多个国家进行科技合作,成功研发出铯(Cs)原子喷泉钟,使我国时间频率基准的精度从30万年不差1秒提高到600万年不差1秒,标志着我国时间频率基准研究进入世界先进行列,已知铯位于元素周期表中第六周期第IA族,根据艳在元素周期表中的位置,推断下列内容:
(1)铯的原子核外共有____ 个电子层,最外层电子数为___ .
(2)铯单质与水剧烈反应,放出______ 色气体,同时使紫色石蕊溶液显______ 色.
(3)预测铯单质的还原性比钠单质的还原性______ (填“弱”或“强”).
(1)铯的原子核外共有
(2)铯单质与水剧烈反应,放出
(3)预测铯单质的还原性比钠单质的还原性
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】实验室加热液体时常加入沸石,其主要成分为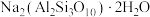 。根据其组成元素完成下列填空:
。根据其组成元素完成下列填空:
(1)元素Si在周期表中的位置是_______ 。
(2)沸石中的元素可形成多种化合物;Na元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为_______ ;化合物乙可作为呼吸面具或潜艇氧气的来源,乙是_______ (填化学式);Na与同周期非金属性最强的元素形成的化合物可做调味品,用电子式表示该化合物的形成过程_______ 。
(3)与氧元素同周期的非金属元素中,简单气态氢化物最稳定的是_______ (填化学式)。
(4)Na所在周期的主族元素中,简单离子半径最小的是_______ (填离子符号)
(5)2022年我国科学家开始参与研究Uue新元素的合成。Uue与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则 中A=
中A=_______ 、Z=_______ 。
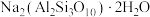 。根据其组成元素完成下列填空:
。根据其组成元素完成下列填空:(1)元素Si在周期表中的位置是
(2)沸石中的元素可形成多种化合物;Na元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
(3)与氧元素同周期的非金属元素中,简单气态氢化物最稳定的是
(4)Na所在周期的主族元素中,简单离子半径最小的是
(5)2022年我国科学家开始参与研究Uue新元素的合成。Uue与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则
 中A=
中A=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】针对下面10种元素,完成以下各小题。
(1)地壳中含量最多的元素是_______ (填名称)。
(2)化学性质最不活泼的元素是_______ (填元素符号)。
(3)Al的原子结构示意图为_______ 。
(4)C与N相比,原子半径较小的是_______ 。
(5)最高价氧化物对应的水化物碱性最强的是_______ (填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是_______ 。
(7)S和Cl相比,元素非金属性较强的是_______ 。
(8)可用来制造光导纤维的物质是_______ ,晶体硅的主要用途是_______ (写出一种)。
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:_______ 。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(1)地壳中含量最多的元素是
(2)化学性质最不活泼的元素是
(3)Al的原子结构示意图为
(4)C与N相比,原子半径较小的是
(5)最高价氧化物对应的水化物碱性最强的是
(6)MgO和Al2O3中,属于两性氧化物的是
(7)S和Cl相比,元素非金属性较强的是
(8)可用来制造光导纤维的物质是
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】按要求填空:
1.用化学用语回答下列问题:
(1)写出二氧化碳分子的电子式:___________ ;
(2)写出氮气分子的结构式___________ 。
(3)A+、Bˉ、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ C+D↑,则A+的电子式:
C+D↑,则A+的电子式:_____________ ;比较C和D的稳定性的强弱:_____________________ (用化学式表示)。
(4)用电子式表示MgCl2的形成过程__________________________________ 。
2.下列物质:① N2 ② CO2 ③ NH3 ④ Na2O ⑤Na2O2 ⑥ NaOH ⑦ CaBr2 ⑧ H2O2 ⑨ NH4Cl ⑩ Ar。
(1)既含有极性键又含有非极性键的是_______ ;(填序号,下同)
(2)含有非极性键的离子化合物是_____ 。
(3)不含化学键的是_____ 。
3.下列变化中:① 干冰气化; ② 硝酸钾熔化; ③ KHSO4熔融; ④ 硫酸溶于水;
⑤ 蔗糖溶于水;⑥ HI分解; ⑦ 碘升华; ⑧ 溴蒸气被木炭吸附。
(1)未破坏化学键的是___________ ;
(2)仅离子键被破坏的是_________ ;
(3)仅共价键被破坏的是_________ 。
4.下列物质:① 1H、2H、3H ; ② H2O、D2O、T2O; ③ O2、O3; ④ 14N、14C
(1)互为同位素的是:______ ;
(2)互为同素异形体的是:______ ;
(3)氢的三种原子1H、2H、3H 与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有________ 种。
1.用化学用语回答下列问题:
(1)写出二氧化碳分子的电子式:
(2)写出氮气分子的结构式
(3)A+、Bˉ、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ
 C+D↑,则A+的电子式:
C+D↑,则A+的电子式:(4)用电子式表示MgCl2的形成过程
2.下列物质:① N2 ② CO2 ③ NH3 ④ Na2O ⑤Na2O2 ⑥ NaOH ⑦ CaBr2 ⑧ H2O2 ⑨ NH4Cl ⑩ Ar。
(1)既含有极性键又含有非极性键的是
(2)含有非极性键的离子化合物是
(3)不含化学键的是
3.下列变化中:① 干冰气化; ② 硝酸钾熔化; ③ KHSO4熔融; ④ 硫酸溶于水;
⑤ 蔗糖溶于水;⑥ HI分解; ⑦ 碘升华; ⑧ 溴蒸气被木炭吸附。
(1)未破坏化学键的是
(2)仅离子键被破坏的是
(3)仅共价键被破坏的是
4.下列物质:① 1H、2H、3H ; ② H2O、D2O、T2O; ③ O2、O3; ④ 14N、14C
(1)互为同位素的是:
(2)互为同素异形体的是:
(3)氢的三种原子1H、2H、3H 与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下表是元素周期表的一部分,请用化学符号和对应的化学式回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为___________ 。
(2)②、③两种元素非金属性较强的是___________ ,写出一个化学方程式能证明该结论的事实___________ 。⑧、⑨、⑩三种元素的气态氢化物稳定性由强到弱的顺序是___________ ,对应的的最高价氧化物的水化物中酸性最强的是___________ 。
(3)第三周期元素形成的简单离子中半径最小的微粒是___________ 。
(4)写出元素⑨的最高价氧化物对应水化物在水中的电离方程式:___________ 。写出实验室里,检验该水化物电离出的负离子的方法:___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)②、③两种元素非金属性较强的是
(3)第三周期元素形成的简单离子中半径最小的微粒是
(4)写出元素⑨的最高价氧化物对应水化物在水中的电离方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】按要求回答下列问题:
(Ⅰ)现有下列物质:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
(1)这些物质中:只含有共价键的是_______ (填序号,下同);只含有离子键的是_______ ;既含有极性共价键又含有离子键的是_______ ;属于离子化合物的是_______ 。
(2)①的结构式是_______ ;⑥的电子式是_______ 。
(3)用电子式表示③的形成:_______ 。
(Ⅱ)为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(4)请补全汞的原子结构示意图_______ 。 、
、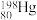 、
、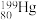 、
、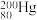 、
、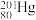 、
、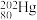 和
和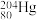 ,其中,
,其中,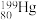 和
和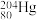 的中子数之比为
的中子数之比为_______ 。
(6)氮、磷、砷都是第VA族元素,下列说法正确的是_______ (填字母)。
a.非金属性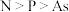 ,所以氮气最活泼
,所以氮气最活泼
b. 与
与 性质相似,
性质相似, 能与
能与 溶液反应
溶液反应
c.As的最高价氧化物对应的水化物是强酸
d.形成的简单氢化物的还原性随着原子序数递增而增强
(Ⅰ)现有下列物质:①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
(1)这些物质中:只含有共价键的是
(2)①的结构式是
(3)用电子式表示③的形成:
(Ⅱ)为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(4)请补全汞的原子结构示意图
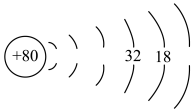
 、
、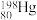 、
、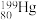 、
、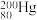 、
、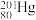 、
、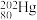 和
和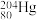 ,其中,
,其中,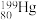 和
和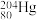 的中子数之比为
的中子数之比为(6)氮、磷、砷都是第VA族元素,下列说法正确的是
a.非金属性
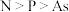 ,所以氮气最活泼
,所以氮气最活泼b.
 与
与 性质相似,
性质相似, 能与
能与 溶液反应
溶液反应c.As的最高价氧化物对应的水化物是强酸
d.形成的简单氢化物的还原性随着原子序数递增而增强
您最近一年使用:0次



