1 . 硫及其化合物广泛存在于自然界中,硫的部分化合物相互转化关系如图所示。回答下列问题: 与NaOH溶液反应可实现转化
与NaOH溶液反应可实现转化______ (填图中的序号),由该反应推断。 属于
属于______ (填“酸性”或“碱性”)氧化物。
(2)在转化②中,硫元素的化合价由+4价变成+6价,这表明 具有
具有______ (填“氧化性”或“还原性”)。
(3) 还具有氧化性,
还具有氧化性, 与
与 反应可生成
反应可生成______ (填化学式)和 ,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
(4)在加热条件下,Cu与浓硫酸反应可实现转化③,该反应中 被Cu
被Cu______ (填“氧化”或“还原”)成 。
。 能使
能使______ (填试剂名称)溶液褪色,说明 具有漂白性,因此可用作草帽、纸张等的漂白剂。
具有漂白性,因此可用作草帽、纸张等的漂白剂。
(5)为检验Cu与浓硫酸反应后溶液中的 ,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴
,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴______ (填化学式)溶液,振荡,生成______ 色沉淀,则证明溶液中含有 ,生成该沉淀的离子反应方程式为
,生成该沉淀的离子反应方程式为______ 。
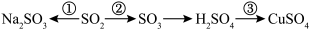
 与NaOH溶液反应可实现转化
与NaOH溶液反应可实现转化 属于
属于(2)在转化②中,硫元素的化合价由+4价变成+6价,这表明
 具有
具有(3)
 还具有氧化性,
还具有氧化性, 与
与 反应可生成
反应可生成 ,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。(4)在加热条件下,Cu与浓硫酸反应可实现转化③,该反应中
 被Cu
被Cu 。
。 能使
能使 具有漂白性,因此可用作草帽、纸张等的漂白剂。
具有漂白性,因此可用作草帽、纸张等的漂白剂。(5)为检验Cu与浓硫酸反应后溶液中的
 ,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴
,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴 ,生成该沉淀的离子反应方程式为
,生成该沉淀的离子反应方程式为
您最近一年使用:0次
2010高二下·湖南·学业考试
2 . 维生素C能增强人体对疾病的抵抗能力。
(1)将维生素C溶于水后向溶液中滴加几滴紫色石蕊试液,试液变红,说明维生素C的水溶液呈________ (填字母)。
A.酸性 B.碱性 C.氧化性 D.还原性
(2)刚切开的苹果露置在空气中易被氧气氧化而变色,如果将刚切开的苹果在溶有维生素C的水溶液中浸泡一下,苹果能保持长时期的不变色,说明维生素C具有________ (填字母)。
A.酸性 B.碱性 C.氧化性 D.还原性
(1)将维生素C溶于水后向溶液中滴加几滴紫色石蕊试液,试液变红,说明维生素C的水溶液呈
A.酸性 B.碱性 C.氧化性 D.还原性
(2)刚切开的苹果露置在空气中易被氧气氧化而变色,如果将刚切开的苹果在溶有维生素C的水溶液中浸泡一下,苹果能保持长时期的不变色,说明维生素C具有
A.酸性 B.碱性 C.氧化性 D.还原性
您最近一年使用:0次
解题方法
3 . 高锰酸钾分别在酸性、中性、碱性条件下发生的反应如下:
MnO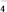 +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
MnO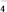 +3e-+2H2O===MnO2↓+4OH-
+3e-+2H2O===MnO2↓+4OH-
MnO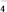 +e-===MnO
+e-===MnO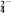 (溶液呈绿色)
(溶液呈绿色)
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的_______ 影响。
(2)将SO2通入高锰酸钾溶液中,发生氧化还原反应的离子方程式为______________ 。
(3)将PbO2投入酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法正确的是________ (填字母)。
a.氧化性:PbO2>KMnO4
b.还原性:PbO2>KMnO4
c.MnSO4溶液可以用盐酸酸化
MnO
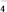 +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2OMnO
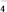 +3e-+2H2O===MnO2↓+4OH-
+3e-+2H2O===MnO2↓+4OH-MnO
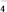 +e-===MnO
+e-===MnO (溶液呈绿色)
(溶液呈绿色)(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的
(2)将SO2通入高锰酸钾溶液中,发生氧化还原反应的离子方程式为
(3)将PbO2投入酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法正确的是
a.氧化性:PbO2>KMnO4
b.还原性:PbO2>KMnO4
c.MnSO4溶液可以用盐酸酸化
您最近一年使用:0次
4 . “鱼浮灵”又称固态双氧水,主要成分为2Na2CO3·3H2O2,是水产品运输过程中常用的化学增氧剂。某小组为探究溶液酸碱性对H2O2溶液中溶解氧含量的影响,进行了如下实验。
[查阅资料]
i.Na2SO4 溶液显中性。
ii.pH<7时, pH越小,溶液的酸性越强; pH>7时,pH越大,溶液的碱性越强。
[进行实验]
向3个均盛有80 mL 4% H2O2溶液的烧杯中,依次加入20 mL的稀硫酸、Na2SO4 溶液、NaOH溶液,分别测定溶液的pH和溶解氧含量。实验记录如下表。
[分析解释]
(1)H2O2发生分解反应的产物是___________ 。
(2)由实验②可知,H2O2 溶液显___________ ( 填字母)。
a.酸性 b.碱性
(3)综合上述实验数据,可以得出的结论是____________ 。
[应用实践]
(4)结合上述实验分析,“鱼浮灵”可以提高水中溶解氧含量的可能原因有___________ 。
[查阅资料]
i.Na2SO4 溶液显中性。
ii.pH<7时, pH越小,溶液的酸性越强; pH>7时,pH越大,溶液的碱性越强。
[进行实验]
向3个均盛有80 mL 4% H2O2溶液的烧杯中,依次加入20 mL的稀硫酸、Na2SO4 溶液、NaOH溶液,分别测定溶液的pH和溶解氧含量。实验记录如下表。
| 实验编号 | ① | ② | ③ |
| 加入的试剂 | 稀硫酸 | Na2SO4溶液 | NaOH溶液 |
| pH | 0.44 | 5.97 | 11.74 |
| 溶解氧含量/ (mg·L-1) | 5.9 | 6.5 | 13.1 |
[分析解释]
(1)H2O2发生分解反应的产物是
(2)由实验②可知,H2O2 溶液显
a.酸性 b.碱性
(3)综合上述实验数据,可以得出的结论是
[应用实践]
(4)结合上述实验分析,“鱼浮灵”可以提高水中溶解氧含量的可能原因有
您最近一年使用:0次
5 . 海带中含有丰富的碘元素,某化学兴趣小组设计如下所示的流程图提取碘:
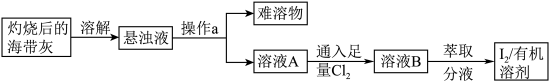
请回答下列问题:
(1)加水溶解海带灰,应采用的装置是_______ (填字母序号)
A.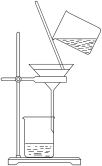 B.
B. C.
C.
(2)操作a的名称是_______ (填“过滤”或“蒸发”);
(3)溶液A中通入足量 发生的反应为:
发生的反应为: ,反应物
,反应物 表现
表现_______ (填“氧化性”或“还原性”);
(4)工业上合成氨的反应为: 。一定条件下,将2 mol
。一定条件下,将2 mol  和6 mol
和6 mol  置于1 L的密闭容器中,10 min后测得
置于1 L的密闭容器中,10 min后测得 为0.4 mol。
为0.4 mol。
①用 的浓度变化表示该反应0~10 min的平均速率为
的浓度变化表示该反应0~10 min的平均速率为_______ mol/(L·min);
②其他条件不变时,压缩容器体积,增大压强,该反应的速率将_______ (填“增大”或“减小”)。

请回答下列问题:
(1)加水溶解海带灰,应采用的装置是
A.
 B.
B. C.
C.
(2)操作a的名称是
(3)溶液A中通入足量
 发生的反应为:
发生的反应为: ,反应物
,反应物 表现
表现(4)工业上合成氨的反应为:
 。一定条件下,将2 mol
。一定条件下,将2 mol  和6 mol
和6 mol  置于1 L的密闭容器中,10 min后测得
置于1 L的密闭容器中,10 min后测得 为0.4 mol。
为0.4 mol。①用
 的浓度变化表示该反应0~10 min的平均速率为
的浓度变化表示该反应0~10 min的平均速率为②其他条件不变时,压缩容器体积,增大压强,该反应的速率将
您最近一年使用:0次
6 . “84消毒液”是常见的消毒剂,其有效成分是NaClO。
(1)Cl2和NaOH制备NaClO的化学方程式为___________ 。
(2)如图是某品牌“84消毒液”的使用注意事项。
①注意事项4“易使有色衣物脱色”,是因为“84消毒液”具有___________ 。
A.碱性 B.强氧化性
②注意事项6“不可与酸性物质同时使用”,例如,若将“84消毒液”与“洁厕灵”(含盐酸)同时使用会生成黄绿色有毒气体。写出反应的离子方程式___________ 。
(1)Cl2和NaOH制备NaClO的化学方程式为
(2)如图是某品牌“84消毒液”的使用注意事项。
| 注意事项 1、外用消毒液,勿口服; 2、现用现配,使用时注意戴手套防护; 3、不适用于钢和铝制品的消毒; 4、易使有色衣物脱色; 5、避光、阴凉处保存; 6、不可与酸性物质同时使用。 |
A.碱性 B.强氧化性
②注意事项6“不可与酸性物质同时使用”,例如,若将“84消毒液”与“洁厕灵”(含盐酸)同时使用会生成黄绿色有毒气体。写出反应的离子方程式
您最近一年使用:0次
名校
7 . 利用如图可以从不同角度研究含硫物质的性质及其转化关系。
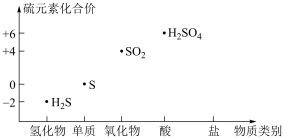
回答下列问题:
(1)H2S与SO2反应的化学方程式为____ ,反应中H2S体现____ (填“氧化性”或“还原性”)。
(2)加热时,浓硫酸与木炭反应的化学方程式为____ ,下列试剂不能用于验证生成物中含有SO2的是____ (填标号)。
a.品红溶液b.酸性KMnO4溶液c.澄清石灰水
(3)SO2的过度排放会引起酸雨,酸雨是指pH<____ 的雨水,其中NOx的排放也会导致酸雨的形成,写出NO2与水反应的化学方程式____ 。
(4)实验室可用碱液吸收法对NOx进行尾气处理,写出NO2与氢氧化钠溶液反应的离子方程式____ 。

回答下列问题:
(1)H2S与SO2反应的化学方程式为
(2)加热时,浓硫酸与木炭反应的化学方程式为
a.品红溶液b.酸性KMnO4溶液c.澄清石灰水
(3)SO2的过度排放会引起酸雨,酸雨是指pH<
(4)实验室可用碱液吸收法对NOx进行尾气处理,写出NO2与氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
名校
8 . 卤族元素在性质上具有相似性与递变性。为了验证卤族部分元素递变规律,设计如图装置进行实验。请回答下列问题。
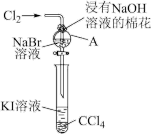
(1)A中发生反应的化学方程式是_______ 。
(2)根据上述实验操作步骤,为确保“非金属性:氯>溴>碘”的实验结论可靠,你认为做好本实验最关键因素是_______ 。
(3)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
IBr、 ICl等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(4)氯化碘 ( ICl)能与水发生反应:ICl+H2O= HIO+ HCl,该反应_______  填“是”或“不是”
填“是”或“不是” 氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为
氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为_______ 。
(5)从原子结构角度解释分子(CN)2中两种元素非金属性的强弱_______ 。
(6)已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。在NaBr和KSCN的混合溶液中通入(CN)2,反应的离子方程式为_______ 。
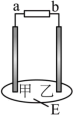
(7)如图所示,E是用饱和NaCl溶液和淀粉-KI溶液的混合液湿润的滤纸,用石墨做电极,通电后发现乙周围滤纸褪为蓝色,则下列判断正确的是
(8)下图是用强光照射广口瓶中新制氯水时传感器所获得数据的图像,下列各项代表纵坐标的物理量,其中与图像不相符的是

(9)下列变化不需要破坏化学键的是

(1)A中发生反应的化学方程式是
(2)根据上述实验操作步骤,为确保“非金属性:氯>溴>碘”的实验结论可靠,你认为做好本实验最关键因素是
(3)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
| A.Cl-、Br-、I-的还原性逐渐增强 | B.Cl2、Br2、I2的熔点逐渐升高 |
| C.HCl、HBr、HI的酸性逐渐减弱 | D.HCl、HBr、HI的稳定性逐渐减弱 |
IBr、 ICl等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(4)氯化碘 ( ICl)能与水发生反应:ICl+H2O= HIO+ HCl,该反应
 填“是”或“不是”
填“是”或“不是” 氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为
氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为(5)从原子结构角度解释分子(CN)2中两种元素非金属性的强弱
(6)已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。在NaBr和KSCN的混合溶液中通入(CN)2,反应的离子方程式为
(7)如图所示,E是用饱和NaCl溶液和淀粉-KI溶液的混合液湿润的滤纸,用石墨做电极,通电后发现乙周围滤纸褪为蓝色,则下列判断正确的是

| A.b是阳极,a是阴极 | B.a是正极,b是负极 |
| C.乙是正极,甲是负极 | D.乙是阳极,甲是阴极 |

| A.溶液中氯离子的浓度 | B.溶液的 pH |
| C.瓶中氧气的体积分数 | D.溶液的导电能力 |
| A.液态水变为水蒸气 | B.HCl 气体溶于水 |
| C.NaHCO3 受热分解 | D.NaCl 熔化 |
您最近一年使用:0次
名校
9 . 如表是元素周期表的一部分,根据表中给出的10种元素(其中X、Y分别表示某种化学元素),按要求作答。
(1)X、Y两种元素符号分别是____ 和____ 。
(2)Mg的原子序数为____ 。
(3)氧元素位于第二周期第____ 。
(4)表中失电子能力最强的原子是____ 。
(5)表中某原子最外层电子数为4,其元素符号是____ 。
(6)F与N相比,原子半径较小的是____ 。
(7)O2与S单质相比,更难与H2化合的是____ 。
(8)NH3中N元素的化合价为____ ,其水溶液呈____ (填“酸性”或“碱性”)。
(9)Cl2与水反应的生成物中具有漂白作用的是____ (填“HCl”或“HClO”),写出该反应的化学方程式:____ 。
(10)下列各项比较,符合相关性质递变规律的是____ (填标号)。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | N | O | F | X | ||||
| 3 | Na | Y | Al | Si | S | Cl |
(2)Mg的原子序数为
(3)氧元素位于第二周期第
(4)表中失电子能力最强的原子是
(5)表中某原子最外层电子数为4,其元素符号是
(6)F与N相比,原子半径较小的是
(7)O2与S单质相比,更难与H2化合的是
(8)NH3中N元素的化合价为
(9)Cl2与水反应的生成物中具有漂白作用的是
(10)下列各项比较,符合相关性质递变规律的是
| A.氧化性:O2>N2 | B.金属性:Na<Mg |
| C.酸性:H2SO4>HClO4 | D.碱性:NaOH<Mg(OH)2 |
您最近一年使用:0次
2022-07-11更新
|
447次组卷
|
2卷引用:2022年01月福建省普通高中高一学业水平合格性考试真题化学试题
解题方法
10 . 利用下图可以从不同角度研究含硫物质的性质及其转化关系。

回答下列问题:
(1) 与
与 反应的化学方程式为
反应的化学方程式为____________ ,反应中 体现
体现___________ (填“氧化性”或“还原性”)。
(2)加热时,浓硫酸与木炭反应的化学方程式为____________ ,下列试剂不能用于验证生成物中含有 的是
的是___________ (填标号)。
a. 品红溶液 b. 酸性 溶液 c. 澄清石灰水
溶液 c. 澄清石灰水

回答下列问题:
(1)
 与
与 反应的化学方程式为
反应的化学方程式为 体现
体现(2)加热时,浓硫酸与木炭反应的化学方程式为
 的是
的是a. 品红溶液 b. 酸性
 溶液 c. 澄清石灰水
溶液 c. 澄清石灰水
您最近一年使用:0次
2021-10-09更新
|
496次组卷
|
4卷引用:山东省2021年普通高中合格考化学试题
山东省2021年普通高中合格考化学试题山东省2021年夏季普通高中学业水平合格考试化学试题(已下线)3.3.1 硫循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)黑龙江省佳木斯市农垦建三江管理局第二高级中学2021-2022学年高一下学期第一次月考化学试题



