1 . 乙烯( )是一种重要的有机化工原料,其产量可以用来衡量一个国家的石油化工发展水平,回答下列问题。
)是一种重要的有机化工原料,其产量可以用来衡量一个国家的石油化工发展水平,回答下列问题。
(1)乙烯分子中的官能团名称为___________ (填“碳碳双键”或“碳碳三键”);从有机物的类别来看,乙烯属于___________ (填“饱和烃”或“不饱和烃”)。
(2)工业上可用乙烯制备乙醇,其反应的化学方程式为: 。该反应属于反应
。该反应属于反应___________ (填“加成”或“取代”)。
(3)在一定条件下,乙烯发生加聚反应生成重要的高分子化合物聚乙烯(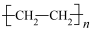 ),其反应的化学方程式为
),其反应的化学方程式为___________ 。
 )是一种重要的有机化工原料,其产量可以用来衡量一个国家的石油化工发展水平,回答下列问题。
)是一种重要的有机化工原料,其产量可以用来衡量一个国家的石油化工发展水平,回答下列问题。(1)乙烯分子中的官能团名称为
(2)工业上可用乙烯制备乙醇,其反应的化学方程式为:
 。该反应属于反应
。该反应属于反应(3)在一定条件下,乙烯发生加聚反应生成重要的高分子化合物聚乙烯(
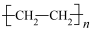 ),其反应的化学方程式为
),其反应的化学方程式为
您最近一年使用:0次
2 . 下表显示了元素周期表中短周期的大部分结构,①~④4种元素和氯元素在其中的位置如下。
回答下列问题:
(1)①的元素符号为___________ 。
(2)②的原子结构示意图为___________ 。
(3)③的最高价氧化物对应的水化物的化学式为___________ (填“ ”或“
”或“ ”)。
”)。
(4)④的单质在氧气中燃烧,可生成一种具有漂白作用的气体,写出其反应的化学方程式___________ 。
| ① | ||||||
| ② | ③ | |||||
| ④ | Cl | |||||
(1)①的元素符号为
(2)②的原子结构示意图为
(3)③的最高价氧化物对应的水化物的化学式为
 ”或“
”或“ ”)。
”)。(4)④的单质在氧气中燃烧,可生成一种具有漂白作用的气体,写出其反应的化学方程式
您最近一年使用:0次
3 . 酸和醇反应是合成酯的一种重要方法,例如:
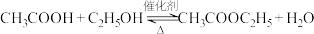
丙烯酸乙酯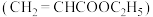 是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:
是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:

回答下列问题:
(1)乙烯和丙烯互称为__________ (填“同系物”或“同分异构体”)。
(2)乙醇分子中的官能团名称为___________ (填“羟基”或“羧基”)。
(3)有机物X的结构简式为__________ 。
(4)丙烯酸乙酯有两种官能团,它能发生的化学反应类型为______ (填标号)。
a.加成反应 b.水解反应 c.置换反应
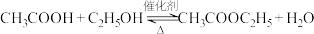
丙烯酸乙酯
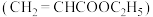 是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:
是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:
回答下列问题:
(1)乙烯和丙烯互称为
(2)乙醇分子中的官能团名称为
(3)有机物X的结构简式为
(4)丙烯酸乙酯有两种官能团,它能发生的化学反应类型为
a.加成反应 b.水解反应 c.置换反应
您最近一年使用:0次
4 . 钛冶炼厂与氯碱厂、甲醇厂组成一个产业链(如图所示),将大大提高资源的利用率,减少环境污染。
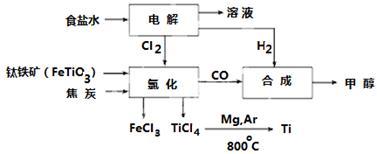
请回答下列问题:
(1)Fe位于元素周期表中第____________ 周期,第___________ 族。
(2)写出钛铁矿在高温下与焦炭经氯化得到四氯化钛的化学方程式______________ 。
(3)制备TiO2的方法之一是利用TiCl4水解生成TiO2·x H2O,再经焙烧制得。水解时需加入大量的水并加热,请结合化学方程式和必要的文字说明原因:
(4)反应后得到Mg、MgCl2、Ti的混合物,可采用蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于____________ ℃即可。
(5)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。滴定分析时,称取TiO2(摩尔质量为M g/mol)试样w g,消耗c mol/L NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数为___________________ 。(用代数式表示)
(6)由CO和H2合成甲醇的方程式是:CO(g)+2H2(g) CH3OH(g)。若不考虑生产过程中物质的任何损失,上述产业链中每合成6mol甲醇,至少需额外补充H2
CH3OH(g)。若不考虑生产过程中物质的任何损失,上述产业链中每合成6mol甲醇,至少需额外补充H2_____________ mol。

请回答下列问题:
(1)Fe位于元素周期表中第
(2)写出钛铁矿在高温下与焦炭经氯化得到四氯化钛的化学方程式
(3)制备TiO2的方法之一是利用TiCl4水解生成TiO2·x H2O,再经焙烧制得。水解时需加入大量的水并加热,请结合化学方程式和必要的文字说明原因:
(4)反应后得到Mg、MgCl2、Ti的混合物,可采用蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
(5)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。滴定分析时,称取TiO2(摩尔质量为M g/mol)试样w g,消耗c mol/L NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数为
(6)由CO和H2合成甲醇的方程式是:CO(g)+2H2(g)
 CH3OH(g)。若不考虑生产过程中物质的任何损失,上述产业链中每合成6mol甲醇,至少需额外补充H2
CH3OH(g)。若不考虑生产过程中物质的任何损失,上述产业链中每合成6mol甲醇,至少需额外补充H2
您最近一年使用:0次
5 . [化学——选修3:物质结构与性质]
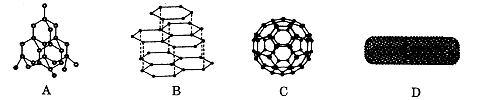
下图分别是金刚石、石墨、足球烯和碳纳米管的结构示意图。图中小黑点或小黑圈均代表碳原子。
(1)四种物质互称为_________ 。写出碳原子的基态电子排布图_________________ 。
(2)试比较:第一电离能I1(C)、I1(N)、I1(O)由大到小的顺序为_____________ 。
(3)石墨中存在的作用力有________ 。
A. 共价键 B. 金属键 C. 氢键
D. 配位键 E. 分子间作用力
石墨中碳原子采取的杂化方式是_____________ 。
(4)C的熔沸点比A_____________ (填“高”或“低”)原因是__________ 。
(5)金刚石晶胞结构如下图所示,若金刚石的密度为ρ g·cm-3,试计算碳原子的半径为__________ pm(用含ρ式子表示,不必化简)。
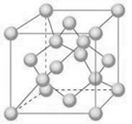
下图分别是金刚石、石墨、足球烯和碳纳米管的结构示意图。图中小黑点或小黑圈均代表碳原子。

(1)四种物质互称为
(2)试比较:第一电离能I1(C)、I1(N)、I1(O)由大到小的顺序为
(3)石墨中存在的作用力有
A. 共价键 B. 金属键 C. 氢键
D. 配位键 E. 分子间作用力
石墨中碳原子采取的杂化方式是
(4)C的熔沸点比A
(5)金刚石晶胞结构如下图所示,若金刚石的密度为ρ g·cm-3,试计算碳原子的半径为

您最近一年使用:0次
6 . 铜是与人类关系非常密切的常见金属。
Ⅰ.已知常温下,在溶液中Cu2+稳定,Cu+易在酸性条件下发生反应:2Cu+ = Cu2++ Cu。
(1)CuH中H元素化合价为_________________ 。
(2)目前制备纳米级Cu2O的一种方法:在氢氧化铜悬浊液中滴入N2H4·H2O水溶液,充分反应后即可得到Cu2O,同时产生无色无味的气体。上述制备过程中总反应的化学方程式为________________ 。
(3)一定条件下,在CuSO4中加入NH4H反应生成氢化亚铜(CuH)。将CuH溶解在足量稀硫酸中,当产生6.72 L H2(标准状况下)时,参加反应的硫酸的物质的量为_______________ 。
Ⅱ.孔雀石呈绿色,是一种名贵的宝石。其主要成分是xCu(OH)2·yCuCO3。某兴趣小组为探究孔雀石组成,利用下图所示的装置(夹持仪器省略)进行实验:
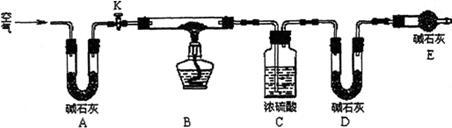
步骤1:检查装置的气密性,将研细的样品置于硬质玻璃管中。
步骤2:称量相关装置的质量,打开活塞K,鼓入空气,一段时间后关闭。
步骤3:加热装置B直至装置C中无气泡产生。
步骤4:_________________________。
步骤5:冷却至室温,称量相关装置的质量。
(1)请补充步骤4操作内容:_____________________________ 。
(2)若无装置E,则实验测定的x/y的值将__________ (选填“偏大”、“偏小”或“无影响”)。
(3)某同学在实验过程中采集了如下数据:
为测定x/y的值,你认为可以选用上述所采集数据中的_______________ (写出所有组合的字母代号)任一组即可进行计算,并根据你的计算结果,写出孔雀石组成的化学式____________ 。
Ⅰ.已知常温下,在溶液中Cu2+稳定,Cu+易在酸性条件下发生反应:2Cu+ = Cu2++ Cu。
(1)CuH中H元素化合价为
(2)目前制备纳米级Cu2O的一种方法:在氢氧化铜悬浊液中滴入N2H4·H2O水溶液,充分反应后即可得到Cu2O,同时产生无色无味的气体。上述制备过程中总反应的化学方程式为
(3)一定条件下,在CuSO4中加入NH4H反应生成氢化亚铜(CuH)。将CuH溶解在足量稀硫酸中,当产生6.72 L H2(标准状况下)时,参加反应的硫酸的物质的量为
Ⅱ.孔雀石呈绿色,是一种名贵的宝石。其主要成分是xCu(OH)2·yCuCO3。某兴趣小组为探究孔雀石组成,利用下图所示的装置(夹持仪器省略)进行实验:

步骤1:检查装置的气密性,将研细的样品置于硬质玻璃管中。
步骤2:称量相关装置的质量,打开活塞K,鼓入空气,一段时间后关闭。
步骤3:加热装置B直至装置C中无气泡产生。
步骤4:_________________________。
步骤5:冷却至室温,称量相关装置的质量。
(1)请补充步骤4操作内容:
(2)若无装置E,则实验测定的x/y的值将
(3)某同学在实验过程中采集了如下数据:
| A.反应前硬质玻璃管与样品的质量163.8g |
| B.反应后硬质玻璃管中残留固体质量20g |
| C.装置C实验后增重2.25g |
| D.装置D实验后增重5.5g |
为测定x/y的值,你认为可以选用上述所采集数据中的
您最近一年使用:0次
7 . 某氯的氧化物A常温下为气态,测得该气体对空气的相对密度为3.0,A溶于水可得只含单一溶质B的弱酸性溶液,B溶液在放置过程中酸性会增强。常温下,气体A与NH3反应生成离子晶体C、气体单质D和常见液体E,D为空气中含量最多的物质。气体A可用氯气与潮湿的Na2CO3反应制得,同时生成两种钠盐。请回答下列问题:
(1)气体A的化学式为____________ 。
(2)用化学方程式表示B溶液酸性增强的原因_________________________ 。
(3)气体A与NH3反应的化学方程式为___________ ,该反应体现气体A具有_________ 性。
(4)试写出制取气体A的化学方程式为__________________________ 。
(5)设计实验探究离子晶体C中阳离子的成分_______________________________ 。
(1)气体A的化学式为
(2)用化学方程式表示B溶液酸性增强的原因
(3)气体A与NH3反应的化学方程式为
(4)试写出制取气体A的化学方程式为
(5)设计实验探究离子晶体C中阳离子的成分
您最近一年使用:0次



