解题方法
1 . 铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
Ⅰ.
(1)生铁含有C、Si、Mn、S、P等元素,其中属于金属元素的除Fe外,还有_____ 元素。
(2)铁元素有三种常见的氧化物,分别是FeO、 、
、 。其中具有磁性的是
。其中具有磁性的是_____ ,可作红色颜料的是_____ 。
(3)某补铁口服液中含有 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为_____ 色,则说明其已变质。向该口服液中加入维生素C可防止其被氧化变质,此过程中利用了维生素C的_____ 性。
(4) 可作为铜电路板的腐蚀液,其反应原理为Cu与
可作为铜电路板的腐蚀液,其反应原理为Cu与 溶液反应生成
溶液反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_____ 。向反应后的溶液中加入_____ ,可回收Cu,并得到 溶液。
溶液。
Ⅱ.高铁酸钾( )是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
)是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
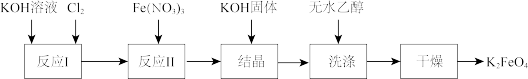
(5)下列说法错误的是_____。
(6)用电解饱和食盐水获得原料氯气的过程中有2mol电子发生转移,试计算理论上最多可制得氯气的体积(标准状况)是_____ L。
Ⅰ.
(1)生铁含有C、Si、Mn、S、P等元素,其中属于金属元素的除Fe外,还有
(2)铁元素有三种常见的氧化物,分别是FeO、
 、
、 。其中具有磁性的是
。其中具有磁性的是(3)某补铁口服液中含有
 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为(4)
 可作为铜电路板的腐蚀液,其反应原理为Cu与
可作为铜电路板的腐蚀液,其反应原理为Cu与 溶液反应生成
溶液反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为 溶液。
溶液。Ⅱ.高铁酸钾(
 )是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
)是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
(5)下列说法错误的是_____。
A. 中铁元素的化合价为+6价 中铁元素的化合价为+6价 |
| B.用无水乙醇洗涤可以减少产品的损耗 |
C.反应Ⅱ中的氧化剂是 |
| D.高铁酸根离子具有强氧化性,能杀菌消毒 |
您最近一年使用:0次
解题方法
2 . Ⅰ.氯气及氯的化合物的“价-类”二维图体现了化学变化之美。
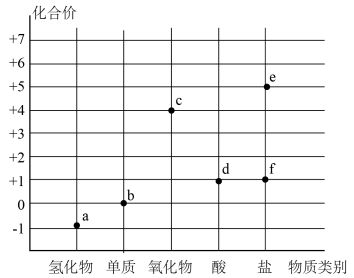
(1)f(84消毒液的主要成分)可用于环境杀菌消毒,f的化学式是_____ 。
(2)不同价态的氯元素可以相互转化,请写出反应前后存在3种价态氯元素的化学方程式_____ 。
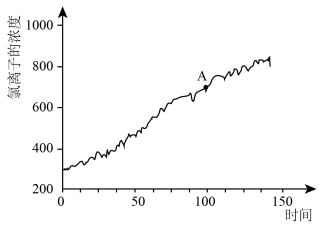
(3)将氯离子传感器插入新制b的水溶液广口瓶中,与数据采集器、计算机连接,用强光照射瓶中溶液,采集数据所得图像如图所示。A点溶液发生分解反应的离子方程式为_____ 。
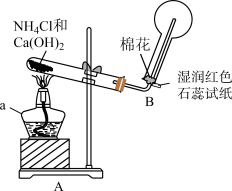
Ⅱ.氨是一种重要的化工产品,也是重要的化工原料。某化学小组在实验室制备氨并完成相关性质实验。
(4)实验一:用如图所示装置制备并收集 。仪器a的名称为
。仪器a的名称为_____ ,装置A中产生 的化学方程式为
的化学方程式为_____ ,装置B中用圆底烧瓶收集 的方法为
的方法为_____ (填“向上排空气法”或“向下排空气法”),当湿润红色石蕊试纸颜色变为_____ 色,表示已经收集满 。
。

(1)f(84消毒液的主要成分)可用于环境杀菌消毒,f的化学式是
(2)不同价态的氯元素可以相互转化,请写出反应前后存在3种价态氯元素的化学方程式
(3)将氯离子传感器插入新制b的水溶液广口瓶中,与数据采集器、计算机连接,用强光照射瓶中溶液,采集数据所得图像如图所示。A点溶液发生分解反应的离子方程式为

Ⅱ.氨是一种重要的化工产品,也是重要的化工原料。某化学小组在实验室制备氨并完成相关性质实验。
(4)实验一:用如图所示装置制备并收集
 。仪器a的名称为
。仪器a的名称为 的化学方程式为
的化学方程式为 的方法为
的方法为 。
。
您最近一年使用:0次
3 . 如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题。
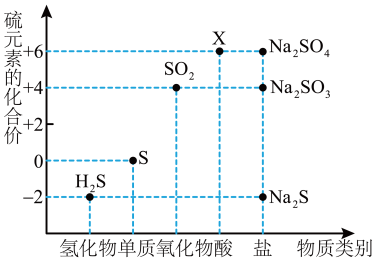
(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的___________ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有___________ (填化学式)。
(3)将 与
与 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为___________ 。
(4)配平下列反应_________________ 。
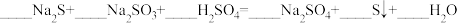
(5)一定条件下,在 密闭容器中发生反应:
密闭容器中发生反应: ,开始时加入
,开始时加入 、
、 、
、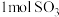 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 ,用
,用 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为___________ ,在 末
末 的浓度为
的浓度为___________ 。若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”)
①升高温度,化学反应速率___________ ;
②再充入 ,化学反应速率
,化学反应速率___________ ;
③将容器体积变为 ,化学反应速率
,化学反应速率___________ 。

(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有
(3)将
 与
与 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为(4)配平下列反应
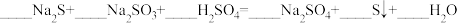
(5)一定条件下,在
 密闭容器中发生反应:
密闭容器中发生反应: ,开始时加入
,开始时加入 、
、 、
、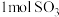 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 ,用
,用 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为 末
末 的浓度为
的浓度为①升高温度,化学反应速率
②再充入
 ,化学反应速率
,化学反应速率③将容器体积变为
 ,化学反应速率
,化学反应速率
您最近一年使用:0次
解题方法
4 . 下表列出了①~⑨九种元素在周期表中的位置。
请按要求回答下列问题:
(1)元素⑦的原子结构示意图:__________________ ,元素⑤与⑧组成的化合物的电子式:____________ 。
(2)元素⑤~⑧中原子半径最大的是____________ (填元素符号)。
(3)元素①~⑨中化学性质最不活泼的是____________ (填元素符号)。
(4)元素③的氢化物,分子的空间构型呈____________ 形。
(5)元素⑤和⑥的最高价氧化物对应的水化物分别为X和Y,其中属于两性氢氧化物的是______ (填化学式),X和Y反应的离子方程式:__________________ 。
(6)元素①与②所形成的最简单有机物分子中含有____________ 个电子。元素①与②所形成的最简单烯烃为Z,写出Z与水在催化剂、加热、加压条件下反应的化学方程式:___________ ,该反应生成物的官能团是_____________ (填名称),反应类型为____________ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素⑦的原子结构示意图:
(2)元素⑤~⑧中原子半径最大的是
(3)元素①~⑨中化学性质最不活泼的是
(4)元素③的氢化物,分子的空间构型呈
(5)元素⑤和⑥的最高价氧化物对应的水化物分别为X和Y,其中属于两性氢氧化物的是
(6)元素①与②所形成的最简单有机物分子中含有
您最近一年使用:0次
解题方法
5 . 浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物。某同学设计了如下图所示的实验。请据此回答下列问题。
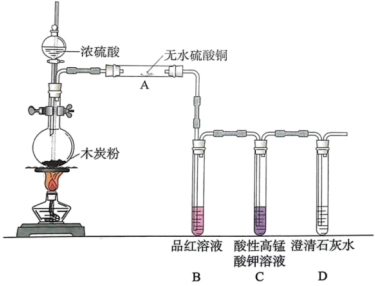
(1)A中的实验现象是_______ ,证明产物中有_______ 。
(2)B中的实验现象是_______ 。
(3)装置C的作用是_______ 。
(4)浓硫酸与木炭在加热条件下发生化学反应的化学方程式_______ 。

(1)A中的实验现象是
(2)B中的实验现象是
(3)装置C的作用是
(4)浓硫酸与木炭在加热条件下发生化学反应的化学方程式
您最近一年使用:0次
名校
6 . 对印刷电路板制作过程中(2FeCl3+Cu=2FeCl2+CuCl2)产生废液X进行回收处理,流程如图所示。

(1)写出FeCl2溶液通入过量氯气发生反应的离子方程式:____ 。
(2)实验室中进行操作①②时,需用到的玻璃仪器有烧杯、漏斗和____ 。
(3)若向溶液A中、溶液B中分别加入少量铁粉,其中一溶液中铁粉有减少,请写出相应的化学方程式:____ 。
(4)下列物质中,在一定条件下能与铁反应,且铁元素化合价全部 变为+3价的是____ 。
(5)1molFeCl3与Cu完全反应,转移电子数约为____ 。

(1)写出FeCl2溶液通入过量氯气发生反应的离子方程式:
(2)实验室中进行操作①②时,需用到的玻璃仪器有烧杯、漏斗和
(3)若向溶液A中、溶液B中分别加入少量铁粉,其中一溶液中铁粉有减少,请写出相应的化学方程式:
(4)下列物质中,在一定条件下能与铁反应,且铁元素化合价
| A.S | B.H2O | C.稀硫酸 | D.氯气 |
您最近一年使用:0次
7 . 下表列出了①~⑩十种元素在周期表中的位置:
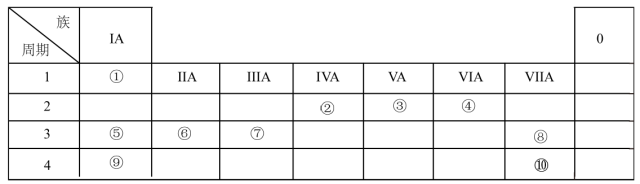
请按要求回答下列问题:
(1)元素⑤的原子结构示意图为___ ;元素②的最高价氧化物的电子式是___ 。
(2)⑤、⑥、⑨三种元素原子半径由大到小的顺序是___ (填元素符号);这三种元素最高价氧化物对应水化物中碱性最强的是___ (填化学式)。
(3)③、④元素的简单氢化物的稳定性较弱的是___ (填化学式)。
(4)①、②、④三种元素形成的有机物的分子结构模型如图所示,写出该有机物的结构简式:___ ;①与②所形成的最简单的烯烃与溴的四氯化碳溶液反应的化学方程式:___ 。

(5)元素⑦的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式:___ 。
(6)写出元素⑨的单质与水反应的化学方程式:___ 。
(7)请从原子结构的角度解释,元素⑧非金属性比元素⑩强的原因:___ 。

请按要求回答下列问题:
(1)元素⑤的原子结构示意图为
(2)⑤、⑥、⑨三种元素原子半径由大到小的顺序是
(3)③、④元素的简单氢化物的稳定性较弱的是
(4)①、②、④三种元素形成的有机物的分子结构模型如图所示,写出该有机物的结构简式:

(5)元素⑦的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式:
(6)写出元素⑨的单质与水反应的化学方程式:
(7)请从原子结构的角度解释,元素⑧非金属性比元素⑩强的原因:
您最近一年使用:0次
2020-07-11更新
|
355次组卷
|
2卷引用:天津市南开区2020届高中学业水平合格性考试模拟试卷化学试题
8 . 亚硝酰氯(ClNO)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+Cl2(g) 2ClNO(g)。
2ClNO(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:① 2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s)
NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g) 2ClNO(g) K3,则K1、K2、K3之间的关系为K3=
2ClNO(g) K3,则K1、K2、K3之间的关系为K3=_______________ (用K1和K2表示);
(2)已知几种化学键的键能数据如下表:(亚硝酰氯的结构为Cl—N==O)
则2NO(g)+Cl2(g) 2ClNO(g)的反应的 △H和a的关系为 △H =
2ClNO(g)的反应的 △H和a的关系为 △H = ___ kJ·mol-1。
(3)300℃时,2NO(g)+Cl2 (g) 2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:
n = ___ ;k = ____ 。
(4)若向绝热恒容密闭容器中充入物质的量之比为2 : 1的NO和Cl2进行反应2NO(g)+Cl2(g) 2ClNO(g),能判断反应已达到化学平衡状态的是
2ClNO(g),能判断反应已达到化学平衡状态的是__ (填标号)。
a.容器中的压强不变 b.2v正(NO) = v逆(Cl2)c.气体的平均相对分子质量保持不变 d.该反应平衡常数保持不变e.NO和Cl2的体积比保持不变
(5)25℃时,向体积为2 L且带气压计的恒容密闭容器中通入0.08 mol NO和0.04 mol Cl2发生反应:2NO(g)+Cl2 (g) 2ClNO(g)△H。
2ClNO(g)△H。
①若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图甲曲线a所示,则 △H__ (填“>”“<”或“不确定”)0;若其他条件相同,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图甲曲线b所示,则改变的条件是______ 。
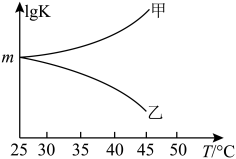
②图是甲、乙同学描绘上述反应平衡常数的对数值(lg K)与温度的变化关系,其中正确的曲线是____ (填“甲”或“乙”),m值为_____ 。
 2ClNO(g)。
2ClNO(g)。(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:① 2NO2(g)+NaCl(s)
 NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s)
NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g) 2ClNO(g) K3,则K1、K2、K3之间的关系为K3=
2ClNO(g) K3,则K1、K2、K3之间的关系为K3=(2)已知几种化学键的键能数据如下表:(亚硝酰氯的结构为Cl—N==O)
| 化学键 | N≡O | Cl-Cl | Cl-N | N==O |
| 键能/(kJ·mol-1) | 630 | 243 | a | 607 |
 2ClNO(g)的反应的 △H和a的关系为 △H =
2ClNO(g)的反应的 △H和a的关系为 △H = (3)300℃时,2NO(g)+Cl2 (g)
 2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:| 序号 | c(ClNO)/(mol·L-1) | v/(mol·L-1·s-l) |
| ① | 0. 30 | 3. 60×10-9 |
| ② | 0. 60 | 1. 44×10-8 |
| ③ | 0. 90 | 3. 24×10-8 |
(4)若向绝热恒容密闭容器中充入物质的量之比为2 : 1的NO和Cl2进行反应2NO(g)+Cl2(g)
 2ClNO(g),能判断反应已达到化学平衡状态的是
2ClNO(g),能判断反应已达到化学平衡状态的是a.容器中的压强不变 b.2v正(NO) = v逆(Cl2)c.气体的平均相对分子质量保持不变 d.该反应平衡常数保持不变e.NO和Cl2的体积比保持不变
(5)25℃时,向体积为2 L且带气压计的恒容密闭容器中通入0.08 mol NO和0.04 mol Cl2发生反应:2NO(g)+Cl2 (g)
 2ClNO(g)△H。
2ClNO(g)△H。①若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图甲曲线a所示,则 △H
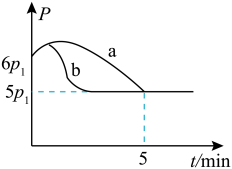
②图是甲、乙同学描绘上述反应平衡常数的对数值(lg K)与温度的变化关系,其中正确的曲线是
您最近一年使用:0次
2019-12-29更新
|
454次组卷
|
3卷引用:天津市河东区2020届高三学业水平等级性考试模拟测试化学试题
名校
9 . 迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图所示。

该物质中含有的所有官能团名称有______________________________________________

该物质中含有的所有官能团名称有
您最近一年使用:0次
名校
10 . 某研究性学习小组要鉴定和研究苯甲酸的结构利性质,现有苯甲酸的粗品,实验步骤如下
(1)定性分析:
对苯甲酸进行分离提纯。此分离提纯的方法为:_____________ 。
(2)化学组成分析:
①定性分析(证明苯甲酸中含有C、H元素): 取一定量的苯甲酸,在密闭容器中与氧气充分燃烧,然后将燃烧产物依次通入_______ 和__________ 。
②定量分析(确定苯甲酸中C、H 元素的质量分数):取一定量的苯甲酸,在密闭容器中与氧气充分燃烧,然后将燃烧产物依次通入_________ 和________ 。
③通过计算证明苯甲酸中是否有氧元素,并确定其质量分数。
④测定苯甲酸的相对分子质量。
(3)波谱分析法鉴定分子结构:
①通过_____ 可获得苯甲酸分子中含有何种化学键或官能团的信息(写方法名称)。
②从核磁共振氢谱上可判定苯甲酸分子中有_____ 种不同类型的氢原子及它们的数目比为____ 。
(1)定性分析:
对苯甲酸进行分离提纯。此分离提纯的方法为:
(2)化学组成分析:
①定性分析(证明苯甲酸中含有C、H元素): 取一定量的苯甲酸,在密闭容器中与氧气充分燃烧,然后将燃烧产物依次通入
②定量分析(确定苯甲酸中C、H 元素的质量分数):取一定量的苯甲酸,在密闭容器中与氧气充分燃烧,然后将燃烧产物依次通入
③通过计算证明苯甲酸中是否有氧元素,并确定其质量分数。
④测定苯甲酸的相对分子质量。
(3)波谱分析法鉴定分子结构:
①通过
②从核磁共振氢谱上可判定苯甲酸分子中有
您最近一年使用:0次
2017-03-26更新
|
440次组卷
|
3卷引用:天津市静海县第一中学2016-2017学年高二下学期小样提高卷化学(理)试题(3.19)



