名校
解题方法
1 . 回答下列问题。
Ⅰ.写出下列反应的离子方程式
(1)醋酸与氢氧化钠溶液反应:___________ 。
(2)二氧化碳通入过量澄清石灰水中:___________ 。
(3)FeCl3腐蚀铜箔:___________ 。
(4)NH4HCO3与足量稀NaOH反应:___________ 。
Ⅱ.在标准状况下,有物质①4gH2,②33.6LCH4,③1molH2O,④ 个O2。
个O2。
(5)上述物质中,含分子数最多的是(填序号,下同)___________ ,含原子数最少的是___________ ,质量最大的是___________ 。密度由大到小的顺序为___________ 。
Ⅰ.写出下列反应的离子方程式
(1)醋酸与氢氧化钠溶液反应:
(2)二氧化碳通入过量澄清石灰水中:
(3)FeCl3腐蚀铜箔:
(4)NH4HCO3与足量稀NaOH反应:
Ⅱ.在标准状况下,有物质①4gH2,②33.6LCH4,③1molH2O,④
 个O2。
个O2。(5)上述物质中,含分子数最多的是(填序号,下同)
您最近一年使用:0次
名校
2 . 使用相关化学用语回答下列问题:
(1)用化学方程式表示金属钠的工业制法:___________ ;
(2)用化学方程式表示高炉炼铁的反应原理:___________ ;
(3)实验室使用 和浓盐酸制备氯气的反应离子方程式:
和浓盐酸制备氯气的反应离子方程式:___________ ;
(4)通过氯碱工业制备氯气的离子方程式:___________ ;
(5)用化学方程式表示氨气实验室制法的反应原理:___________ ;
(6)实验室制乙烯的化学反应方程式:___________ ;
(7)实验室制乙炔的化学反应方程式:___________ ;
(8)泡沫灭火器反应原理的离子方程式:___________ 。
(1)用化学方程式表示金属钠的工业制法:
(2)用化学方程式表示高炉炼铁的反应原理:
(3)实验室使用
 和浓盐酸制备氯气的反应离子方程式:
和浓盐酸制备氯气的反应离子方程式:(4)通过氯碱工业制备氯气的离子方程式:
(5)用化学方程式表示氨气实验室制法的反应原理:
(6)实验室制乙烯的化学反应方程式:
(7)实验室制乙炔的化学反应方程式:
(8)泡沫灭火器反应原理的离子方程式:
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)下列为用氯化铁固体制备氢氧化铁胶体的相关实验,可以达到实验目的的是___________。
(2)磷的一种化合物叫亚磷酸(H3PO3)。已知:
Ⅰ.0.1mol/LH3PO3溶液的pH=1.7;
Ⅱ.H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ.H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。
①关于H3PO3的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是___________ 。
A.②④⑥ B.②③⑥ C.①④⑤ D.②③⑤
②写出H3PO3与过量NaOH溶液反应的离子方程式___________ 。
(3)H3PO2(次磷酸)是一元中强酸,H3PO2及NaH2PO2均可将溶液中的 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。
①NaH2PO2属于___________ (填“正盐”“酸式盐”或“碱式盐”)。
②利用H3PO2化学镀银,反应中氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为___________ (写化学式)。
(1)下列为用氯化铁固体制备氢氧化铁胶体的相关实验,可以达到实验目的的是___________。
| A | B | C | D |
| 配制FeCl3溶液制备 | Fe(OH)3胶体 | 观察胶体的丁达尔效应 | 分离Fe(OH)3胶体与溶液 |
 |  |  | 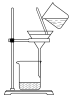 |
| A.A | B.B | C.C | D.D |
Ⅰ.0.1mol/LH3PO3溶液的pH=1.7;
Ⅱ.H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ.H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。
①关于H3PO3的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是
A.②④⑥ B.②③⑥ C.①④⑤ D.②③⑤
②写出H3PO3与过量NaOH溶液反应的离子方程式
(3)H3PO2(次磷酸)是一元中强酸,H3PO2及NaH2PO2均可将溶液中的
 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。①NaH2PO2属于
②利用H3PO2化学镀银,反应中氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为
您最近一年使用:0次
名校
4 . 回答下列问题
(1)铝是地壳中含量最多的金属元素,画出铝原子结构示意图_______ 。在酒精灯的火焰上灼烧铝片,可观察到铝熔化但不滴落,说明铝的熔点比较_______ (高、低),外层氧化铝薄膜是_______ (疏松、致密)的。
(2)根据反应 ,回答下列问题:
,回答下列问题:
①画双线桥,请标出变价元素化合价、电子得失及转移数目_______ 。
②还原剂是_______ ,被_______ (氧化、还原)。
③当有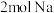 反应时,转移
反应时,转移_______  电子,生成
电子,生成
_______ L(标准状态下)。
(1)铝是地壳中含量最多的金属元素,画出铝原子结构示意图
(2)根据反应
 ,回答下列问题:
,回答下列问题:①画双线桥,请标出变价元素化合价、电子得失及转移数目
②还原剂是
③当有
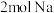 反应时,转移
反应时,转移 电子,生成
电子,生成
您最近一年使用:0次
5 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)我们学习过很多颜色的化学物质,写出下列物质的颜色:
过氧化钠固体___________ ,氢氧化铁胶体___________ 。
(2)写出下列物质的电离方程式:
Al2(SO4)3___________ ,Ba(OH)2___________ 。
(3)通过学习,我们掌握了胶体的知识,请完成下列问题:
鉴别胶体和溶液的方法(只需写出方法名称,不用展开写)___________ ,胶体和溶液的本质区别是___________ 。
(4)某同学写出以下三个化学方程式(未配平)
①NO+HNO3―→N2O3+H2O
②NH3+NO―→HNO2+H2O
③N2O4+H2O―→HNO3+HNO2
其中你认为一定不可能实现的是___________ 。
(5)红热的木炭与浓硝酸反应的化学方程式为:C+4HNO3(浓) CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为
CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为___________ ;如果产生标准状况下22.4LCO2,则转移的电子的物质的量为___________ mol。
(6)有下列6种物质:Na2SO4、Na2SO3、K2SO4、I2、H2SO4、KIO3组成一个氧化还原反应,请回答下列问题:
i.将除Na2SO3的5种物质分别填入下面对应的横线上,组成化学方程式并配平:_____+Na2SO3+_____—_____+_____+_____+H2O,___________ 。
ii.反应物中发生氧化反应的物质是___________ (填化学式),被还原的元素是___________ ;
iii.反应中1mol氧化剂___________ (填“得到”或“失去”)___________ mol电子。
(1)我们学习过很多颜色的化学物质,写出下列物质的颜色:
过氧化钠固体
(2)写出下列物质的电离方程式:
Al2(SO4)3
(3)通过学习,我们掌握了胶体的知识,请完成下列问题:
鉴别胶体和溶液的方法(只需写出方法名称,不用展开写)
(4)某同学写出以下三个化学方程式(未配平)
①NO+HNO3―→N2O3+H2O
②NH3+NO―→HNO2+H2O
③N2O4+H2O―→HNO3+HNO2
其中你认为一定不可能实现的是
(5)红热的木炭与浓硝酸反应的化学方程式为:C+4HNO3(浓)
 CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为
CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为(6)有下列6种物质:Na2SO4、Na2SO3、K2SO4、I2、H2SO4、KIO3组成一个氧化还原反应,请回答下列问题:
i.将除Na2SO3的5种物质分别填入下面对应的横线上,组成化学方程式并配平:_____+Na2SO3+_____—_____+_____+_____+H2O,
ii.反应物中发生氧化反应的物质是
iii.反应中1mol氧化剂
您最近一年使用:0次
2021-12-03更新
|
268次组卷
|
2卷引用:天津市咸水沽第一中学2022-2023学年高三上学期学开学考试化学试题
名校
解题方法
6 . 1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一、元素周期表与元素周期律在化学学习研究中有很重要的作用。
(1)下表是元素周期表的一部分
i.元素④的过氧化物的电子式为___________ ,其最高价氧化物对应的水化物含有的化学键类型为___________ ,⑩元素最高价氧化物对应的水化物的化学式是___________ 。
ii.元素①、②、③的简单氢化物的稳定性最强的是___________ (用化学式表示,下同),②、⑧简单氢化物熔点高的是___________ ,④、⑤最高价氧化物的水化物碱性更强的是___________ ,④、⑤、⑧、⑨的简单离子半径由大到小的顺序(用离子符号表示)___________ 。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置___________ 。
ii.铷单质性质活泼写出在点燃条件下它与氯气反应的化学方程式:___________ ;铷单质易与水反应,反应的离子方程式为___________ ,实验表明铷与水反应比钠与水反应___________ (填“剧烈”或“缓慢”);反应过程中铷在水___________ (填“面”或“底”)与水反应。同主族元素的同类化合物的化学性质相似,写出过氧化铷与 反应的化学方程式:
反应的化学方程式:___________ 。
(1)下表是元素周期表的一部分
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
i.元素④的过氧化物的电子式为
ii.元素①、②、③的简单氢化物的稳定性最强的是
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置
ii.铷单质性质活泼写出在点燃条件下它与氯气反应的化学方程式:
 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
名校
7 . 由C、H、O三种元素组成的链状有机化合物X,只含有羟基和羧基两种官能团。
(1)若化合物X的分子式为C3H6O3。X与氧气在铜丝催化加热的条件下得到产物Y,取少量Y加入到足量新制Cu(OH)2悬浊液中并加热,无现象。
①请写出X生成Y的化学反应方程式______ 。
②该化合物X在浓硫酸加热的条件下生成的六元环化合物的结构简式是______ 。
(2)若化合物X的羟基数目大于羧基数目。称取2.04g纯净的X,与足量金属钠充分反应,生成672mL氢气(标准状况)。请确定摩尔质量最小的X分子中羟基、羧基数目及该X的相对分子质量_____ 。
(1)若化合物X的分子式为C3H6O3。X与氧气在铜丝催化加热的条件下得到产物Y,取少量Y加入到足量新制Cu(OH)2悬浊液中并加热,无现象。
①请写出X生成Y的化学反应方程式
②该化合物X在浓硫酸加热的条件下生成的六元环化合物的结构简式是
(2)若化合物X的羟基数目大于羧基数目。称取2.04g纯净的X,与足量金属钠充分反应,生成672mL氢气(标准状况)。请确定摩尔质量最小的X分子中羟基、羧基数目及该X的相对分子质量
您最近一年使用:0次
名校
8 . 原子结构与性质
(1)元素As与N同族。As的氢化物沸点比NH3的___ (填“高”或“低”),其判断理由是______ 。
(2)铜原子在基态时的价电子排布式为______ 。
(3)Fe是人体需要补充的元素之一,试写出Fe2+的核外电子排布式:_____ 。与Al同一周期的Na、Mg元素也是人体所需元素,Na、Mg、Al基态原子第一电离能的大小关系____ 。某同学所画基态镁原子的核外电子排布图如图 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了______ 。
(4)K元素处于元素周期表的____ 区,其基态原子中,核外电子占据的电子云轮廓图为球形的能级有____ 个。
(1)元素As与N同族。As的氢化物沸点比NH3的
(2)铜原子在基态时的价电子排布式为
(3)Fe是人体需要补充的元素之一,试写出Fe2+的核外电子排布式:
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(4)K元素处于元素周期表的
您最近一年使用:0次
2019-09-27更新
|
205次组卷
|
2卷引用:天津市六校(天津中学、南开中学、实验中学等)2020届高三上学期期初检测化学试题
名校
9 . 有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。请根据以上信息回答下列问题:
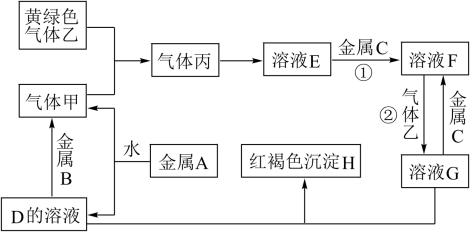
(1)写出下列物质的化学式:乙_________ 、H__________ ;
(2)写出反应②的离子方程式______________________ ;
(3)写出金属A与水反应的离子方程式___________________________ ;
(4)写出金属B与D的溶液反应的离子方程式____________________ ;
(5)F与D溶液反应后的产物在空气中转化为H的化学方程式___________ ;现象为_________________ 。

(1)写出下列物质的化学式:乙
(2)写出反应②的离子方程式
(3)写出金属A与水反应的离子方程式
(4)写出金属B与D的溶液反应的离子方程式
(5)F与D溶液反应后的产物在空气中转化为H的化学方程式
您最近一年使用:0次
2019-02-15更新
|
389次组卷
|
2卷引用:天津市咸水沽第一中学2022-2023学年高三上学期学开学考试化学试题
名校
解题方法
10 . 现有下列几种物质:蔗糖、氯化钡固体、干冰、硫酸钡、纯碱、铁、盐酸、硝酸银溶液,按要求回答问题:
(1)难溶于水的电解质的是_______ 。
(2)写出纯碱在水中的电离方程式________________________ 。
(3)将足量的干冰升华后所得的气体通入烧碱溶液中,发生反应的离子方程式为____________ 。
(4)a、b、c、d是Na2CO3、BaCl2、盐酸、AgNO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
①b是________ (用化学式填写),
②写出 a+c 反应的离子方程式________________________ 。
(1)难溶于水的电解质的是
(2)写出纯碱在水中的电离方程式
(3)将足量的干冰升华后所得的气体通入烧碱溶液中,发生反应的离子方程式为
(4)a、b、c、d是Na2CO3、BaCl2、盐酸、AgNO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |
①b是
②写出 a+c 反应的离子方程式
您最近一年使用:0次
2018-12-05更新
|
121次组卷
|
2卷引用:天津市咸水沽第一中学2022-2023学年高三上学期学开学考试化学试题



