18. 乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂和防腐剂、乙酰苯胺的制备原理为:
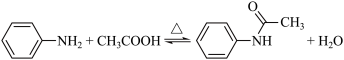
实验参数
| 名称 | 相对分子质量 | 性状 | 密度(g/mL) | 沸点(℃) | 溶解性 |
| 苯胺 | | 无色油状液体 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚 |
| 乙酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
乙酰
苯胺 | 135 | 白色晶体 | 1.22 | 304.0 | 微溶于冷水
可溶于热水 | 易溶于乙醇、乙醚 |

实验步骤:
步骤1:向圆底烧瓶中加入无水苯胺9.3mL、冰醋酸18.4mL、锌粉0.1g和少量沸石,安装好仪器后,对圆底烧瓶均匀加热,使反应液在微沸状态下回流,调节加热温度,使温度计温度控制在105℃左右;反应约60
∼80min,反应生成的水及少量醋酸被蒸出,当反应基本完成时,停止加热。
步骤2:在搅拌下,趁热将蒸馏烧瓶中的液体以细流状倒入盛有冰水的100mL烧杯中,快速搅拌,乙酰苯胺结晶析出,烧杯内试剂冷却至室温后,进行抽滤、洗涤、干燥,可得到乙酰苯胺粗品。
步骤3:将乙酰苯胺粗品进行重结晶,待结晶完全后抽滤,尽量压干滤饼。将产品置于干净的表面皿中晾干,称重,计算产率。
注:a.刺型分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离。
b.苯胺易被氧化。
请回答下列问题:
(1)步骤1中所选圆底烧瓶的最佳规格是
_____。
a.25mL
b.50mL
c.150mL
d.200mL
(2)实验中加入锌粉的目的是
_____。
(3)从化学平衡的角度分析,控制温度计的温度在105℃左右的原因是
_____。
(4)通过
_____可判断反应基本完成。
(5)步骤1加热可用
_____(填“水浴”或“油浴”)。
(6)洗涤乙酰苯胺粗品最合适的方法是
_____(填字母)。
A.用少量冷水洗
B.用少量热水洗
C.先用冷水洗,再用热水洗
D.用酒精洗
(7)步骤2得到的粗品中因含有某些杂质而颜色较深,步骤3重结晶的操作是:将粗品用热水溶解,加入活性炭0.1g,煮沸进行脱色,
_____,再将滤液冷却结晶。
(8)该实验最终得到产品9.1g,则乙酰苯胺的产率是
_____(小数点后保留两位数字。)