21. 实验室用下图所示装置制备FeSO
4,该物质应用广泛。
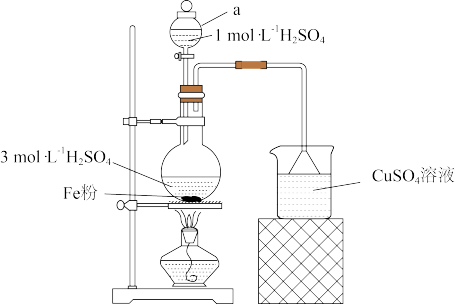
已知:硫酸亚铁铵晶体在空气中不易被氧化,易溶于水,不溶于乙醇。
(1)实验装置
图中仪器a的名称为
___________。反应过程中会产生少量PH
3气体,需使用封闭装置,用CuSO
4溶液吸收PH
3时会生成H
3PO
4和Cu,该反应的化学方程式为
________。
(2)药品用量
将2 g Fe粉、10 mL 3 mol·L
-1 H
2SO
4溶液加入烧瓶中反应。采取铁粉过量的原料配比的主要原因是
_________。
(3)制备FeSO
4溶液
保持温度70~80℃,至反应无明显气泡产生,停止加热,过滤,除去残留固体,滤液经
_________、
_________,过滤、洗涤、干燥,得到FeSO
4·7H
2O[已知:FeSO
4·7H
2O的溶解度随着温度升高增加程度大]。
(4)用途
①制备(NH
4)
2Fe(SO
4)
2·6H
2O
将FeSO
4·7H
2O溶于稀硫酸,向FeSO
4溶液中加入一定质量的(NH
4)
2SO
4固体,70~80℃条件下溶解后,趁热倒入50 mL乙醇中,继而析出晶体。上述过程中,溶于稀硫酸的目的是
_________,后续加入乙醇的作用为
_________。
②絮凝剂——聚合硫酸铁
向稀硫酸酸化的FeSO
4溶液中缓慢滴加H
2O
2,此时发生反应的离子方程式为
__________,继续在加热条件下反应一段时间,制得红棕色的聚合硫酸铁。