17. 硫酸亚铁铵晶体[(NH
4)
2Fe(SO
4)
2·6H
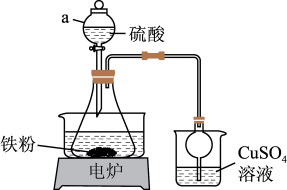
2O]俗称摩尔盐,用途十分广泛。实验室通常用如图所示装置制备FeSO
4溶液后,再与等物质的量的(NH
4)
2SO
4反应制备摩尔盐。
已知:硫酸亚铁铵晶体在空气中不易被氧化,易溶于水,不溶于乙醇。
(1)制备FeSO
4用图示装置制备FeSO
4。仪器a的名称是
___________,该实验不用明火加热的原因是
___________。将0.7g铁粉加入锥形瓶中,放入15mL1mol·L
−1H
2SO
4溶液,保持温度在50℃~60℃之间反应,待无明显气泡产生后停止加热,趁热过滤。
(2)制备摩尔盐
向滤液中加入适量(NH
4)
2SO
4饱和溶液,70℃~80℃水浴加热,保持溶液pH为1~2,蒸发浓缩至溶液表面出现晶膜,冷却至室温即得晶体,减压过滤,用乙醇洗涤晶体。蒸发浓缩时,如果溶液pH太高或用玻璃棒搅拌,均可能导致溶液变黄,其原因是
___________。选用乙醇洗涤晶体的目的是
___________。
(3)尾气吸收
由于加入的铁粉不纯,反应过程中会产生少量H
2S、PH
3气体,故需使用封闭装置。用CuSO
4溶液吸收H
2S时发生反应的离子方程式为
___________。
(4)产品检验
称取摩尔盐产品3.920g溶于稀硫酸中,转入100mL容量瓶定容。每次用移液管取25.00mL溶液放入锥形瓶,用0.02000mol·L
−1的KMnO
4溶液滴定(还原产物为Mn
2+,杂质不与KMnO
4反应),三次平均消耗24.30mL的KMnO
4溶液。
①滴定终点时的现象是
___________。
②酸性高锰酸钾溶液与Fe
2+反应的离子方程式是
___________。
③产品中(NH
4)
2Fe(SO
4)
2·6H
2O(相对分子质量为392)的质量分数为
___________。
④实验过程中的下列操作,可能导致测定结果偏高的是
___________(填标号)。
A.取用的晶体不够干燥
B.容量瓶定容时俯视刻度线
C.滴定管未用待盛溶液润洗
D.滴定完成后,滴定管尖嘴处留有气泡