23. Ⅰ.铁及其化合物在生产生活中有极其重要的用途。

可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将

转化为

,以利于人体吸收。为了验证这一猜想,设计了如下实验:
| 实验方案 | 实验现象 |
取适量 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 | 紫色褪去 |
(1)由上述实验能否得出“维生素C可将

转化为

”的结论?请说明理由:
______。
Ⅱ.高铁酸钾(

)是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于水而形成暗紫色溶液,静置后会分解并释放出大量氧气,同时生成KOH和

胶体。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法等。
(2)熔融法:在苛性碱存在的环境中,铁盐被过氧化钠高温氧化成高铁酸钠:
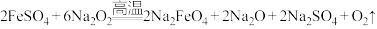
,再加入适量饱和KOH溶液反应得到

。上述反应在熔融状态下进行,而不在水溶液中进行的原因是
______。
(3)高铁酸钾可通过次氯酸钾氧化

溶液来制备。次氯酸钾的制备装置如图所示。
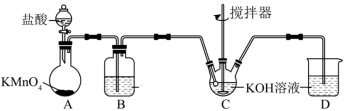
回答下列问题:
①装置A中

与盐酸反应生成

和

,其化学方程式为
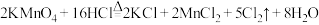
。
a.请用双线桥法标出电子转移方向与数目
_______。
b.上述反应中的HCl体现了什么性质?
_______。
②将制备的

通过装置B可除去杂质HCl,B中的溶液为
_____。
③

和KOH溶液在较高温度下反应生成

。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是
______。
④若实验制得的次氯酸钾溶液中

(N代表微粒个数),则
 _______
_______。
⑤装置D的作用是
_______。
⑥次氯酸盐氧化法是在碱性条件下,KClO饱和溶液可将

转化为

,写出反应的离子方程式:
________。